Clear Sky Science · sv
Rumslig mönstring av kontraktilitet genom ett självorganiserat mekanogenaktivitetsgradient ligger bakom Drosophila-gastrulation
Hur vävnader formar sig
Tidiga embryon förvandlar på något sätt enkla cellskikt till intrikata tredimensionella former. Denna studie ställer en grundläggande fråga bakom det knepet: hur samordnar celler var de ska dra ihop sig och böjas så att en vävnad viker sig på rätt plats och i rätt riktning? Genom att följa flugembryon med hög upplösning identifierar författarna en kemisk signal som beter sig som en ”mekanisk morfogen” och direkt mönstrar var cellerna drar i sig själva för att driva en avgörande veckningshändelse i utvecklingen.
En våg som veckar embryot
I fruktflugan Drosophila är ett viktigt steg i tidig utveckling gastrulation, när ett platt cellager buktar inåt för att börja bilda mag-tarmkanalen. Bakre delen av embryot, en cellfläck kallad den posteriora endodermprimordien, påbörjar denna process genom att kontrahera sina övre (apikala) sidor. Denna initiala böj startar en framåtriktad våg av invagination som sveper över intilliggande celler. Författarna visar att vågen är beroende av en signal kallad Fog, ett sekretoriskt molekyl som aktiverar en familj receptorer kända som GPCR:er, vilka i sin tur slår på cellens kontraktila maskineri byggt kring motorproteinet Myosin-II.
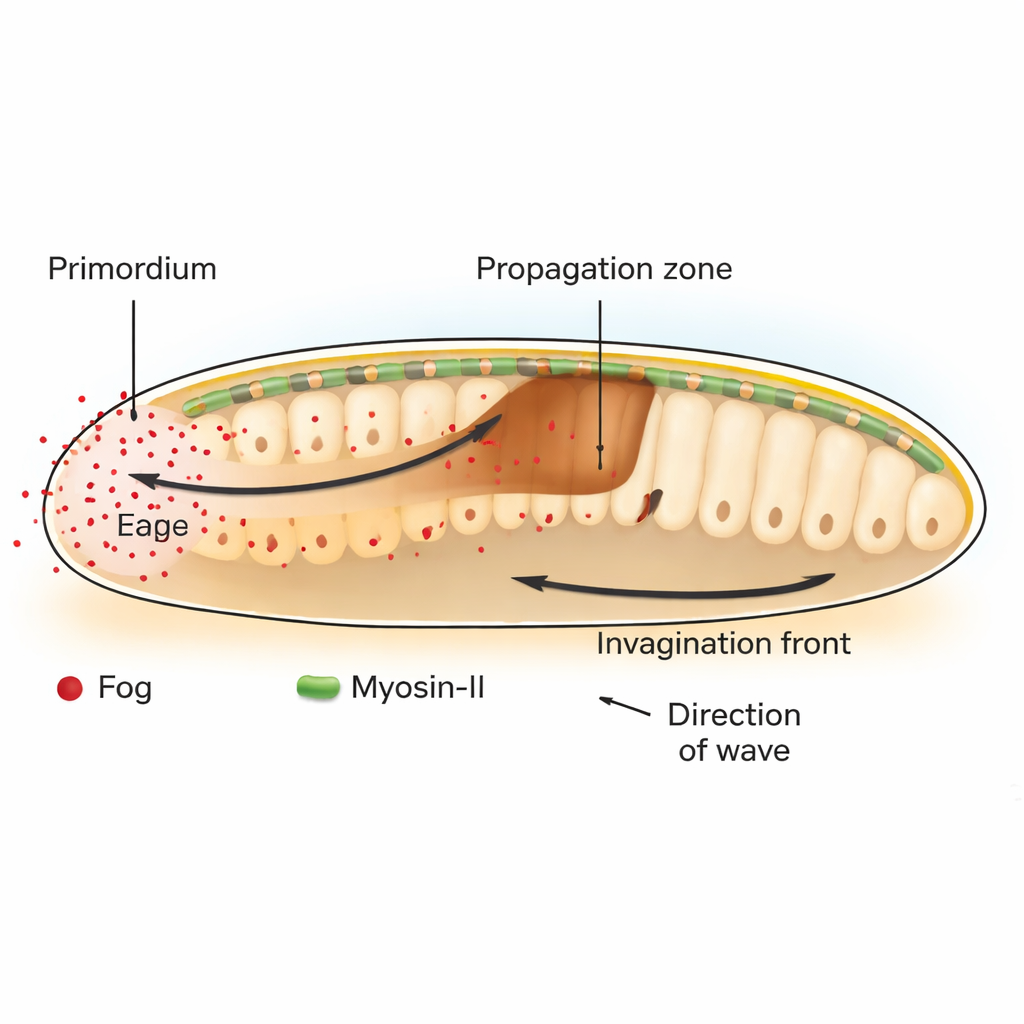
En kemisk som mönstrar kraft, inte öde
Traditionellt har utvecklingsbiologer fokuserat på ”morfogener”, diffunderande molekyler vars koncentrationsgradienter talar om för celler vilken identitet de ska anta. Här uppträder Fog annorlunda. Istället för att ändra vilken celltyp en region kommer att bli, justerar Fog direkt hur starkt cellerna kontraherar. Genom att selektivt återställa eller blockera Fog och dess nedströms budbärare Gα endast i vissa regioner visar forskarna att Fog som produceras i primordien är både nödvändig och tillräcklig för att utlösa Myosin-II-aktivering och vävnadsveckning på avstånd i den intilliggande propagationszonen. När Fog förankras så att den inte kan spridas krymper endast de producerande cellerna och invaginationsvågen stannar efter bara en eller två cellrader.
En dold gradient på cellytan
En naturlig idé är att Fog skulle bilda en klassisk koncentrationsgradient utanför cellerna. Med en fluorescensmärkt version av Fog och känsliga fluorescensmätningar finner teamet motsatsen: i det tunna vätskeskiktet mellan vävnaden och dess omslutande hölje (vitellinmembranet) är Fog anmärkningsvärt jämnt fördelad. Ändå bildar Myosin-II-aktiviteten tydligt en brant, framrusande gradient, starkast precis framför den framåtskridande vecket och avtagande några celldiametrar bort. Den saknade biten är att Fog inte verkar som en enkel bulkkoncentrationssignal; istället fastnar en liten andel Fog kortvarigt vid cellytan, binder sina GPCR-receptorer och bildar en ytbundet aktivitetsgradient trots att de fria Fog-molekylerna förblir jämnt utblandade i vätskan.
Receptorer, endocytos och adhesion formar vågen
Författarna visar att denna ytbundna Fog, tillsammans med sina receptorer, självorganiserar till ett mönster. Där Fog upprepade gånger möter receptorer främjar den receptor-klustring och aktivering, vilket rekryterar mer Myosin-II. En cellulär ”städprocess” — GPCR-endocytos — avlägsnar sedan aktiva komplex, förhindrar okontrollerad aktivering och hjälper till att finjustera hur långt signalen sprids. När denna endocytos genetiskt fördröjs blir Myosin-II-gradienten högre och bredare. En annan nyckelspelare är en uppsättning adhesionsmolekyler kallade integriner. När vävnaden böjs pressar cellerna framför vecket mot vitellinmembranet; denna kontakt aktiverar lokalt integriner, vilket i sin tur förstärker Fog–GPCR-signaleringens effektivitet. Regionen med stark integrinengagemang överensstämmer med utbredningen av Myosin-II-gradienten, och utan integriner blir vågen svag och kort räckvidd även om Fog-signaleringen i övrigt är förstärkt.
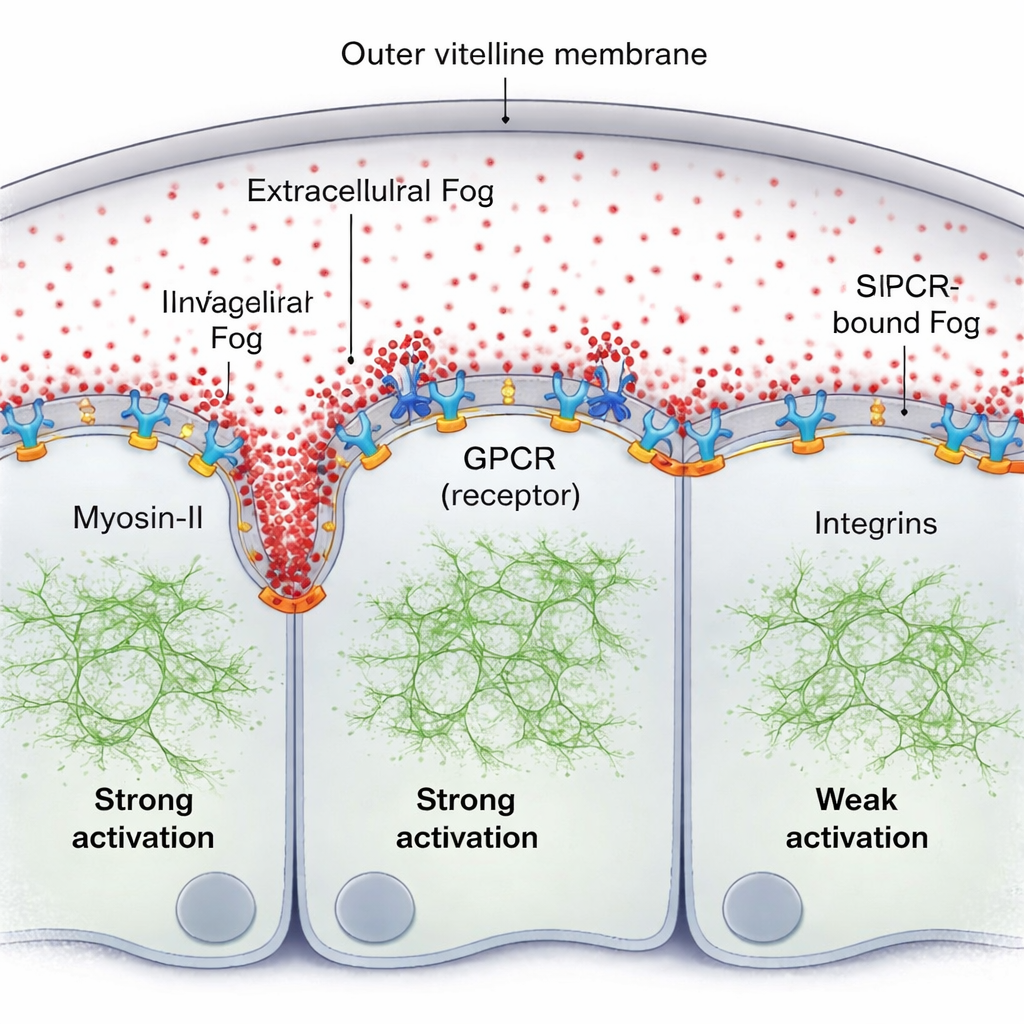
En självförnyande mekanisk pattern
För en icke-specialist är huvudbudskapet att embryot inte enbart förlitar sig på förritade kemiska kartor för att bestämma var det ska veckas. Istället bygger det upp ett rörligt mönster av mekanisk aktivitet i realtid. Fog sprids jämnt, men dess effektiva verkan skulpteras vid cellytan genom receptor-klustring, receptorborttagning och förändrad vävnadsgeometri när celler trycker mot omgivningen. Detta skapar en självorganiserad, framrusande gradient av kontraktil kraft som drar vävnaden inåt i en koordinerad våg. Arbetet ger ett konkret exempel på en länge teoretiserad ”mekanogen”: en diffunderande molekyl som direkt mönstrar de fysiska krafterna i en vävnad och bidrar till att förklara hur levande organismer så pålitligt formar sig under utvecklingen.
Citering: Mundhe, G., Dunsing-Eichenauer, V., Philippe, JM. et al. Spatial patterning of contractility by a self-organized mechanogen activity gradient underlies Drosophila gastrulation. Nat Commun 17, 1721 (2026). https://doi.org/10.1038/s41467-026-68418-z
Nyckelord: gastrulation, mechanogen, Drosophila-embryo, vävnadsmekanik, Fog-signalering