Clear Sky Science · sv
DNA-ändars konfigurationer styr bildandet av synaptiska komplex under NHEJ-medierad ändbro
När DNA går sönder måste celler agera snabbt
Varje dag blir DNA i våra celler rispat, klippt och attackerat av normal ämnesomsättning och yttre påfrestningar. Bland de farligaste skadorna finns dubbelsträngsbrott, där båda DNA-spiralens strängar går av. Om dessa brott inte repareras snabbt och korrekt kan celler dö eller, i värsta fall, röra sig mot cancer. Denna studie undersöker hur den exakta formen och kemin hos brutna DNA-ändar påverkar huruvida en nyckelreparationsväg, kallad icke-homolog ändinfogning (NHEJ), för samman dessa ändar effektivt och med så få fel som möjligt.
Två sätt att föra ihop brutet DNA
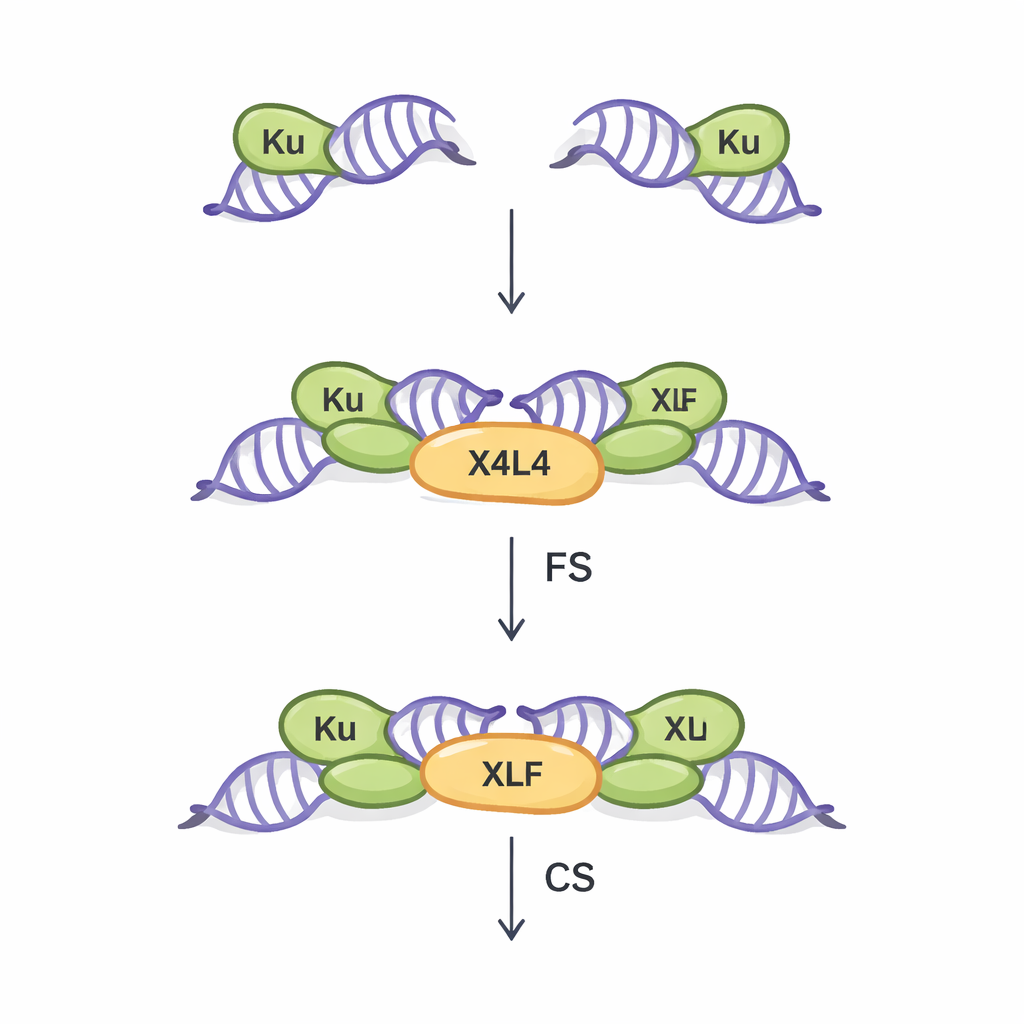
NHEJ är huvudvägen för reparation av dubbelsträngsbrott i de flesta av kroppens celler. Den fungerar utan behov av en matchande DNA-mall, vilket gör den snabb men något felbenägen. Det första avgörande steget i denna väg kallas synaps: att fysiskt föra de två brutna DNA-ändarna samman så att de senare kan fogas ihop. Tidigare arbete, mestadels med idealiserade rakade (blunt) DNA-ändar, visade två typer av synaptiska uppsättningar. I det "flexibla synaptiska" (FS) tillståndet hålls ändarna nära varandra och kan röra sig, prova parningar. I det "nära synaptiska" (CS) tillståndet ligger ändarna linje mot linje och är redo att förseglas av ett ligasenzym. Tre kärnproteiner — Ku, XRCC4–Ligase IV (tillsammans kallade X4L4) och XLF — har länge ansetts samordna denna process, men hur verklighetstrogna, oregelbundna DNA-ändar påverkar vilket synaptiskt tillstånd som bildas har hittills varit dåligt förstått.
Ändform och korta matchningar styr reparationsvägen
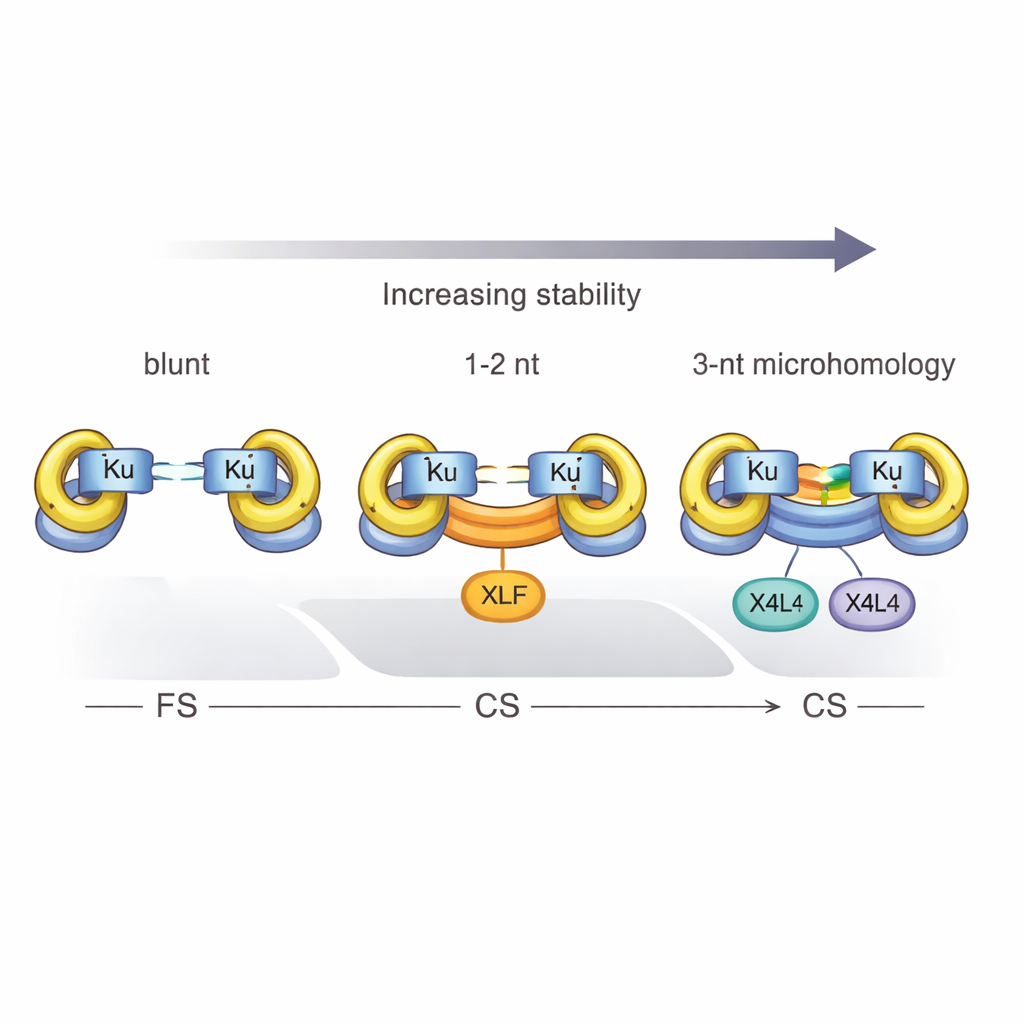
Forskarna använde single-molecule FRET, en fluorescensbaserad teknik som spårar avstånd i nanometernivå, för att iaktta enskilda DNA-molekyler när de fördes samman av NHEJ-proteiner. De jämförde enkla rakade ändar med mer realistiska ändar som bar korta överhäng — små enkelsträngade svansar som potentiellt kan para med varandra. De fann att när överhängen är komplementära, även bara genom några få baser, ökar chansen dramatiskt att ett nära synaptiskt komplex bildas. Faktum är att tre matchande baser av "mikrohomologi" vid brottet räckte för att Ku och X4L4 ensamma skulle skapa ett stabilt CS-komplex, utan behov av XLF. Detta visar att DNA:t självt kan bidra med en del av den energi och vägledning som normalt tillhandahålls av hjälpproteiner.
Hur små DNA-flikar hjälper till att stabilisera bron
Genom att analysera distinkta FRET-signaturer avslöjade teamet minst två strukturella varianter av det nära synaptiska tillståndet för ändar med överhäng. I den ena parar överhängens allra spetsar med varandra och bildar ett nicks eller ett gapat fogar. I den andra trycks skarvarna där dubbelsträngat DNA möter enkelsträngade överhäng ihop i en rak linje, medan överhängen flippas ut som små flikar. Dessa flikar tillåter fortfarande basparning och håller ändarna mycket nära varandra, vilket sannolikt stabiliserar komplexet och ger enzymer utrymme att trimma eller förlänga DNA:t efter behov innan slutlig försegling. Intressant nog påverkade vanlig oxidativ skada i överhängen, såsom 8-oxoguanin, bara måttligt denna process, vilket betonar hur robust NHEJ är mot vissa typer av skada.
Proteiner, fosfater och kraften i tre
Studien definierade också en tydlig tröskel: minst tre komplementära baspar krävs för att Ku och X4L4 pålitligt ska kunna omvandla ett flexibelt komplex till ett nära. Med bara en eller två matchningar stannar systemet mestadels i det flexibla tillståndet om inte XLF kommer in och hjälper till att klämma ihop ändarna. Kemiska detaljer spelar också roll. När det brutna DNA:t bär en 5′-fosfatgrupp — en normal egenskap hos många fysiologiska brott — blir synapsen mer effektiv och nära komplex är mer benägna att verkligen ligeras, vilket förvandlar en tillfällig bro till en permanent reparation. Denna fosfatökning kan dock inte helt ersätta den stabiliserande effekten av basparning vid brottet.
Varför detta är viktigt för hälsa och genredigering
I vardagligt språk visar detta arbete att brutna DNA-ändar inte är passiva offer som väntar på att bli åtgärdade. Deras exakta former, små fläckar av matchande sekvens och kemiska taggar vägleder aktivt hur reparationsproteiner griper, alignerar och återansluter dem. När tre eller fler matchande baser finns hjälper DNA-ändarna själva till att låsa brottet i en reparationsfärdig konfiguration, vilket ibland gör vissa hjälpproteiner valfria. När sådana matchningar är sällsynta blir extra proteinfaktorer nödvändiga. Dessa insikter hjälper till att förklara varför vissa brott lagas prydligt medan andra leder till små mutationer eller omstruktureringar. De erbjuder också ledtrådar för att förbättra genredigeringsverktyg som CRISPR, där avsiktligt skapade DNA-brott repareras av samma NHEJ-maskineri. Genom att finjustera ändarna på dessa brott kan forskare bättre kontrollera hur genomet formas om.
Citering: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
Nyckelord: Reparation av DNA-dubbelsträngsbrott, icke-homolog ändinfogning, DNA-synaps, mikrohomologi, genomstabilitet