Clear Sky Science · sv
En enda valin–till–leucin-ändring stör Plasmodium falciparum AP2-G:s DNA-bindning och avslöjar GDV1:s roll i ap2-g-aktivering
Hur malariaparasiter fattar ett livsavgörande val
Malariaparasiter i vårt blod står ständigt inför ett livsavgörande beslut: fortsätta föröka sig inom en värd eller växla till en form som kan hoppa till nästa värd via ett myggbett. Denna studie avslöjar hur en enda liten förändring i ett parasitprotein helt kan stänga av det infektiösa, myggredo stadiet, vilket öppnar nya möjligheter att blockera malariasmitta.
Parasitens vägskäl
I blodomloppet fokuserar Plasmodium falciparum mest på snabb tillväxt, vilket orsakar sjukdom. Men en liten minoritet omvandlas till sexuella former kallade gametocyter, de enda stadier som myggor kan plocka upp och föra vidare. Hur bara några parasiter i en population gör denna omställning har länge varit ett mysterium. Tidigare arbete visade att två parasitproteiner, GDV1 och ett DNA-bindande protein kallat AP2-G, ligger i hjärtat av beslutet. GDV1 hjälper till att väcka det normalt tysta ap2-g-genet, och AP2-G aktiverar i sin tur en rad gener som driver sexuell utveckling. Den aktuella studien avsåg att undersöka ett annat protein, en kinas kallad STK2, men råkade istället på en mycket mer dramatisk upptäckt i AP2-G självt.
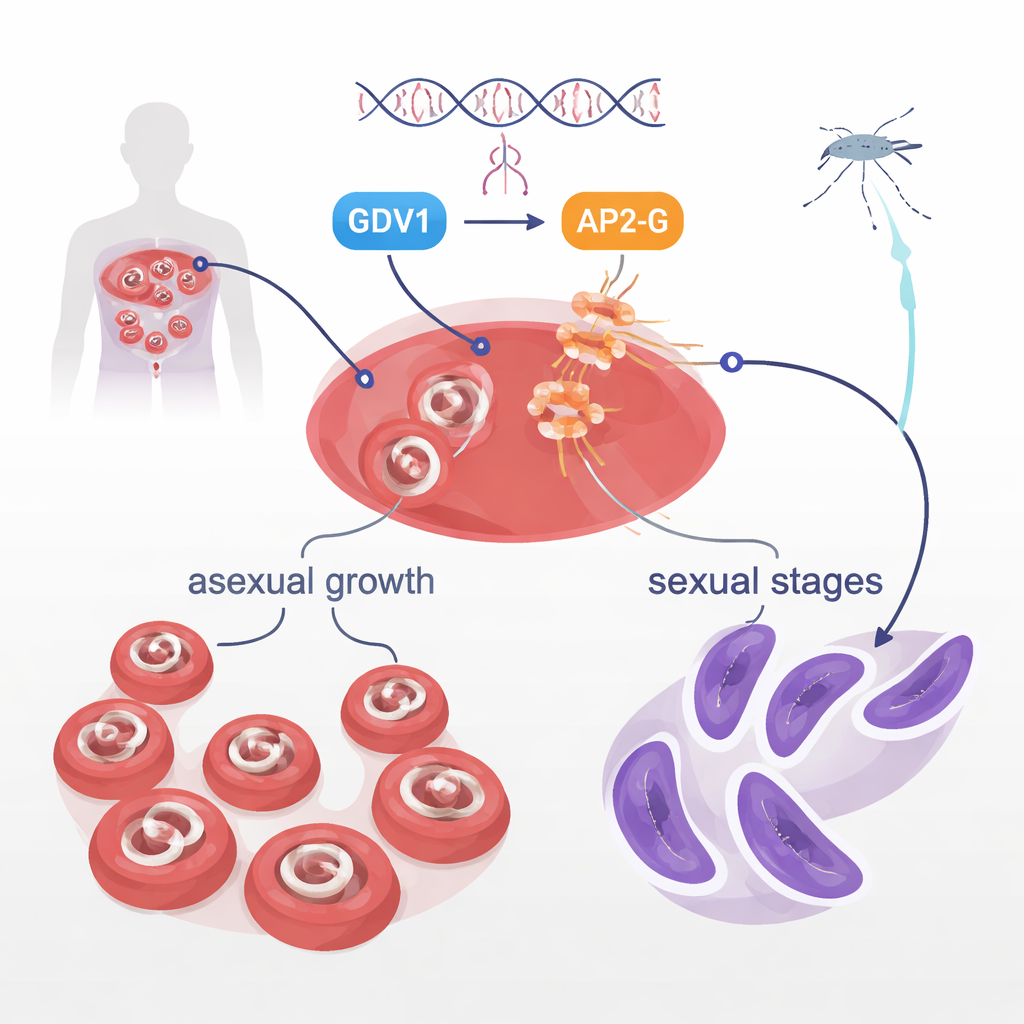
En enda aminosyra som stoppar transmission
När forskarna raderade stk2-genen i en labbparasitsstam märkte de att dessa parasiter helt förlorade förmågan att bilda gametocyter, samtidigt som de fortfarande växte asektuellt utan problem. Överraskande nog bildades gametocyter normalt när liknande manipulationer upprepades i en annan stam. Helgenomssekvensering avslöjade den dolda boven: en enda ”bokstavs”-ändring i ap2-g-genet som bytte ut en aminosyra, valin, mot en mycket liknande leucin vid position 2163. Denna position ligger i början av AP2-G:s DNA-bindande region, den del som fysiskt greppar specifika DNA-motiv för att slå på gener. Denna lilla valin–till–leucin-växling räckte ensam för att avskaffa gametocytbildning. När forskarna åstadkom denna mutation i annars normala parasiter försvann gametocyterna; när de återställde valin återkom den sexuella utvecklingen helt.
Hur bytet förstör den molekylära låsen
För att förstå varför denna subtila förändring är så förödande kombinerade teamet datorbaserad modellering med laboratorieexperiment. Strukturella förutsägelser antydde att ersättning av valin med leucin förskjuter och destabliserar den precisa formen av AP2:s DNA-bindande domän. I provrörsbaserade analyser med renade proteiner band normal AP2-G starkt till sin föredragna DNA-sekvens, en kort kod innehållande motivet ”GnGTAC.” I kontrast lyckades den mutanta AP2-G med leucin vid position 2163 inte binda denna sekvens alls. Utan stabil DNA-bindning kunde AP2-G varken slå på sitt eget gen (en positiv återkopplingsslinga känd som autoreglering) eller aktivera dussintals downstream-gener som behövs för att driva parasiter in i den sexuella vägen. Funktionellt blev de mutanta parasiterna ”sterila”: de kunde inte bilda de former som infekterar myggor, även om de fortfarande frodades i röda blodkroppar.
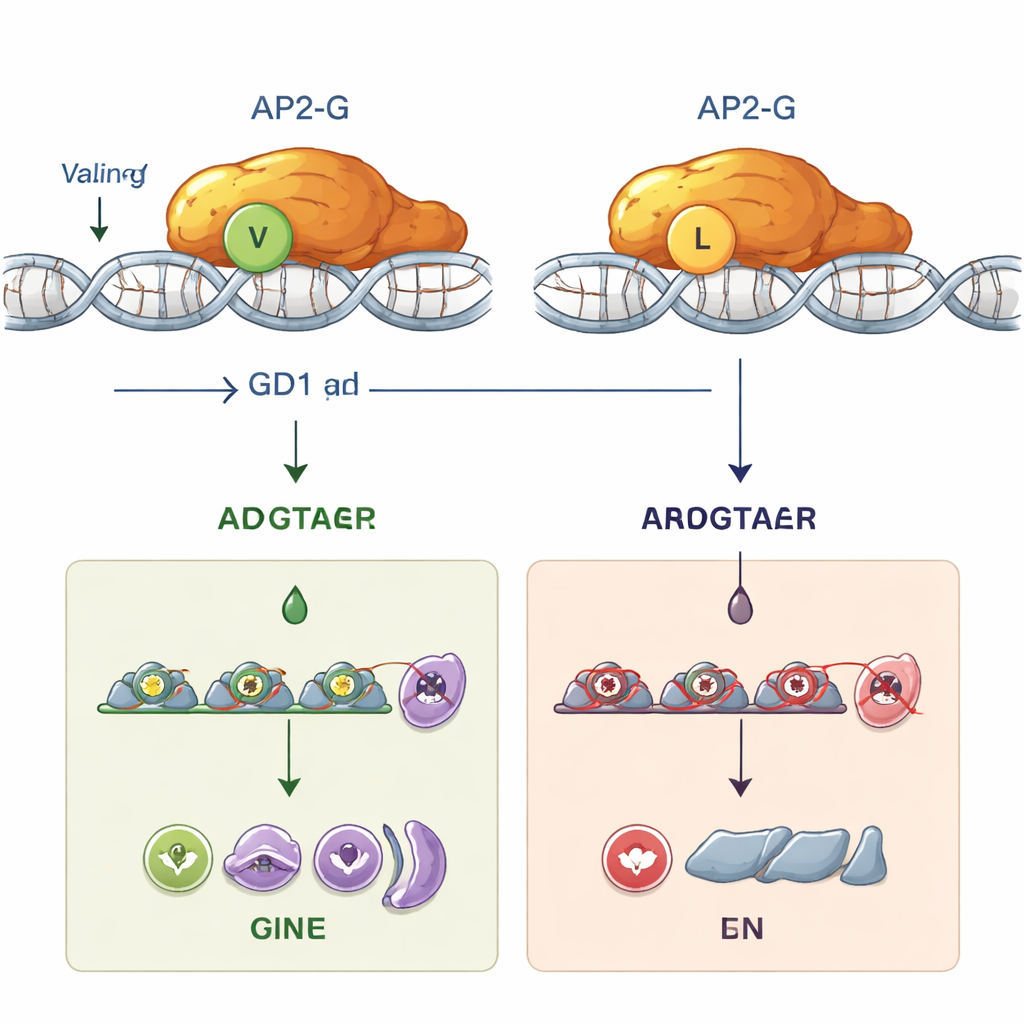
GDV1:s dolda roll innan AP2-G tar över
Mutationen gav också forskarna ett unikt verktyg: parasiter där ap2-g-genet kan slås på, men AP2-G inte kan binda DNA. Med hjälp av lysande och luminescerande rapportörer följde de när olika aktörer agerar under parasitens 48-timmarscykel i röda blodkroppar. De fann att GDV1-proteinet dyker upp först, tidigt i ett stadium kallat schizogoni, och är nödvändigt för att kickstarta ap2-g-uttrycket från dess tysta tillstånd. Denna tidiga aktivering skedde oavsett om ap2-g kodade för normal AP2-G eller den mutanta versionen. Först senare, när tillräckligt med normal AP2-G byggts upp, uppstod den starka självförstärkande slingan och aktiveringen av andra ”sexuella” gener. En viktig markör, ett protein kallat MSRP1, tändes endast i parasiter med funktionell AP2-G, vilket gav ett praktiskt sätt att skilja tidigt och sent sexuellt kommiterade parasiter. I mutanta linjer med leucinbytet kunde GDV1 fortfarande väcka ap2-g, men det brutna AP2-G-proteinet kunde inte föra processen vidare, så den sexuella utvecklingen stannade av.
Konsekvenser för att stoppa malariaspridning
För en allmän läsare är slutsatsen enkel: malariaparasiter förlitar sig på ett extremt känsligt molekylärt lås för att avgöra om de blir smittsamma. Denna studie visar att ändra bara en ”tand” i det låset—en enda valin i AP2-G:s DNA-gripande region—hindrar parasiten från att nå de mygginfektiösa stadierna. Samtidigt klargör den att ett annat protein, GDV1, verkar tidigare som nyckeln som först låser upp det tysta ap2-g-genet, innan AP2-G stärker sin egen produktion och aktiverar ett bredare sexuellt program. Genom att kartlägga denna händelseföljd och skapa rapportörparasiter som lyser när varje steg inträffar, ger arbetet kraftfulla verktyg för att screena läkemedel eller mänskliga faktorer som stör sexuell commitment. På lång sikt kan riktade angrepp mot AP2-G:s DNA-bindande region eller GDV1-drivna aktiveringssteg utgöra grunden för nya strategier som inte bara botar malaria hos en patient utan kapar hela smittkedjan.
Citering: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
Nyckelord: malariatransmission, Plasmodium falciparum, gametocytutveckling, AP2-G, GDV1