Clear Sky Science · sv
Multimodal AI för opportunistisk screening, stadieindelning och riskstratifiering av progress för steatotisk leversjukdom
Varför leverfett och ärrbildning är viktiga för alla
Fettleversjukdom är inte längre sällsynt eller nischad: ungefär en av tre vuxna globalt har förhöjt fettinnehåll i levern, och andelen ökar. Hos många förblir det tyst, men hos andra leder det till farlig ärrbildning (fibros), skrumplever, levercancer och hjärtproblem. Samtidigt genomgår miljontals människor redan CT‑undersökningar av andra skäl—bröstsmärta, uppföljning av cancer eller rutinundersökningar—utan att någon noggrant granskar levern. Denna studie ställer en enkel men kraftfull fråga: kan artificiell intelligens (AI) i tysthet skanna de befintliga bilderna, flagga dold leversjukdom och hjälpa läkare att agera innan allvarliga skador uppstår?
En ny AI‑assistent byggd på verkliga sjukhusdata
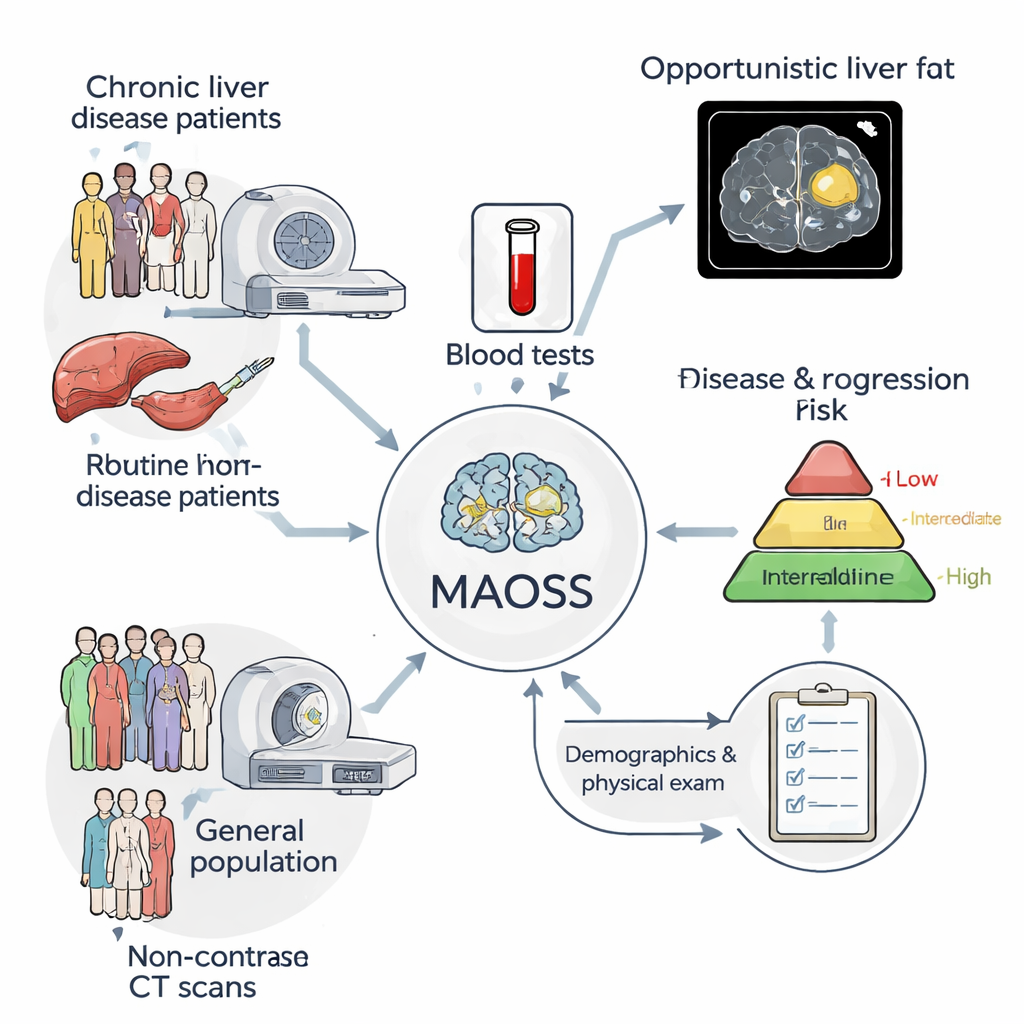
Forskarna utvecklade ett multimodalt AI‑system kallat MAOSS (Multi‑modal AI for Opportunistic hepatic Steatosis Screening). Istället för att förlita sig på en enda typ av information kombinerar MAOSS tre källor: 3D‑CT‑bilder utan kontrast av levern, standardprovresultat från blodprov och grundläggande kliniska uppgifter som ålder och kroppsstorlek. Teamet tränade systemet på mer än 2 000 patienter från ett stort kinesiskt sjukhus, inklusive nästan 1 000 vars levervävnad undersökts i mikroskop (guldstandarden) och över 1 100 vars skanningar hade detaljerade radiologiska rapporter. Denna blandning gjorde det möjligt för AI att lära sig både från de mest precisa etiketteringarna (biopsier) och från de bredare, lättare att samla in rapporterna som används i daglig praxis.
Att lära AI att känna igen både fett och ärrvävnad
MAOSS utformades för att svara på två nyckelfrågor från varje CT‑skanning: hur mycket fett finns i levern (steatos) och hur avancerad eventuell ärrbildning är (fibros). För att göra detta behandlar modellen sjukdomsstadier som en ordnad stege—from ingen, via mild och måttlig, till svår—and lär sig placera varje patient på rätt steg. En särskild ”multimodal” konstruktion låter systemet flexibelt hantera ofullständig information; till exempel kan det fortfarande fungera när vissa blodprov saknas och då förlita sig mer på bildmaterialet. Forskarna lade också till ett förklaringsverktyg baserat på ”integrerade gradienter” som framhäver specifika regioner och tätheter i leverbilden som mest påverkar AI:ns beslut, vilket ger kliniker en värmekarta över misstänkta fettförändringar.
Hur väl MAOSS presterar jämfört med nuvarande verktyg
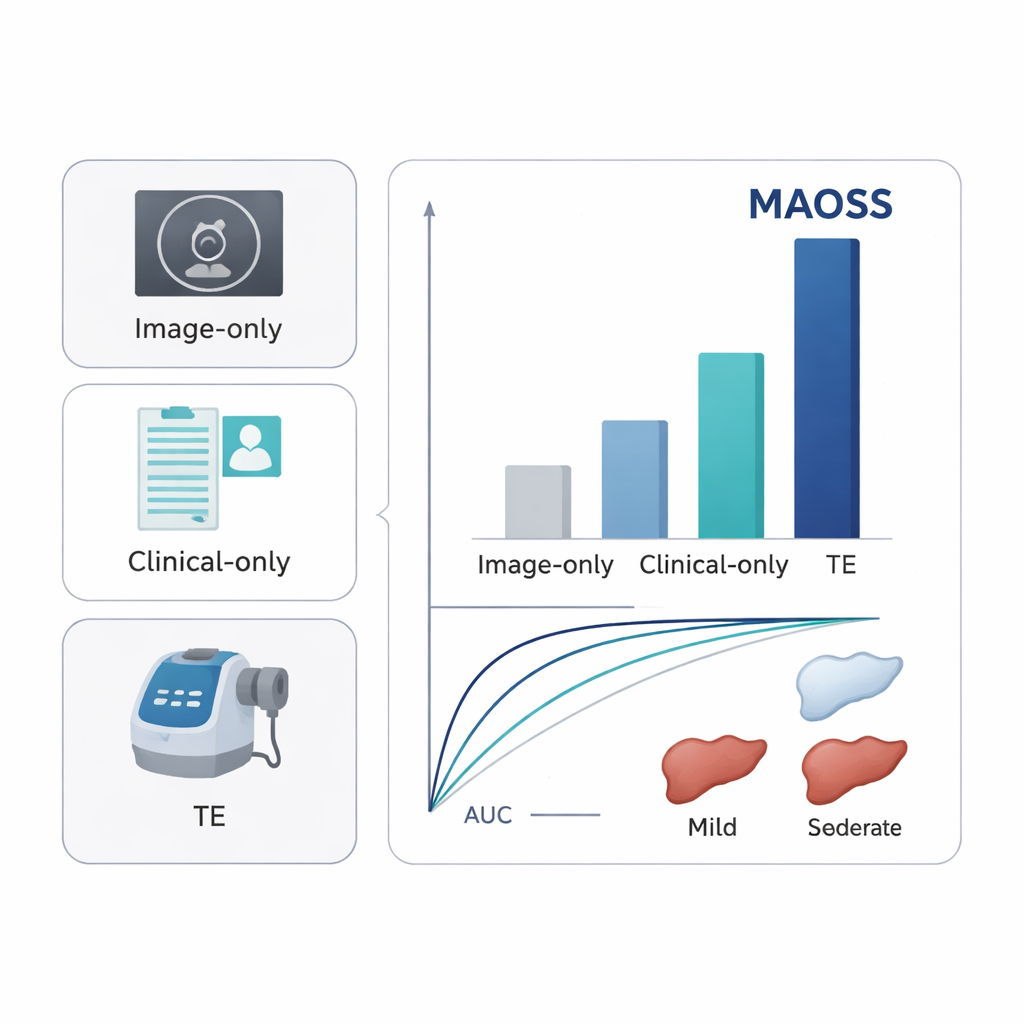
När MAOSS testades på separata patientgrupper från flera sjukhus—inklusive en extern kohort och en grupp med MR‑baserade leverfettmätningar—visade systemet hög noggrannhet även för att upptäcka mild leversteatos, med areor under ROC‑kurvan (AUC) kring 0,90–0,93. Det presterade också väl vid identifiering av kliniskt betydelsefull fibros, med AUC‑värden runt 0,82–0,89. Dessa resultat var konsekvent bättre än modeller som endast använde bilder, endast kliniska data eller standardmått från ultraljud såsom transient elastografi. I en läsarstudie med 11 radiologer fungerade MAOSS som assistent: när läkarna såg AI‑poängen tillsammans med CT‑bilden förbättrades deras förmåga att upptäcka tidig fettleversjukdom märkbart, särskilt när det gällde att skilja normala levervärden från subtil sjukdom.
Att förvandla rutinundersökningar till ett tidigt varningsnätverk
Teamet undersökte sedan hur MAOSS kan fungera i den röriga verkligheten i vardagsmedicin. De tillämpade systemet på mer än 18 000 verkliga CT‑skanningar från akutmottagningar, inneliggande patienter, öppenvård och hälsokontroller, de flesta ursprungligen beställda av skäl som inte rörde levern. MAOSS:s bedömningar av ”fettlevern” kontra ”ingen fettlevern” överensstämde väl med radiologernas rapporter, särskilt i större hälsokontrollkohorter. Därefter integrerade de MAOSS i en etablerad klinisk riktlinje som bestämmer vilka patienter med fettlevern som bör remitteras till specialistvård. I en biopsibekräftad grupp om 1 192 personer identifierade den MAOSS‑förstärkta vårdvägen cirka en tredjedel fler patienter med risk för att utveckla steatohepatit eller avancerad fibros än standardmetoden baserad endast på ultraljudsmått, samtidigt som den tryggt uteslöt låg‑riskindivider.
Vad detta betyder för patienter och framtida vård
För en lekman är huvudbudskapet att samma CT‑undersökningar som redan görs för andra hälsoproblem kan fungera som ett tyst screeningsystem för leversjukdom, utan extra besök eller invasiva ingrepp. Genom att automatiskt tolka CT‑bilder tillsammans med rutinblodprover kan MAOSS upptäcka fettlevern och oroande ärrbildning tidigare än traditionella metoder, hjälpa radiologer att se subtil sjukdom de annars kan missa och mer exakt dela in patienter i låg, mellan och hög risk för progression till skrumplever. Författarna påpekar visserligen att större och längre studier behövs och att AI inte är felfri, men deras resultat tyder på att multimodal AI kan bli en viktig del i att förebygga svår leversjukdom innan den tyst progredierar.
Citering: Gao, Y., Li, C., Chang, W. et al. Multi-modal AI for opportunistic screening, staging and progression risk stratification of steatotic liver disease. Nat Commun 17, 1562 (2026). https://doi.org/10.1038/s41467-026-68414-3
Nyckelord: fettleversjukdom, medicinsk AI, CT‑bildgivning, leverfibros, opportunistisk screening