Clear Sky Science · sv
Hierarkiska mekanismer styr rensningen av DNA-skada–stannad RNA-polymeras II
När genkopieringsmaskiner stöter på ett hinder
Varje sekund färdas miljontals små molekylära maskiner kallade RNA-polymeras II längs vårt DNA och kopierar gener till RNA. Men när DNA skadas – till exempel av ultraviolett (UV)-ljus från solen – kan dessa maskiner tvärstanna. Om de stannade kopiorna hopar sig kan celler inte längre läsa sina gener korrekt, vilket är särskilt farligt för hjärnceller och kan leda till sällsynta sjukdomar som Cockayne-syndrom. Denna studie avslöjar i detalj hur våra celler känner igen dessa blockerade maskiner och antingen startar om dem eller avlägsnar dem innan de orsakar bestående skada.
Ett nytt sätt att övervaka cellulära trafikstockningar
För att förstå hur celler rensar blockerade polymeraser byggde forskarna en tidsupplöst ”trafikkamera” för transkription. De använde ett läkemedel som tillåter befintliga RNA-polymeras II-molekyler att fortsätta röra sig men förhindrar att nya startar, och skapade sedan en liten fläck med UV-skada inne i varje cellkärna. Genom att följa en specifik kemisk markör på polymerasets aktiva form kunde de se hur snabbt det försvann från det skadade området jämfört med resten av genomet. Parallellt utvecklade de ett kompletterande test som mätte den totala mängden aktivt polymeras i cellextrakt, vilket avslöjade inte bara när polymeraser lämnade DNA utan också när de bröts ner av cellens avfallssystem.
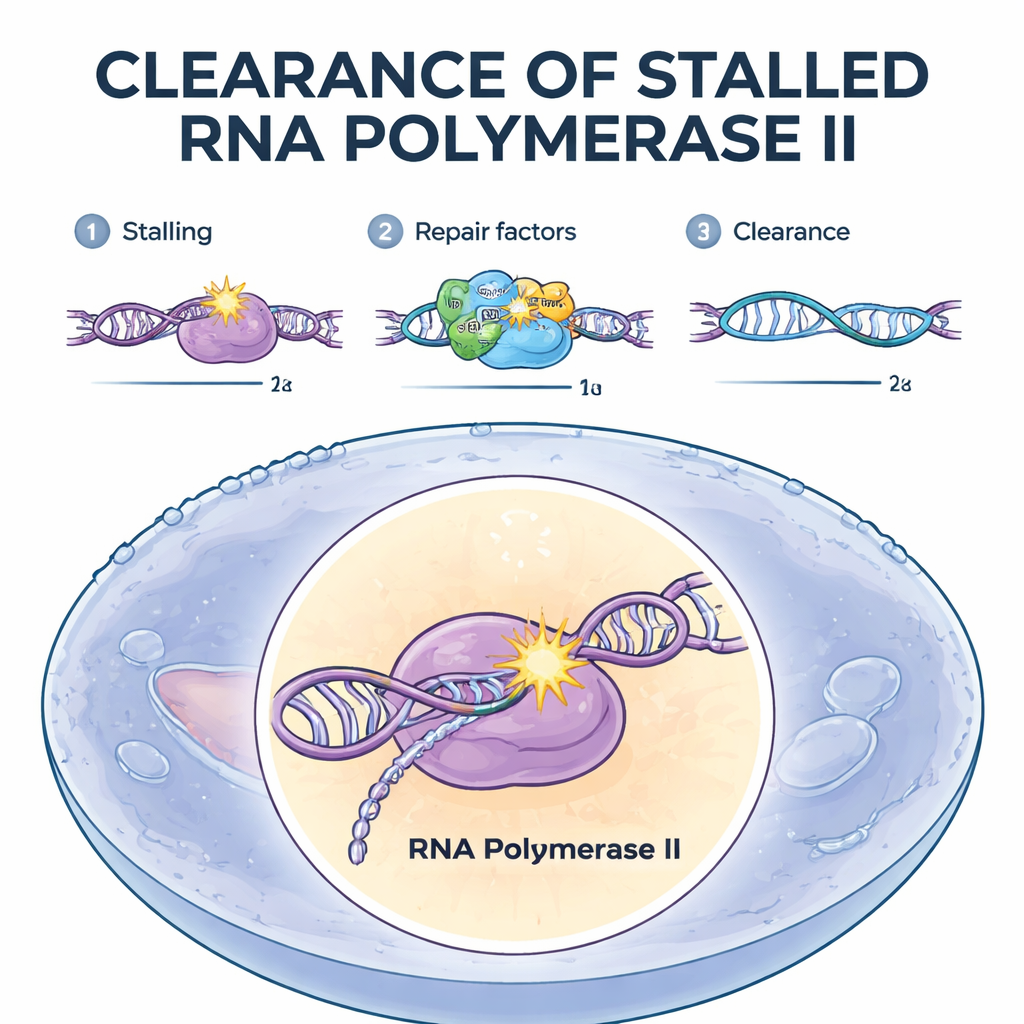
Tagga de stannade maskinerna för borttagning
Teamet inriktade sig på transkriptionskopplad reparation, ett specialiserat reparationssystem som åtgärdar lesioner på aktivt lästa gener. De använde en matchad uppsättning humana cellinjer, där varje linje saknade en särskild reparationsfaktor. Två proteiner, CSB och CSA, framträdde som avgörande grindvakter. När någon av dem saknades ackumulerades RNA-polymeras II och stannade envist vid skadeställena, och cellen misslyckades med att bryta ner det. Biokemiskt kunde dessa celler inte heller fästa små ubiquitin-taggar på en nyckelplats på polymeraset. I kontrast rensade celler som saknade senare reparationsproteiner – de som skär ut och ersätter det skadade DNA:t – polymeraset normalt. Detta visade att den inledande ubiquitin-märkningen av det stannade polymeraset är den kritiska utlösaren för att bestämma dess öde.
Två städkrafter: en snabb, en som reserv
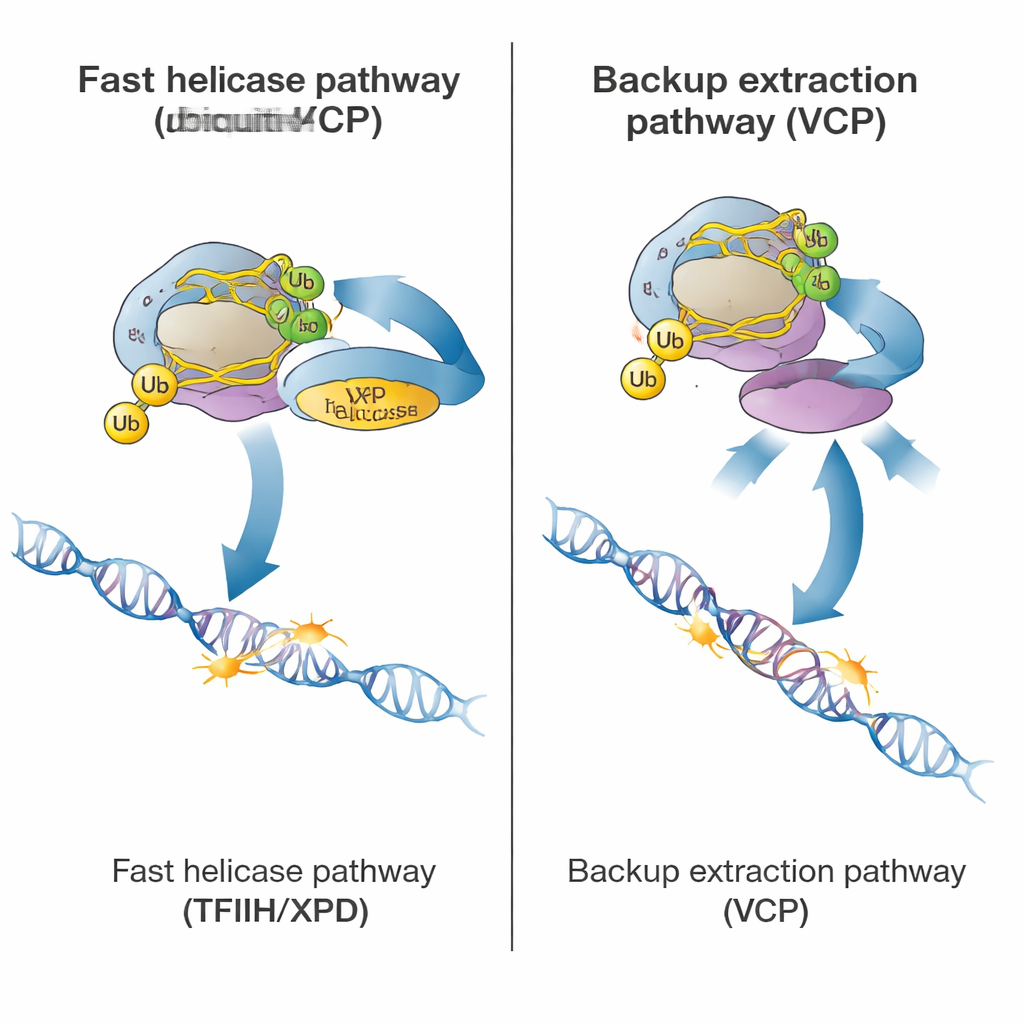
När polymeraset är märkt kan cellen välja mellan två sätt att rensa det. Den primära, snabba vägen förlitar sig på ett stort reparationskomplex kallat TFIIH, särskilt dess XPD-helicassubenhet, som använder energi för att veckla upp DNA. Hjälpproteiner, inklusive ELOF1, UVSSA och STK19, för TFIIH till det stannade polymeraset och positionerar XPD på DNA precis framför det. Med nya tester i patientceller som bär en helicas-dödande XPD-mutation visade författarna att när XPD inte kan veckla upp DNA, saktar polymerasrensningen dramatiskt, även om resten av reparationsmaskineriet finns på plats. Detta indikerar att den mekaniska dragkraft som XPD utövar normalt är det som ”skakar” loss polymeraset från lesionen så att reparationsenzym kan nå den skadade platsen.
En långsam men nödvändig plan B
Studien avslöjade också en långsammare, nödrutt för rensning av stannat polymeras. Denna väg är beroende av VCP (även känd som p97), ett protein som känner igen ubiquitin-taggar och kan med kraft dra ut proteiner från kromatinet. I friska celler med fullt fungerande TFIIH hade blockering av VCP endast en marginell effekt. Men i celler där TFIIH saknades, var felpositionerat eller hade en helicas-död mutation, blev polymerasrensningen nästan helt beroende av VCP. I dessa situationer kunde VCP fortfarande dra det märkta polymeraset bort från DNA, även när normal reparation inte kunde fortsätta. Avgörande var att denna reservväg fortfarande krävde viss ubiquitin-märkning, vilket förklarar varför celler som saknar CSB eller CSA – och därmed ubiquitin-märken – misslyckades i både huvud- och reservvägarna.
Varför detta är viktigt för hälsa och sjukdom
Tillsammans skisserar arbetet ett hierarkiskt säkerhetsprogram som celler använder närhelst RNA-polymeras II stöter på DNA-skada. Först flaggar CSB och CSA den stannade maskinen med ubiquitin. Om allt fungerar korrekt lösgör TFIIH och dess XPD-helicase snabbt polymeraset så att lesionen kan skäras ut och repareras. Om TFIIH inte kan utföra sitt arbete går VCP in för att extrahera polymeraset och skicka det för nedbrytning, vilket förhindrar att det blockerar genuttryck även om själva DNA-skadan består. Detta ramverk hjälper till att förklara varför ärftliga fel i CSB eller CSA orsakar särskilt allvarliga neurologiska problem: utan ubiquitin-märkning förlorar cellerna både den primära reparationsdrivna vägen och reservutdragningsvägen, vilket lämnar stannade polymeraser fast på skadade gener och leder till kronisk blockering av transkription.
Citering: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
Nyckelord: transkriptionskopplad DNA-reparation, RNA-polymeras II, UV-inducerad DNA-skada, proteinubiquitylering, Cockayne-syndrom