Clear Sky Science · sv
Ett nanosystem som riktar sig mot vävnadsinhibitor av metalloproteinas‑1 för kontinuerlig spatiotemporal behandling av idiopatisk lungsfibros
Varför envis lungsärrbildning spelar roll
Idiopatisk lungsfibros (IPF) är en obeveklig lungsjukdom där normal, svamp‑liknande lungvävnad långsamt ersätts av stel ärrvävnad. Personer med IPF blir andfådda vid vardagliga aktiviteter, och de flesta överlever bara några år efter diagnos. Dagens läkemedel kan hos vissa bromsa sjukdomen, men de återställer sällan redan uppkommen ärrvävnad och ger ofta biverkningar. Denna studie undersöker en smart, inhalerad ”nano‑terapi” utformad för att inte bara bromsa IPF utan också aktivt rensa ärrvävnad och hjälpa lungorna att reparera sig själva.
Problemet: klibbiga ärr och kemisk stress
I IPF fylls de utrymmen där syre normalt förs över till blodet av överskott av proteiner som kollagen, vilket omvandlar flexibla luftblåsor till styva partier. Författarna fokuserade på ett protein kallat TIMP‑1, som fungerar som en broms på de naturliga enzymer som normalt bryter ner överflödigt kollagen. Genom att undersöka lungprover från patienter och från möss med framkallad lungsärrbildning fann de att TIMP‑1‑nivåerna var flera gånger högre än i friska lungor och ökade i takt med kollagenuppbyggnaden. Samtidigt visade skadade lungor förhöjda nivåer av reaktiva syreradikaler (ROS) — kemiska ”gnistor” som skadar celler — och en förlust av viktiga markörer för friska luftblåsors celler. Dessa fynd pekade tillsammans på en ond cirkel: för mycket TIMP‑1 bromsar ärrnedbrytning, medan oxidativ stress ytterligare skadar lungstrukturen.
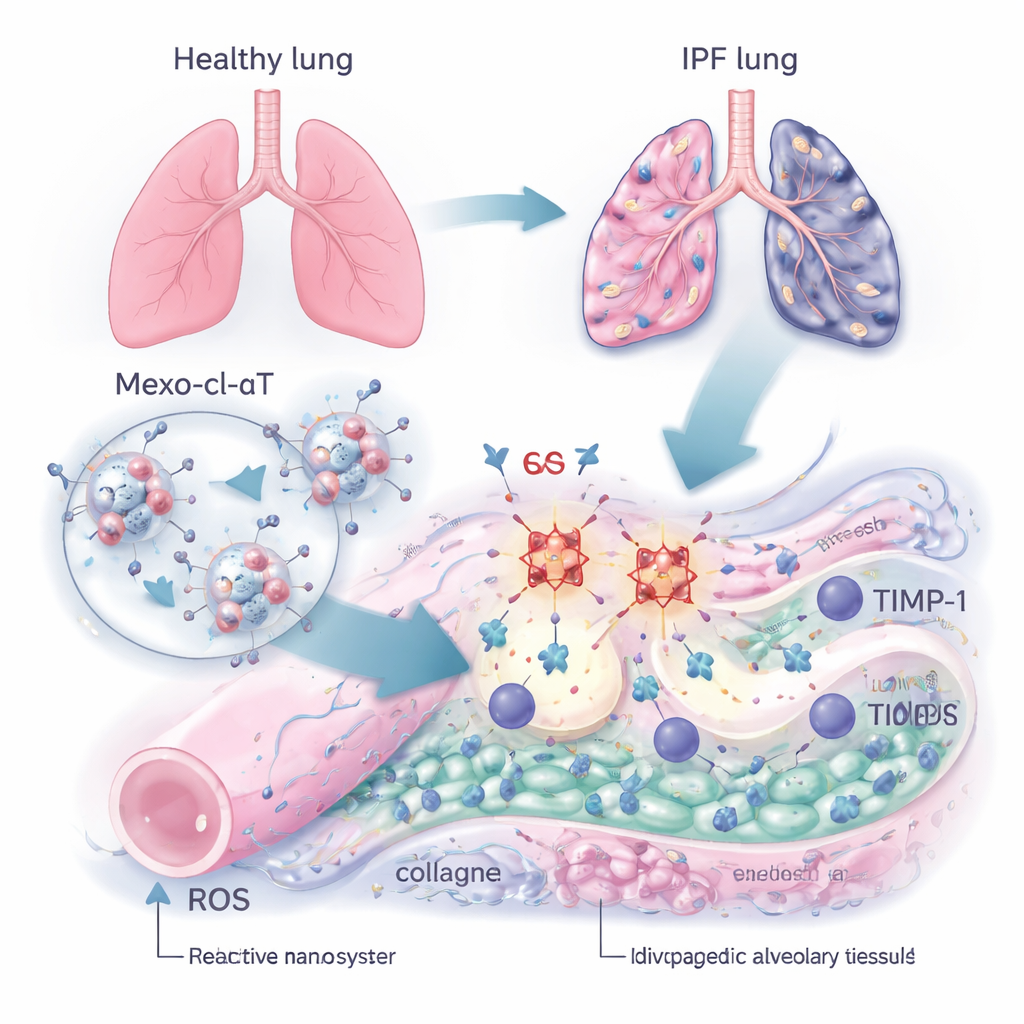
En smart leveransfordon: små reparationspaket
För att bryta denna cykel konstruerade teamet en nanoskala‑terapi kallad Mexo‑cl‑aT. De började med exosomer — naturliga, bubbelliknande partiklar som frigörs av stamceller och som redan är kända för att söka sig till skadad vävnad och stödja läkning. På ytan av dessa exosomer fäste de antikroppar som specifikt binder TIMP‑1. Kopplingen mellan exosomen och antikroppen gjordes med en speciell kemisk länkare som kan klippas av av ROS. Med andra ord används det hårda kemiska miljön i en ärrad lunga som en signal: när exosomen når en skadad region rik på ROS bryts länkaren, en del av ROS tas upp och antikroppen frigörs precis där TIMP‑1 är koncentrerat, medan exosomen själv fortsätter att främja vävnadsreparation.
Hur nanosystemet beter sig och verkar
I cellstudier visade forskarna att Mexo‑cl‑aT förblir stabil i vätska men snabbt släpper sina antikroppar när det utsätts för väteperoxidnivåer liknande de i sjuka lungor. Samtidigt minskar det kraftigt mängden peroxid som är närvarande, vilket bekräftar dess ROS‑upptagande roll. I ärrliknande cellmodeller minskade de frigjorda antikropparna TIMP‑1‑nivåerna och frigjorde enzymer som bryter ner kollagen, medan exosomkomponenten minskade celldöd, ökade celltillväxt och påskyndade sårslutning i både lung‑ och blodkärlsceller. Jämfört med varianter där länkaren inte kunde klippas bort tog den ROS‑responsiva designen bort mer kollagen och reducerade kemisk stress mer effektivt, vilket framhäver vikten av kontrollerad frisättning.
Testning i en modell med svår lungsärrbildning
Teamet testade därefter terapin i möss med avancerad lungsfibros framkallad av läkemedlet bleomycin, en modell vald för att efterlikna sent stadium av IPF. En enda dos inhalerad Mexo‑cl‑aT dröjde kvar i lungorna i flera dagar och behöll mer antikropp än en enkel blandning av dess beståndsdelar. Behandlade lungor såg friskare ut både för blotta ögat och i mikroskop: luftutrymmen återöppnades, ärrtjockleken minskade och det totala kollageninnehållet återgick nästan till normalt. Markörer för aktiverade ärrbildande celler sjönk, medan proteiner kopplade till friska luftblåse‑ och blodkärlsceller ökade. Kemiska mätningar visade att behandlingen kraftigt sänkte TIMP‑1‑nivåerna, återställde balansen hos kollagen‑nedbrytande enzymer och avlägsnade omkring tre fjärdedelar av överskotts‑ROS. Viktigt är att inflammationsmått minskade och blodprover samt organundersökningar inte avslöjade uppenbar toxicitet.
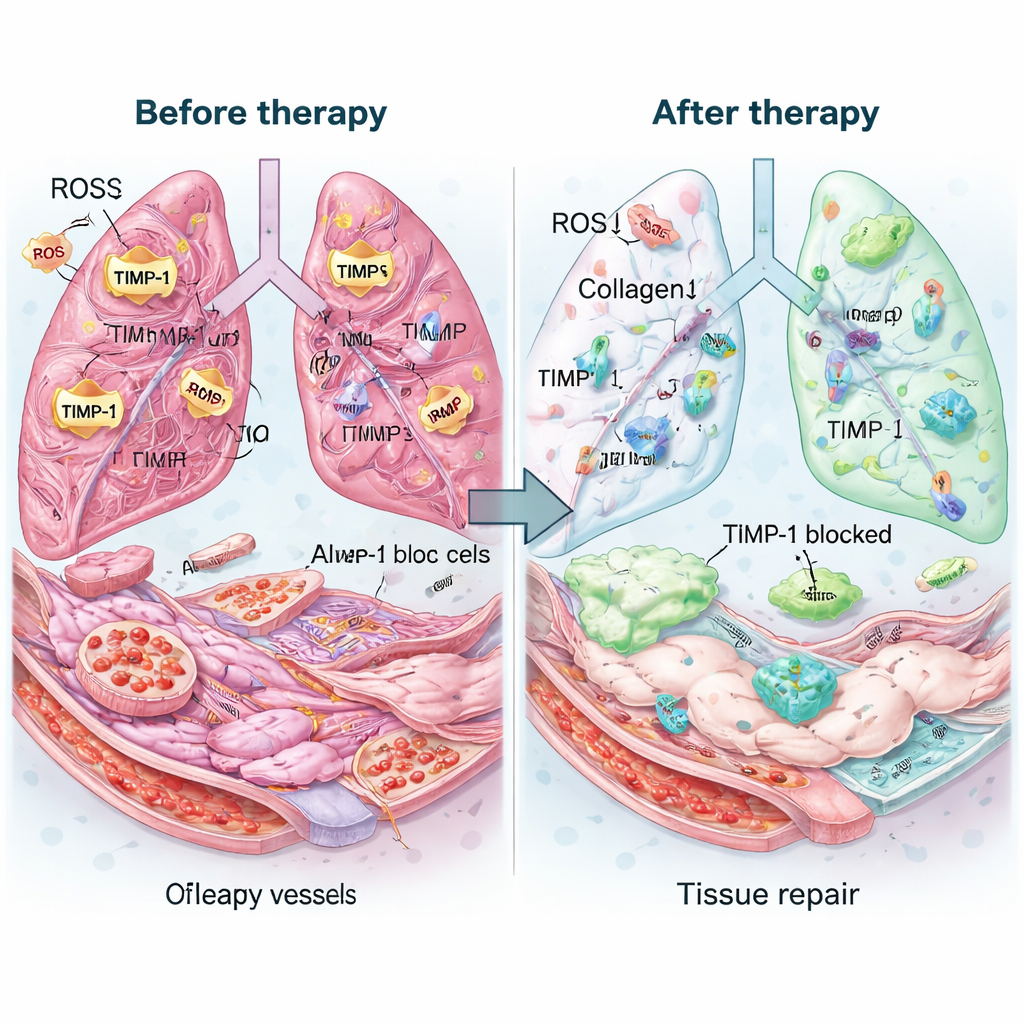
Vad detta kan innebära för patienter
För personer som lever med IPF erbjuder detta arbete ännu inte en omedelbar bot, men det introducerar en lovande strategi. Istället för att endast bromsa ytterligare skador syftar Mexo‑cl‑aT‑nanosystemet till att aktivt ångra redan uppkomna ärr, dämpa skadlig kemisk stress och stödja återuppbyggnad av skör lungvävnad — allt i en riktad, inhalerad form som koncentrerar behandlingen där den behövs mest. Medan utmaningar såsom storskalig exosomproduktion och prövningar i människor återstår, antyder studien att precisionsnanoterapier anpassade till den sjuka miljön en dag kan förändra hur envis lungsärrbildning, och kanske andra fibrotiska sjukdomar, behandlas.
Citering: Li, C., Lu, G., Chen, H. et al. A nanosystem targeting tissue inhibitor of metalloproteinase-1 for continuous spatiotemporal idiopathic pulmonary fibrosis therapy. Nat Commun 17, 1694 (2026). https://doi.org/10.1038/s41467-026-68398-0
Nyckelord: idiopatisk lungsfibros, lungsärrbildning, nanomedicin, exosomterapi, TIMP‑1