Clear Sky Science · sv
Skadade epitelcellstillstånd påverkar njurallografts överlevnad efter T‑cellsmedierad rejektion
Varför denna njurforskning är viktig för patienter
Njurtransplantationer kan rädda liv, men många går ändå i stå år efter operation även när läkare tycks ha kontroll över den immuna attacken som kallas T‑cellsmedierad rejektion. Denna studie ställer en enkel men avgörande fråga: om den immuna reaktionen ser "behandlad" ut i mikroskopet, varför slits vissa transplanterade njurar ändå ut tidigt? Genom att zooma in på enskilda celler i transplanterade njurar från möss och människor avslöjar forskarna ett dolt skikt av skada inne i njurens filtrerande tubuli som hjälper förklara vilka grafts som överlever och vilka som inte gör det.
Att se bortom klassiska tecken på avstötning
Läkare diagnostiserar vanligtvis T‑cellsmedierad rejektion genom att se vita blodkroppar invadera njuren och angripa de små tubuli som bearbetar urinen. Kraftfulla anti‑avstötningsläkemedel kan ofta driva bort dessa immunceller och få biopsin att se bättre ut. Ändå löper patienter med denna form av rejektion fortsatt hög risk för graftförlust. Tidigare storskaliga genstudier antydde att signaler om vävnadsskada inne i njurceller bättre förutsäger utfall än mått på hur många immunceller som finns närvarande. Författarna ville därför definiera dessa skadesignaler på enskild cell‑nivå och pröva hur tätt de är kopplade till långsiktig transplantationsöverlevnad.
Att dissekera rejektion en cell i taget
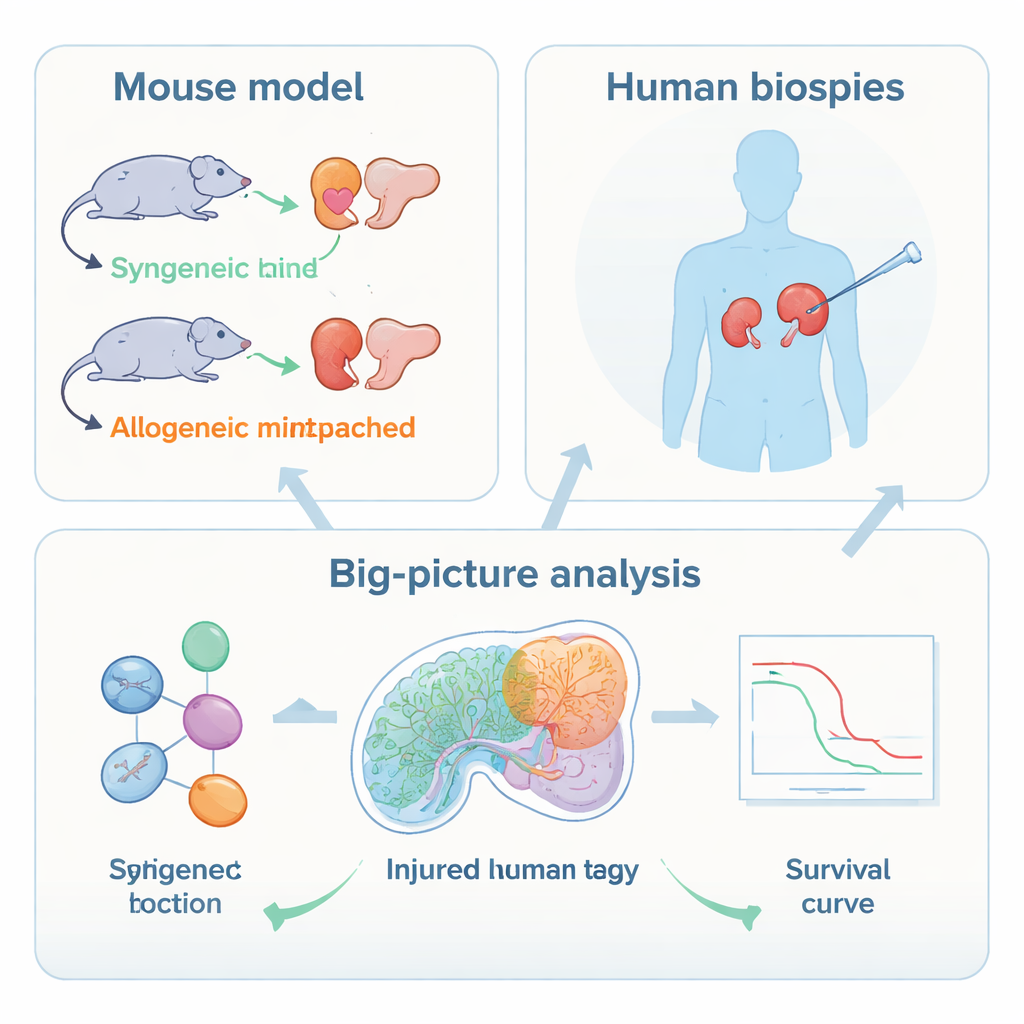
Gruppen använde först en kontrollerad musmodell, där njurar transplanterades antingen mellan genetiskt identiska möss eller mellan osamsatta stammar för att framkalla rejektion. De tillämpade sedan single‑nucleus RNA‑sekvensering, som läser aktiviteten hos tusentals gener i individuella celler, och spatial transkriptomik, som visar var dessa celler ligger i vävnadsstycket. Dessa verktyg visade att de starkaste molekylära förändringarna vid rejektion inte sker i immuncellerna utan i njurens egna epitelceller som bekläder proximala tubuli och ett segment kallat tjockt uppåtstigande ben. I dessa områden slog celler på gener för skada och stress, inflammatoriska signaler och markörer för ett mer primitivt, mindre specialiserat tillstånd, samtidigt som de slog ner transportfunktioner som behövs för hälsosam filtrering.
Dolda fickor av svårt skadade tubuliceller
Genom att gruppera celler med liknande genaktivitet upptäckte forskarna flera distinkta "skadestatusar" bland tubulicellerna i musnjurarna. Vissa speglade tidiga stressreaktioner, medan andra representerade svårt skadade, kraftigt förändrade celler som förlorat normal identitet och producerade många inflammatoriska och ärrbildande molekyler. Rumslig kartläggning visade att dessa celltillstånd inte spred sig jämnt: vissa svåra skadestatusar bildade fläckvisa fickor över njurbarken och yttre märgen och låg i komplexa grannskap med T‑celler, makrofager och fibroblaster. I kontrast var några skadade celler i djupare regioner förvånansvärt isolerade från immunceller, vilket antyder olika sätt som skada kan uppstå och bestå.
Matchning av musens skadestatusar med mänskliga transplantat
Författarna frågade sedan om liknande celltillstånd finns hos människor. De analyserade biopsier från mänskliga njurtransplantat med aktiv T‑cellsmedierad rejektion och från stabila grafts. Single‑cell‑data visade återigen skadade proximala tubuli‑ och tjockt uppåtstigande ben‑celler vars genmönster stämde väl överens med de mest svårt skadade mus‑cellstillstånden. Med hjälp av dessa humana signaturer "dekonvoluterade" teamet tusentals äldre bulk‑biopsi‑genuttrycksprofiler och fann att svårt skadade tubulicellstillstånd var vanligare vid T‑cellsmedierad och blandad rejektion än vid enbart antikroppsmedierad rejektion eller ingen rejektion. Viktigt var att de byggde kompakta genset som representerade varje skadestatus och poängsatte dem i en stor kohort med detaljerad uppföljning.
Skadade tubuliceller som förutsägare för graftens öde
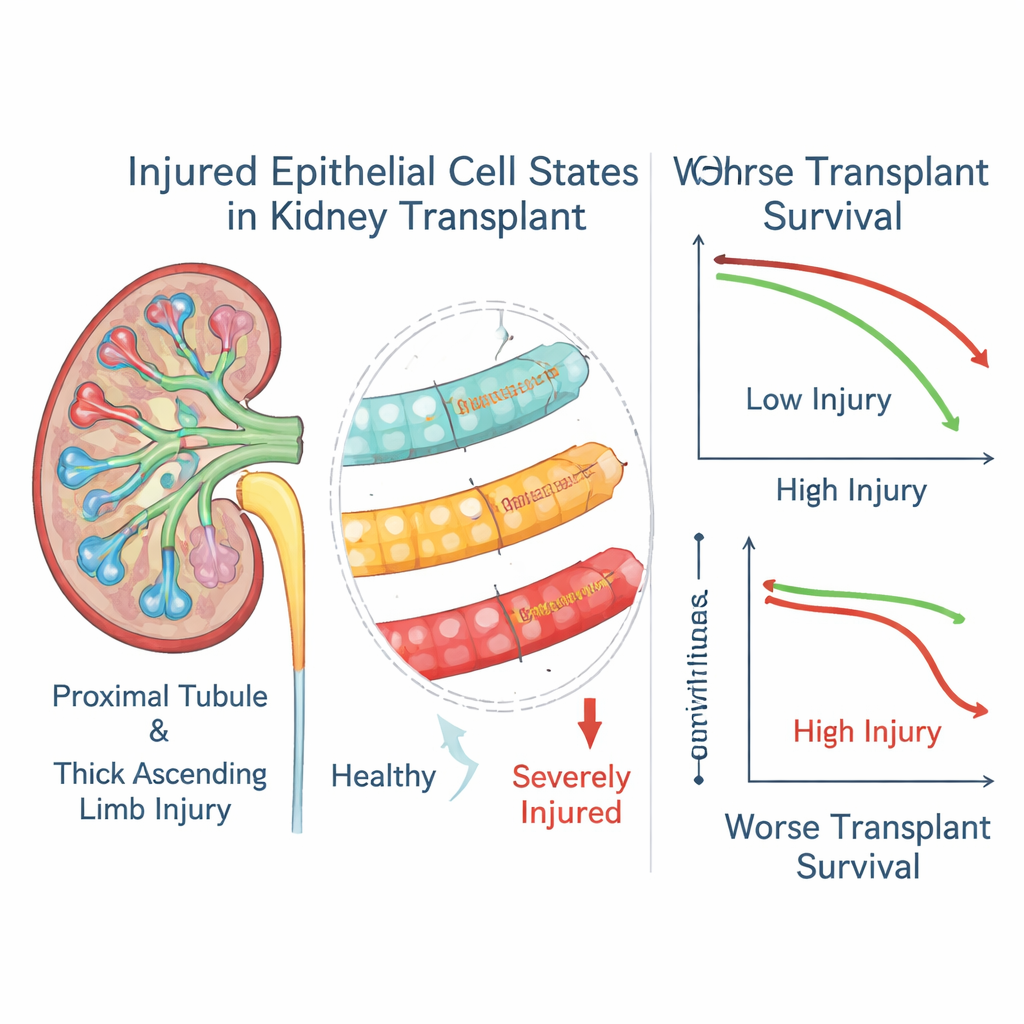
När författarna kopplade dessa genpoäng till treårsutfall hos över tusen transplantationsmottagare framträdde ett tydligt mönster. Höga nivåer av markörer för de mest svårt skadade epitelialiska tillstånden i både proximala tubuli och tjockt uppåtstigande ben var starkt förknippade med ökad risk för graftförlust, även bland patienter vars biopsier annars klassificerades som behandlad rejektion. Ett mildare tubulärt skadetillstånd visade motsatt trend och var kopplat till bättre överlevnad, vilket tyder på att det kan representera ett mer framgångsrikt reparationsprogram. I en delmängd av patienter med upprepade biopsier förblev "svårt skade"‑poängen ofta höga långt efter att rejektionsepisoden skenbart hade lösts, vilket antyder att dessa förändrade celler kan dröja kvar och fortsätta påverka sjukdomen.
Vad detta innebär för transplantationsvård
För icke‑specialister är huvudbudskapet att inte all skada i en avstött njure kommer direkt från immunceller, och att inte all skada försvinner när den immuna attacken tystnar. Denna studie visar att envetna fickor av svårt skadade tubuliceller fungerar som ett tidigt varningssystem för framtida graft‑failur. I längden skulle enkla tester baserade på dessa skadegenssignaturer—möjligen till och med med celler som lossnat i urinen—kunna hjälpa läkare identifiera högriskpatienter, skräddarsy behandlingar och övervaka om njurarna verkligen återhämtar sig. Arbetet pekar också på dessa skadade epitelceller som potentiella mål för nya terapier som syftar till att skydda transplanterade njurar utöver standard immunundertryckning.
Citering: Pfefferkorn, A.M., Jahn, L., Gauthier, P.T. et al. Injured epithelial cell states impact kidney allograft survival after T-cell-mediated rejection. Nat Commun 17, 1060 (2026). https://doi.org/10.1038/s41467-026-68397-1
Nyckelord: njurtransplantationsavstötning, tubulär cellskada, single-cell-sekvensering, transplantationsöverlevnad, epitelcellstillstånd