Clear Sky Science · sv
Modellering av vävnadsspecifik Drosophila-metabolism identifierar högsockerdiet‑inducerad metabolisk dysreglering i muskel på reaktions‑ och väg‑nivå
Varför denna bananfluga‑studie är viktig för människors hälsa
För mycket socker i våra dieter kan pressa kroppens förmåga att hantera bränsle och så småningom bidra till typ 2‑diabetes. Den här studien använder bananflugor för att i detalj kartlägga hur olika vävnader hanterar metabolism och hur en högsockerdiet stör muskelfunktionen. Eftersom flugor delar många metaboliska gener och organsystem med människor, hjälper dessa insikter att förklara vad som kan gå fel i våra egna muskler vid långvarig sockeroverbelastning.
Kartläggning av metabolism vävnad för vävnad
Våra kroppar, liksom bananflugornas, består av vävnader som har mycket olika metaboliska roller: muskel förbrukar bränsle, fett lagrar det, tarmarna bearbetar maten och så vidare. Istället för att mäta varje enzym direkt byggde forskarna storskaliga ”kartor” över metabolism—så kallade genomskaliga metaboliska modeller—för 32 olika flugvävnader. De kombinerade ett befintligt, kuraterat nätverk av kemiska reaktioner med enkelcells genuttrycksdata, som anger vilka metabola gener som är aktiva i varje vävnad. Det gjorde det möjligt att jämföra hur många reaktioner, metaboliter och gener som är aktiva i varje vävnadsspecifika nätverk och att se vilka vägar som prioriteras i muskel, fettkropp, tarm och olika nervcellstyper.
Olika energijobb för olika organ
Jämförelsen avslöjade tydliga metaboliska ”personligheter” mellan vävnader. Fettkroppen och oenocyter—flugornas motsvarigheter till mänskligt fett och lever—innehöll det rikaste utbudet av reaktioner, särskilt de som bryter ner fetter via beta‑oxidation. Muskel hade däremot inte det största nätverket, men hade den högsta andelen reaktioner som flyttar ämnen in och ut ur celler, vilket tyder på att muskel är en viktig nav för utbyte av bränslen och byggstenar med resten av kroppen. Forskarna kontrollerade också om de förutspådda vägarna matchade verkliga metabolitmönster mätta i olika kroppsregioner. Med riktad metabolomik analyserade de hundratals små molekyler från flughuvuden, thorax, tarmar och bakkroppar och undersökte om de vägar som var förhöjda i data överlappade med modellerna. I muskel och fettkropp var överensstämmelsen stark, vilket ökade förtroendet för att de vävnadsspecifika modellerna fångade verklig biologi bättre än genuttryck ensam.
Vad en högsockerdiet gör med muskels bränsleflöde
Med en validerad muskelmodell i handen simulerade teamet vad som händer när flugor matas med en långvarig högsockerdiet, en väletablerad modell för typ 2‑diabetes. De begränsade modellen med kända drag hos diabetisk muskel, såsom minskat glukosupptag och dämpad aktivitet i den centrala energicykeln i mitokondrierna. Beräkningsmässiga ”flödes”analyser—beräkningar av hur snabbt reaktioner kan gå—visade breda minskningar i reaktioner som beror på redoxparet NAD/NADH, molekyler som shuttle elektroner och är avgörande för energiproduktion. Särskilt bromsade reaktioner i den centrala sockerförbränningsvägen, glykolysen, inklusive de katalyserade av enzymet GAPDH. Modellen förutspådde också en ungefärlig minskning med en fjärdedel i muskelns kapacitet att producera NADH totalt sett, vilket antyder en påfrestad redoxbalans. Direkta mätningar i flugors thoraxmuskulatur bekräftade att förhållandet NAD/NADH faktiskt sjönk under högsockerdiet.
Följa märkta sockerarter och oxiderade proteiner
För att avgöra om dessa förutspådda flaskhalsar verkligen inträffade i levande djur matade forskarna flugor med en högsockerdiet innehållande uniformt märkta kol‑13‑glukosmolekyler och spårade sedan vart det märkta kolet hamnade. De fann att tidiga glykolytiska intermediärer uppströms om GAPDH ackumulerades, medan nedströms produkter och deras märkta andelar minskade, vilket signalerar en verklig avmattning vid och under detta steg. På liknande sätt minskade bidragen av glukoskol till den centrala energicykeln. Samtidigt visade redox‑proteomik—en metod som upptäcker oxidativa förändringar på specifika aminosyror i proteiner—ökad oxidation av många glykolytiska enzymer, inklusive flera platser på GAPDH. Över glykolysen tenderade enzymer med fler oxiderande modifieringar att visa större minskningar i förutsagt flöde, även om deras totala proteinnivåer förblev mestadels oförändrade. Detta tyder på att kemisk skada från oxidativ stress, snarare än minskad enzymmängd, är en viktig drivkraft bakom nedsatt sockerhantering i muskel.
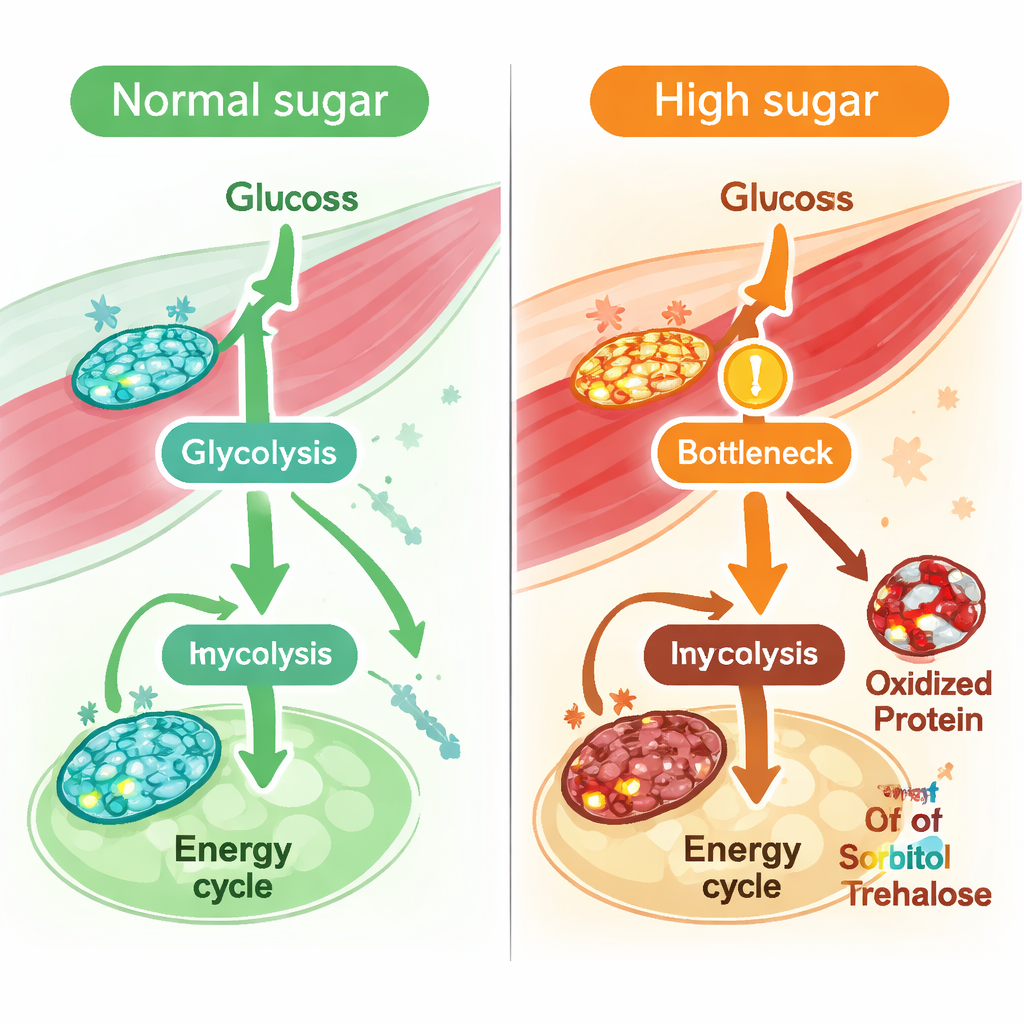
Gömda problem i hantering av fruktos och sackaros
Om man ser bortom enskilda reaktioner tog teamet medelvärden av flöden över hela vägar för att se vilka som påverkades mest av högt socker. Glykolys, energicykeln och oxidativ fosforylering visade alla nedgångar, men en av de starkaste förutspådda minskningarna gällde fruktosmetabolism. Metabolitprofilering av muskel stödde denna idé: sorbitol och trehalos/sackaros ökade, och ett nyckelenzym som omvandlar trehalos till glukos, trehalas, visade både reducerad förutspådd aktivitet och ökad oxidation vid en känslig metioninrest. Tillsammans pekar dessa fynd på en bredare störning i hur muskel hanterar kostsocker—särskilt fruktosliknande och sackaros‑härledda bränslen—vid kronisk sockeroverbelastning.
Vad detta betyder för förståelsen av diabetes
Enkelt uttryckt visar detta arbete att för mycket socker inte bara överbelastar blodomloppet; det omformar också tyst hur muskelceller dirigerar och förbränner bränsle. Genom att bygga detaljerade, vävnadsspecifika metaboliska kartor för bananflugan och korskontrollera dem med metabolomik, isotopspårning och redox‑proteomik visar forskarna att högsockerdiet driver redoxstress, oxiderar nyckel‑glykolytiska enzymer som GAPDH, saktar ner sockerbrytningen och stör fruktosrelaterade vägar. Dessa insikter, hämtade från en mycket lätthanterlig modellorganism, erbjuder ett kraftfullt ramverk för att identifiera vilka reaktioner och vägar som kan vara viktigast att skydda eller återställa i mänsklig muskel för att förebygga eller behandla typ 2‑diabetes.
Citering: Moon, S.J., Hu, Y., Dzieciatkowska, M. et al. Modeling tissue-specific Drosophila metabolism identifies high sugar diet-induced metabolic dysregulation in muscle at reaction and pathway levels. Nat Commun 17, 1692 (2026). https://doi.org/10.1038/s41467-026-68395-3
Nyckelord: Drosophila‑metabolism, vävnadsspecifika metaboliska modeller, högsockerdiet, muskulär glykolys, redoxreglering