Clear Sky Science · sv
OCT4 ökar start-effektiviteten hos sena DNA-replikationsorigin i musens embryonala stamceller
Varför detta spelar roll för våra celler
Varje gång en cell delar sig måste den kopiera hela sitt DNA korrekt och enligt schema. Om denna kopieringsprocess går fel kan det leda till utvecklingsstörningar eller sjukdom, inklusive cancer. Denna studie undersöker hur ett viktigt stamcellsprotein, OCT4, hjälper till att organisera när och var DNA-kopiering startar i musens embryonala stamceller — och ger därmed insikt i hur tidiga embryon håller sina genom stabila samtidigt som de delar sig i rasande takt.
Kartläggning av när DNA kopieras
Författarna fokuserar på ”replikationstiming” — i vilken ordning olika delar av genomet dupliceras under DNA-kopieringsfasen i cellcykeln, S-fasen. Genomet är indelat i stora område, eller timing-domäner, som kopieras tidigt, i mitten eller sent under S-fasen. Med högkapacitetssekvenseringsmetoder som märker nybildat DNA kartlade teamet replikationstiming-landskapet i musens embryonala stamceller och jämförde det med mer mogna celltyper, som fibroblaster och mesenkymala stamceller. De identifierade tusentals ”initieringszoner”, DNA‑sträckor där replikationen faktiskt börjar, och klassificerade dem som tidiga, mitt- eller sena baserat på vilken timing-domän de tillhör.
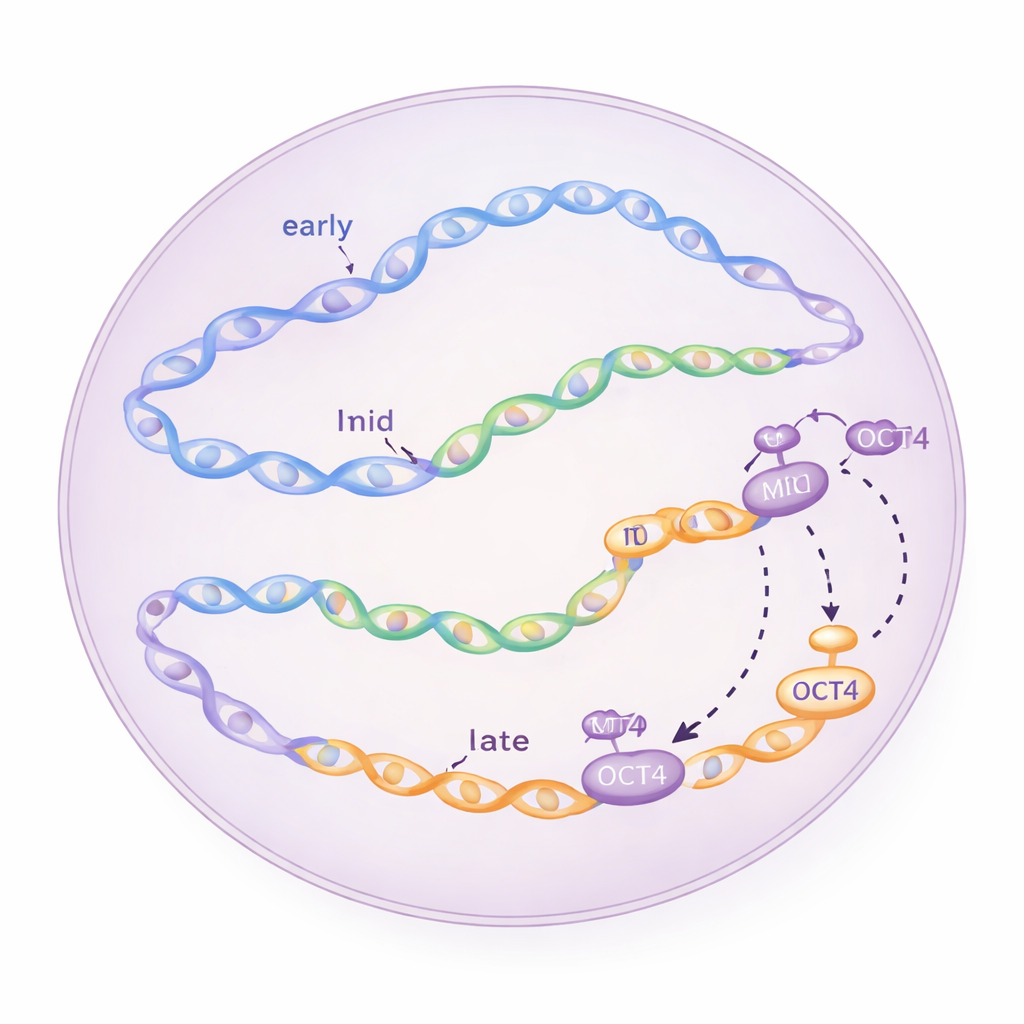
Sena startare som hoppar kön
Konventionell visdom säger att regioner planerade för sen replikation mestadels väntar tills slutet av S-fasen för att börja kopiera. Överraskande nog såg forskarna i embryonala stamceller att vissa initieringszoner i sena domäner började aktiveras mycket tidigt efter S-fasens början — inom bara en till två timmar. Genom att synkronisera celler i olika cellcykelfaser och upprepade gånger ta bilder av nysyntetiserat DNA bekräftade de att dessa ”sena” zoner verkligen tänds tidigt och att deras aktivitet beror på vanliga cellcykelregulatorer såsom kinaserna CDC7 och CDK1, samt ATR‑kontrollvägen som normalt hjälper till att förhindra överbelastning av replikationsmaskineriet.
Öppna DNA‑områden och OCT4:s roll
För att förstå vad som gör dessa ovanliga tidigt aktiva sena regioner speciella granskade teamet deras lokala miljö. De lade replikationskartor över data om RNA‑produktion och kromatinmarkörer — kemiska taggar och strukturella egenskaper som visar om DNA är i ett öppet, åtkomligt tillstånd eller hårt packat. Tidiga initieringszoner tenderade att ligga nära aktiva gener och öppet kromatin, medan sena zoner oftare fanns i repressiva, tätt packade områden. Ändå visade de särskilda sena zoner som aktiverades tidigt i embryonala stamceller tecken på öppenhet: de sammanföll med åtkomligt kromatin, enhancer‑liknande element och bindningsställen för pluripotensfaktorer som OCT4, SOX2, NANOG och KLF4. Det antyder att samma proteiner som håller stamceller flexibla i sitt öde också kan förbereda specifika sena regioner av genomet för tidigare replikation.
Att stänga av OCT4 ändrar schemat
Författarna testade sedan idén med en särskild stamcellslinje där OCT4‑nivåerna snabbt kan sänkas genom att tillsätta doxycyklin. När OCT4 depleterades under bara en del av en enda cellcykel förblev den övergripande progressionen in i S‑fas i stort sett oförändrad, men aktiveringen av många mitt‑ och sena initieringszoner försvagades eller försenades. Genom genomeomfattande analyser visade sig att i regioner där OCT4 normalt binder minskade både kromatinåtkomlighet och signaler för replikationsinitiering parallellt när OCT4 stängdes av. Statistisk modellering bekräftade att denna effekt var starkast i sent replikande zoner: ju mer en initieringszon var beroende av OCT4 för öppet kromatin, desto mer påverkades dess replikationseffektivitet i OCT4:s frånvaro.
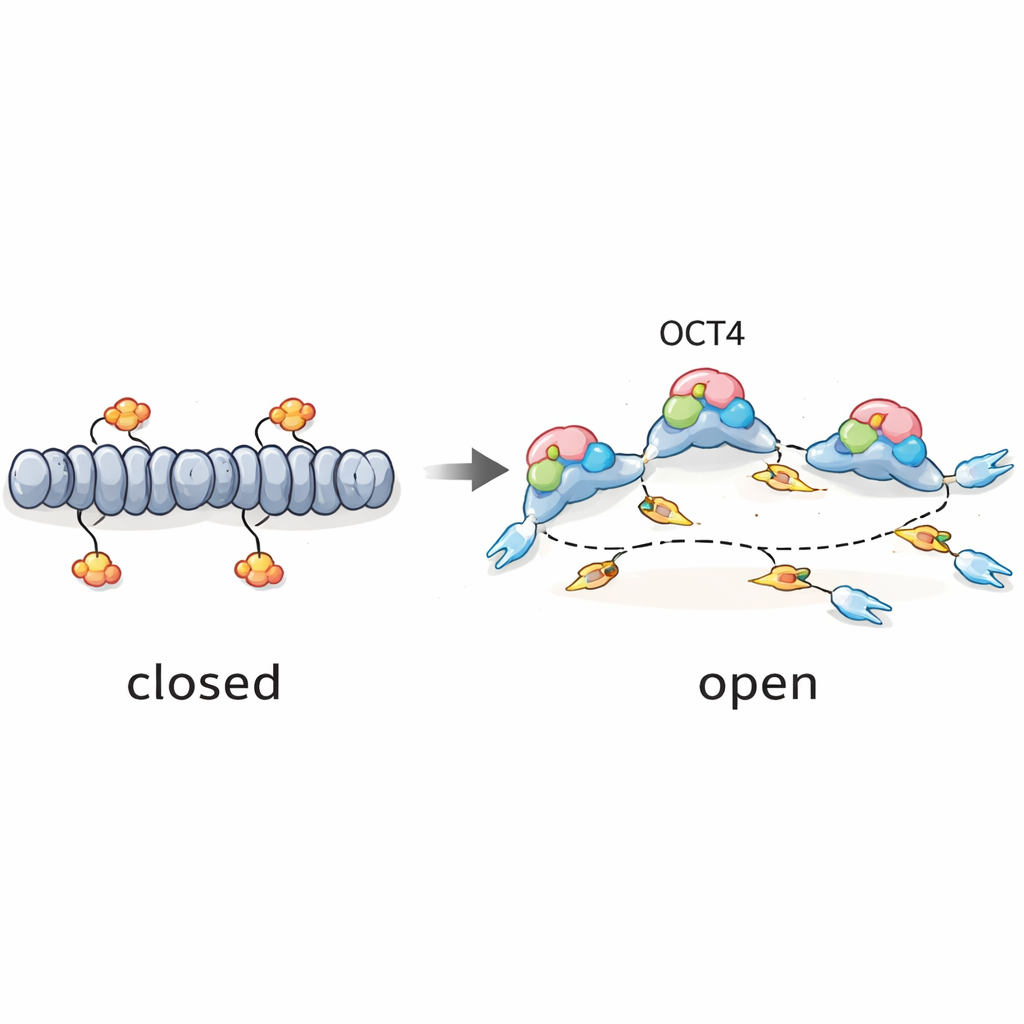
En pionjärfaktor som också tidstämplar DNA‑kopiering
Sammantaget stödjer resultaten en enkel idé: OCT4 fungerar som en ”pionjär”faktor inte bara för genaktivitet utan också för DNA‑replikation. Genom att öppna specifika sena regioner av genomet i embryonala stamceller skapar OCT4 effektiva startpunkter för DNA‑kopiering som kan aktiveras tidigare och mer pålitligt än i differentierade celler. Samtidigt finjusterar globala regulatorer som ATR, CDC7 och CDK1 hur många av dessa platser som tillåts aktiveras, för att förhindra att replikationssystemet överbelastas. För en allmän läsare är huvudbudskapet att samma proteiner som håller stamceller flexibla också hjälper till att koordinera när olika delar av deras DNA kopieras, vilket lägger till ett ytterligare skikt i vår förståelse av hur snabbt delande embryonala celler upprätthåller ordning i sina genom.
Citering: Rodriguez-Carballo, E., Dionellis, V.S., Ntallis, S.G. et al. OCT4 enhances the firing efficiency of late DNA replication origins in mouse embryonic stem cells. Nat Commun 17, 1686 (2026). https://doi.org/10.1038/s41467-026-68389-1
Nyckelord: DNA-replikationstiming, embryonala stamceller, OCT4, kromatinåtkomlighet, origin-aktivering