Clear Sky Science · sv
Precisionsutskärning av expanderade GGC-repetitioner i NOTCH2NLC med CRISPR/Cas9 för behandling av neuronal intranukleär inklusionssjukdom
Redigera DNA för att tackla en gåtfull hjärnsjukdom
Neuronal intranukleär inklusionssjukdom (NIID) är en sällsynt men förödande hjärnsjukdom som kan orsaka demens, rörelsestörningar och i värsta fall tidig död. Det finns i dagsläget ingen bot. I denna studie undersöks om ett kraftfullt verktyg för genredigering, CRISPR, kan användas för att klippa bort en liten men giftig DNA-sträcka som driver NIID, vilket ger en försmak av hur framtida behandlingar skulle kunna skriva om våra gener för att bekämpa hjärnsjukdomar. 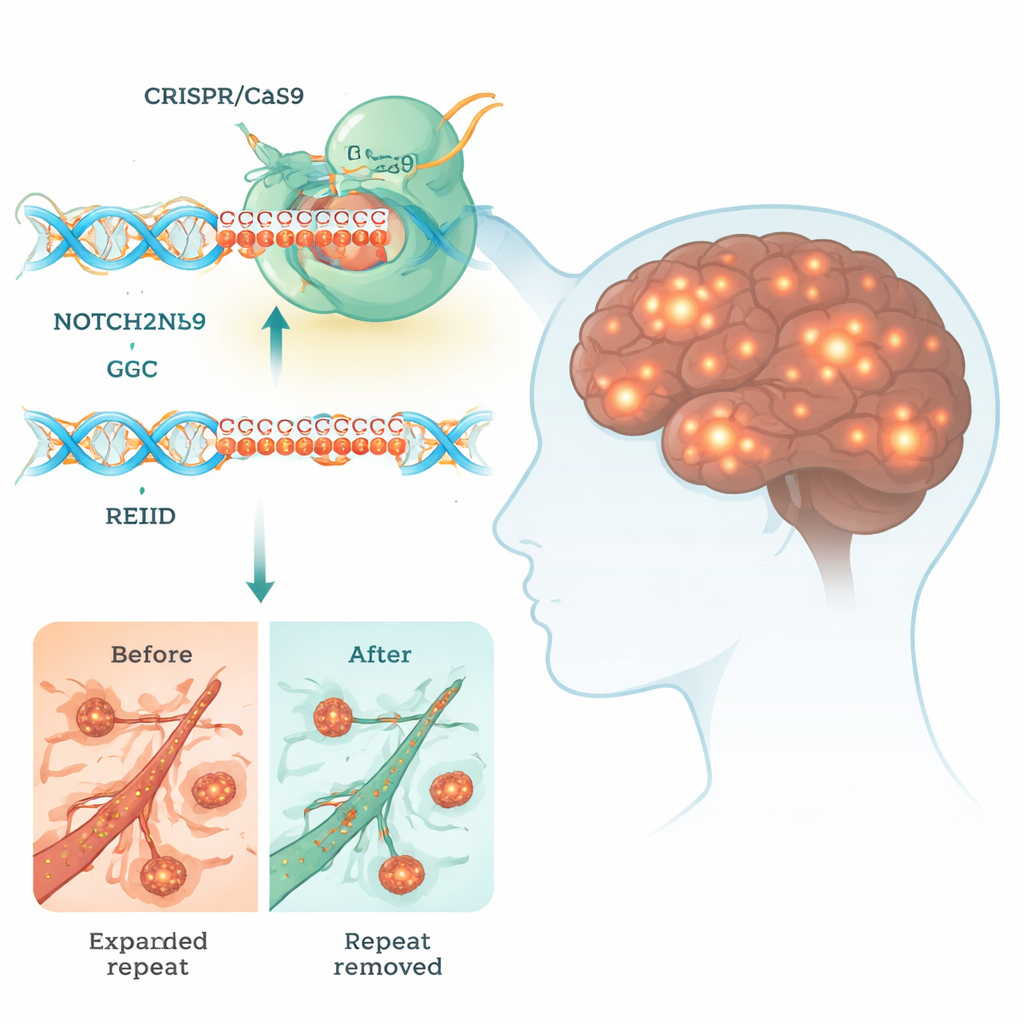
En dold genetisk bov
Många ärftliga hjärnsjukdomar orsakas av korta DNA-sekvenser som vuxit långt utöver sin normala längd. I NIID är problemet en överväxt följd av tre-bokstavs-DNA-enheter, "GGC", i en gen som heter NOTCH2NLC. Även om denna sekvens ligger i ett område som inte direkt kodar för ett klassiskt protein, kan den ändå läsas av cellens maskineri och ge upphov till abnorma polyglycin-kedjor (polyG). Dessa klibbiga kedjor klumpar ihop sig till ansamlingar inne i cellkärnan i nervceller och andra vävnader och stör viktiga processer såsom energiproduktion, RNA‑bearbetning och transporten av molekyler mellan kärna och cytoplasma.
Utmaningen med precis genkirurgi
Att utforma en genredigeringsbehandling för NIID är ovanligt svårt eftersom NOTCH2NLC har flera nästan identiska systergener som är viktiga för mänsklig hjärnutveckling. Om CRISPR klipper fel gen kan det göra mer skada än nytta. Forskarna skannade noggrant DNA:t runt GGC-repetitionen och fann små sekvensskillnader som skiljer NOTCH2NLC från dess släktingar. De designade sedan par av CRISPR-guide-RNA som leder Cas9‑"molekylära saxen" att klippa precis före och efter den expanderade repetitionen. Denna dubbelklippsstrategi låter cellens reparationssystem ta bort den giftiga segmentet samtidigt som resten av genfamiljen lämnas intakt.
Från celler i skål till patient‑härledda neuroner
Teamet testade först sin CRISPR‑design i standardiserade humana celler och i celler som konstruerats för att bära en stor NOTCH2NLC‑repetition. I dessa modeller klippte redigeraren effektivt ut repetitionen, och nivån av polyG‑ansamlingar sjönk med ungefär hälften eller mer. De gick sedan vidare till inducerade pluripotenta stamceller (iPSC) som härletts från en patient med NIID och omvandlade dessa till neurala progenitorceller, ett tidigt stadium av hjärnceller. Med CRISPR tog de antingen bort den expanderade repetitionen eller ersatte den med en normal‑lång version. Detaljerad DNA‑ och helgenomssequencing visade att redigeringen var mycket exakt, med små tecken på oönskade klipp, och de redigerade cellerna delade sig och mognade fortsatt normalt. 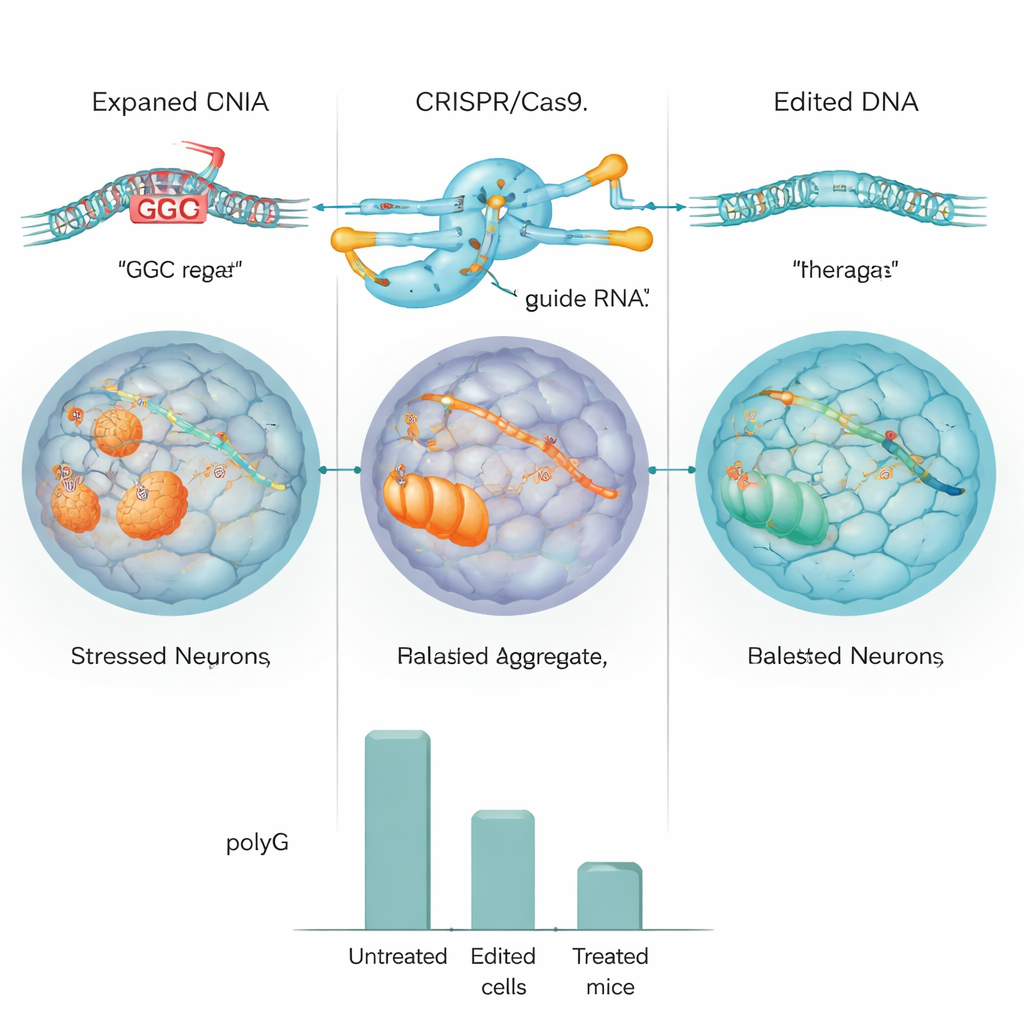
Återställning av hjärna och kropp i en musemodell
För att se om denna metod verkligen kunde förbättra sjukdomen vände forskarna sig till möss konstruerade för att bära den mänskliga NOTCH2NLC‑repetitionen och utveckla NIID‑lika drag, inklusive nukleära inklusioner, rörelsestörningar och förkortad livslängd. De paketerade CRISPR‑systemet i ett modifierat virus som kan spridas i hela hjärnan efter en enkel injektion i blodomloppet hos nyfödda möss. Hos behandlade djur togs den expanderade repetitionen bort i hjärnvävnad. Som ett resultat sjönk de toxiska polyG‑nivåerna kraftigt, markörer för nervcellshälsa förbättrades och onormal aktivering av stödjeceller i hjärnan minskade. Beteendetester visade att behandlade möss rörde sig mer, hade bättre balans och överlevde längre än sina obehandlade kullsyskon. Liknande fördelar sågs i hjärtat, som också ackumulerar polyG i denna modell.
Vad detta kan innebära för framtida behandlingar
För en lekman är huvudbudskapet att NIID verkar drivas i stor utsträckning av en specifik överväxt DNA‑repetition, och att en precis borttagning av den repetitionen kan vända många tecken på sjukdom i celler och i möss. Detta arbete översätts ännu inte till en färdig människoterapi: forskarna behöver fortfarande förfina långtidssäkerheten, förbättra leveransmetoder och testa i större, mer människoliknande djur. Men studien erbjuder ett starkt konceptbevis för att noggrant riktad genredigering säkert kan tysta en toxisk repetition samtidigt som närliggande gener sparas. Den strategin kan en dag anpassas inte bara för NIID utan också för andra hjärn‑ och muskelsjukdomar orsakade av liknande repetitions‑expansioner.
Citering: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
Nyckelord: CRISPR-genredigering, neuronal intranukleär inklusionssjukdom, sjukdomar med repeterande expansioner, NOTCH2NLC, neurodegeneration