Clear Sky Science · sv
Generativ AI baserad på sekvenser för utformning av mångsidiga tryptophansyntaser
Att lära enzymer nya färdigheter med AI
Modern samhällsfunktion bygger på molekyler—läkemedel, material och specialkemikalier—som ofta tillverkas med energikrävande och förorenande processer. Naturens katalysatorer, enzymer, kan utföra liknande uppgifter rent och effektivt, men att hitta eller konstruera rätt enzym för en ny industriell uppgift är långsamt och osäkert. Denna studie visar att generativ artificiell intelligens, samma typ av teknik som ligger bakom textskrivande chatbottar, kan användas för att designa helt nya enzymer som inte bara fungerar väl i labbet utan ibland överträffar de bästa varianterna som evolution och års ingenjörsarbete redan har frambringat.
Varför enzymer spelar roll i vardagen
Enzymer är små proteinmaskiner som snabbar upp kemiska reaktioner i levande celler. Kemister har lärt sig att återanvända dem för att tillverka läkemedel, livsmedelsingredienser och andra värdefulla produkter med mindre energiåtgång och färre giftiga reagenser än traditionell kemi. Problemet är att varje ny tillämpning vanligen kräver ett enzym med precis rätt egenskaper—kapabelt att acceptera särskilda utgångsmaterial, tåla bearbetningsförhållanden och ge höga utbyten. Konventionell “styrd evolution” förbättrar enzymer genom att skapa och testa många muterade varianter, generation efter generation. Det fungerar bra men förutsätter ett hyfsat startenzym och kan ta månader eller år av prövande och fel, vilket lämnar många användbara reaktioner outforskade.
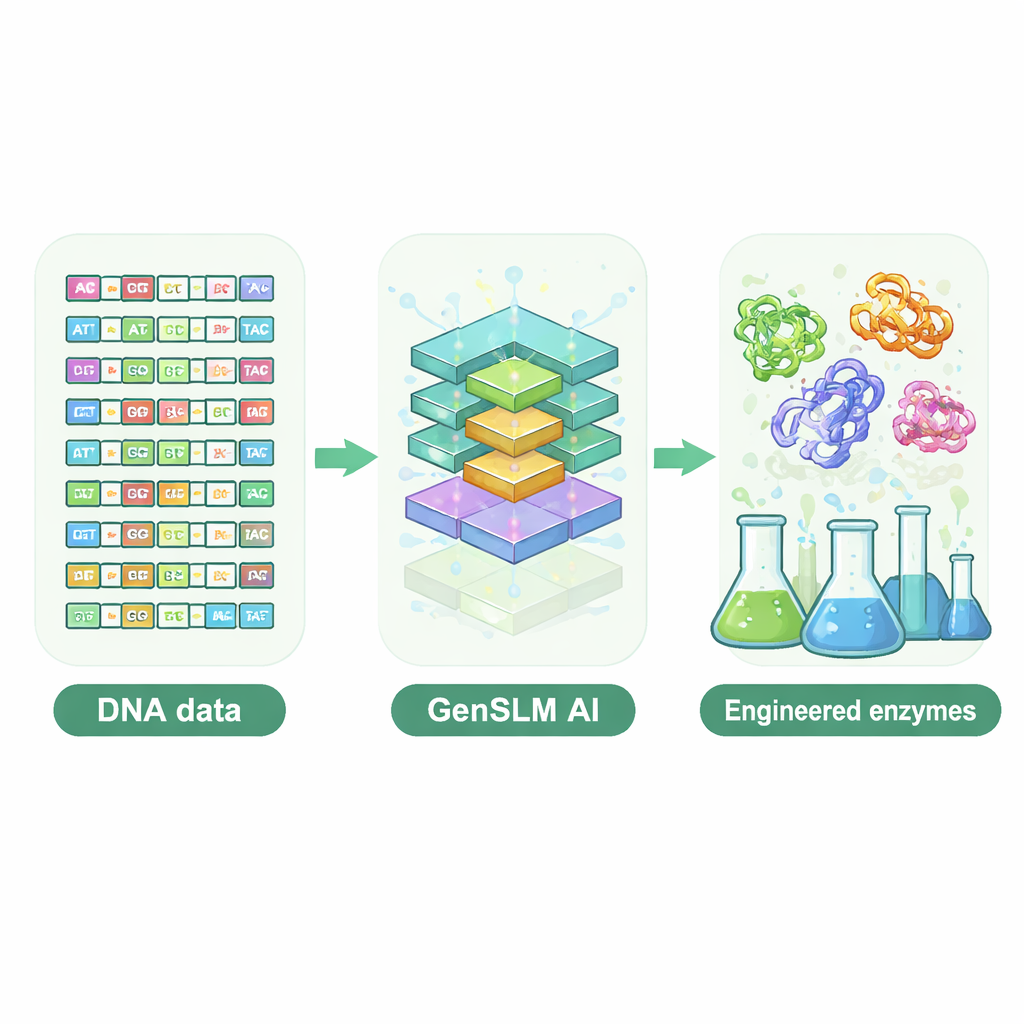
Att låta en språkmodell skriva DNA
Forskarna vände sig till en genomomfattande språkmodell kallad GenSLM, som lär sig mönster i DNA på samma sätt som en språkmodell lär sig grammatik och stil i text. Istället för att arbeta med färdiga proteinsekvenser läser och skriver GenSLM DNA i trebokstavskodon, vilket speglar hur celler översätter gener till proteiner. Teamet finjusterade först GenSLM på tiotusentals naturliga gener för en särskilt komplex enzymdel, kallad TrpB, som hjälper till att bygga aminosyran tryptofan. Därefter bad de modellen att generera tusentals helt nya trpB‑gener. Enkla beräkningsfilter gallrade bort sekvenser som var för korta eller för långa, osannolika att vika korrekt eller nästan identiska med kända naturliga enzymer, vilket lämnade 105 olika kandidater för experimentell testning i bakterier.
Från datordesigner till fungerande katalysatorer
När dessa 105 AI‑designade TrpB‑enzymer producerades i E. coli veckades många bra och producerades i höga mängder. Dussintals kunde utföra sitt huvudsakliga arbete: omvandla indol och den naturliga partneraminosyran serin till tryptofan. Några fungerade robust även vid förhöjda temperaturer, trots att ingen särskild design för värmetålighet hade gjorts. I jämförande tester matchade eller slog en del av GenSLM‑TrpB:erna ett referensenzym som mödosamt hade utvecklats i labbet under år för att fungera självständigt vid 75 °C. En framstående design, betecknad 230, producerade mer tryptofan än denna industriellt använda referens både vid rumstemperatur och vid hög temperatur, vilket visar att en modell tränad enbart på sekvensdata kan hoppa direkt till topprestanda.
Ny flexibilitet bortom vad naturen byggt
Teamet utmanade sedan enzymerna med en panel av icke‑naturliga substrat—indolderivat, en annan alkohol‑liknande partner och en fluorinerad förening som används i läkemedelstillverkning. Naturliga versioner av TrpB är vanligtvis kräsna: de föredrar kraftigt sina nativa substrat och visar liten aktivitet på sådana alternativ. Anmärkningsvärt var att de AI‑genererade enzymerna ofta var mer äventyrliga. För varje icke‑naturligt substrat som testades visade åtminstone en GenSLM‑design mätbar aktivitet, och många presterade bättre än naturliga enzymer. Återigen utmärkte sig variant 230 och omvandlade alla sju alternativa substrat med utbyten från måttliga till nästan fullständiga—en bredd av “promiskuitet” som tidigare inte setts i denna enzymfamilj. När forskarna jämförde 230 med dess närmaste naturliga släkting—skiljande sig vid endast 78 av 400 aminosyrapositioner—visade sig den naturliga enzymet sakna denna mångsidighet trots att dess övergripande struktur och viktiga aktiva‑ställe‑rester var nästan identiska.
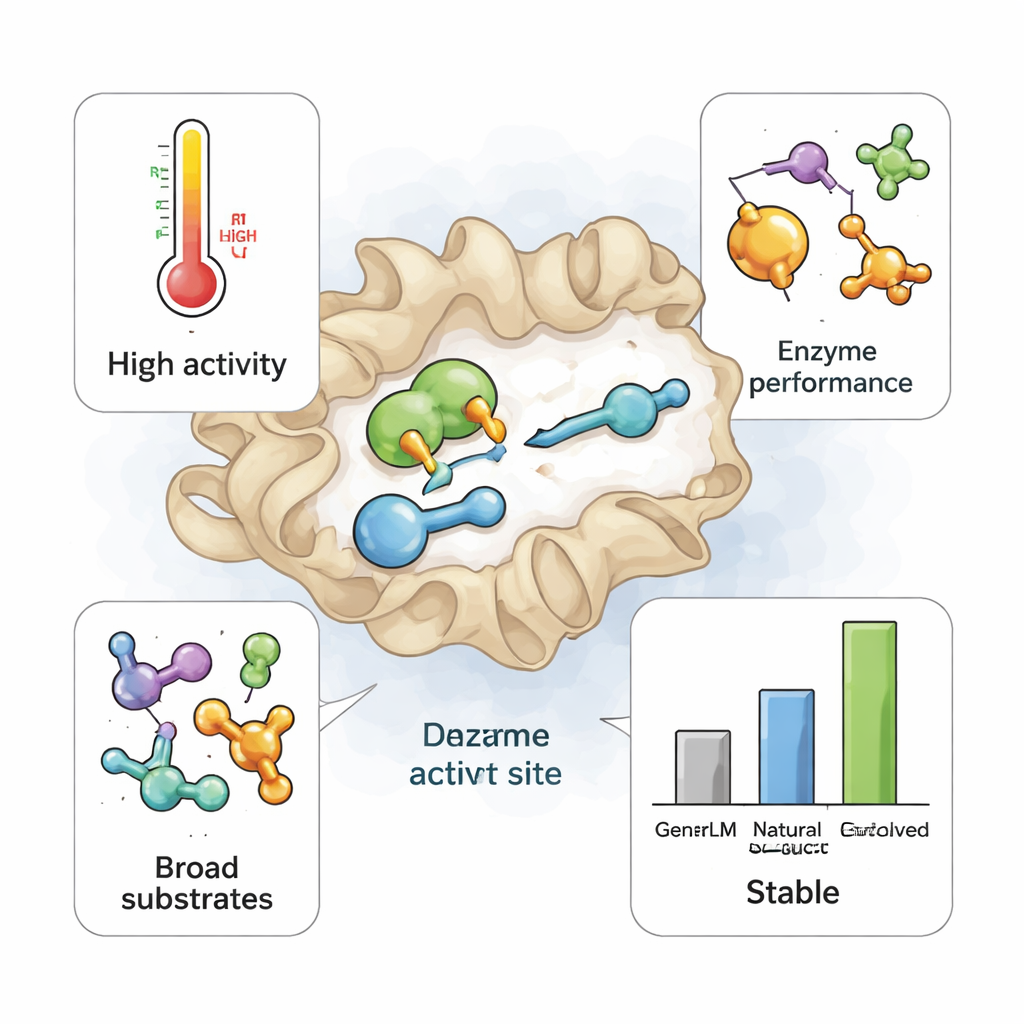
Vad detta betyder för framtidens grönare kemi
För en icke‑specialist är huvudbudskapet att en AI‑modell tränad enbart på befintliga DNA‑sekvenser kan föreställa sig realistiska nya enzymer som naturen aldrig provat, varav några är bättre verktyg för kemi än de vi idag använder. Dessa AI‑designade TrpB‑varianter behåller den grundläggande formen och funktionen hos sina naturliga kusiner men får en ovanlig förmåga att hantera många olika utgångsmaterial. Denna flexibilitet kan dramatiskt minska mängden labbarbete som behövs för att upptäcka enzymbaserade vägar till nya läkemedel och andra produkter. När design, DNA‑syntes och tester blir snabbare och billigare kan liknande generativa modeller göra enzymupptäckt från en långsam skattjakt till en snabb, rutinmässig designuppgift och därigenom hjälpa till att flytta mer industriell kemi mot renare, enzymdrivna processer.
Citering: Lambert, T., Tavakoli, A., Dharuman, G. et al. Sequence-based generative AI design of versatile tryptophan synthases. Nat Commun 17, 1680 (2026). https://doi.org/10.1038/s41467-026-68384-6
Nyckelord: enzymteknik, generativ AI, proteindesign, tryptophansyntas, biokatalys