Clear Sky Science · sv
Tmem110 reglerar TRPML1:s konformation för att bevara endolysosomal homeostas och förhindra läckage av mitokondriellt DNA och patologisk behandling av själv‑DNA
Varför utsipprande DNA efter skada spelar roll
När vi drabbas av svåra trauman, till exempel ett kraftigt slag mot huvudet, stannar inte skadan vid själva skadeplatsen. Många patienter utvecklar en farlig helkroppsreaktion där lungor, lever, njurar och andra organ börjar fallera. Denna studie visar hur mikroskopiska strukturer i cellerna — lysosomer, mitokondrier och immunsensorer — kommunicerar för att avgöra om kroppen tyst rensar upp skräpet eller snärjer in sig i en självdriven immunattack. Att förstå detta dolda rengöringssystem kan öppna nya vägar för att förebygga organsvikt efter trauma och för att behandla autoimmuna och inflammatoriska sjukdomar.
Från huvudskada till helkroppskris
Traumatisk hjärnskada (TBI) kan utlösa en kraftig inflammatorisk storm kallad multipelt organsviktssyndrom (MODS), men hur skadan i hjärnan sprider sig till avlägsna organ har varit oklart. Författarna fokuserar på monocyter och makrofager, immunceller som patrullerar blod och vävnader och fungerar som professionella soprensare. Efter TBI dör celler på ett okontrollerat sätt och släpper ut hela mitokondrier — små energifabriker som bär sitt eget DNA — ut i cirkulationen. Detta mitokondriella DNA (mtDNA) liknar till immune systemet bakterie‑DNA och kan aktivera kraftfulla antivirala försvar om det inte avlägsnas snabbt. Vanligtvis internaliserar cellerna dessa vilsna mitokondrier i sura rum kallade lysosomer, där enzymer bryter ner DNA innan det läcker ut i cellvätskan. 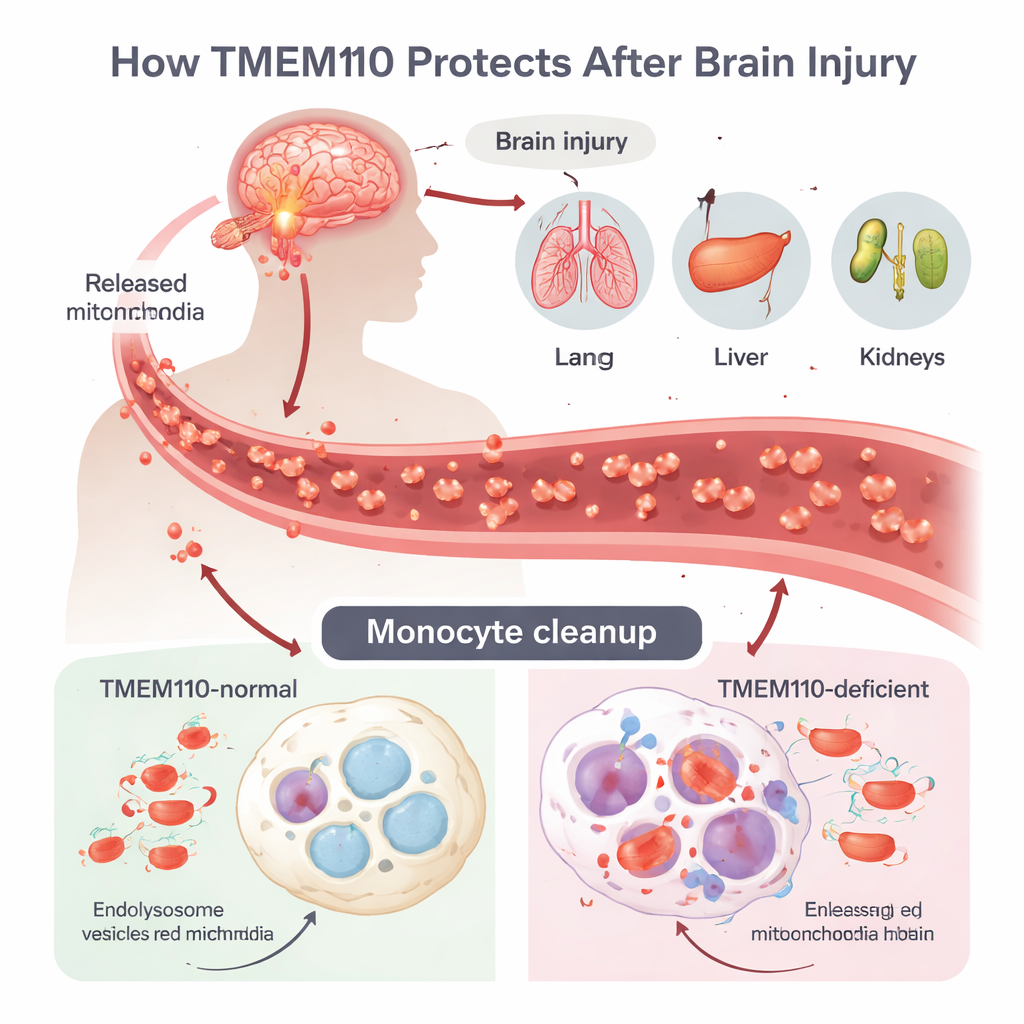
En grindvakt som håller lysosomer stabila
Teamet identifierade TMEM110, ett protein som korsar membranet i det endoplasmatiska retiklet (ett stort intracellulärt membrannätverk), som en avgörande grindvakt i denna process. Genom att använda genetiskt modifierade möss som saknade TMEM110 endast i monocyter och makrofager skapade de en kontrollerad modell för hjärnskada. Jämfört med normala möss utvecklade TMEM110‑defekta djur mycket högre nivåer av typ I interferoner — potenta antivirala signalmolekyler — i blod och cerebrospinalvätska. Deras lungor, lever, njurar och lymfkörtlar visade allvarligare skador, och deras långsiktiga överlevnad efter TBI var markant sämre. När forskarna blockerade receptorn för typ I interferoner, eller ersatte det mutanta benmärgen med normala celler, minskade organ‑skador och dödlighet, vilket visar att överdriven interferonsignalering från perifera monocyter är en central drivkraft för MODS i detta sammanhang.
Hur felaktig jonhantering tillåter DNA att läcka
När forskarna gick in i dessa immunceller fann de att TMEM110‑defekta lysosomer var kemiskt obalanserade: de var mindre sura och överladdade med kalcium. Under dessa förhållanden förlorade enzymet DNase II — som normalt klyver DNA i lysosomer — sin aktivitet, lysosomala membran blev sköra och mtDNA läckte ut i omgivande cytosol. Laboratorieexperiment med humana monocyter som fagocyterade märkt donormitokondrier bekräftade att utan TMEM110 läckte mer mtDNA ut i cellvätskan och utlöste en våg av interferon‑stimulerade gener. Studien visar att TMEM110 verkar genom att kontrollera ett annat protein, den lysosomala jonkanalen TRPML1. När TMEM110 finns närvarande kontaktar det fysiskt TRPML1 och förflyttar det till en "öppen" konformation som skapar små kalcium‑frisättningshotspots på lysosomytan. Dessa kontrollerade kalciumutflöden hjälper till att bibehålla rätt surhetsgrad, stöder membranreparation och håller mtDNA fångat och nedbrutet inuti. 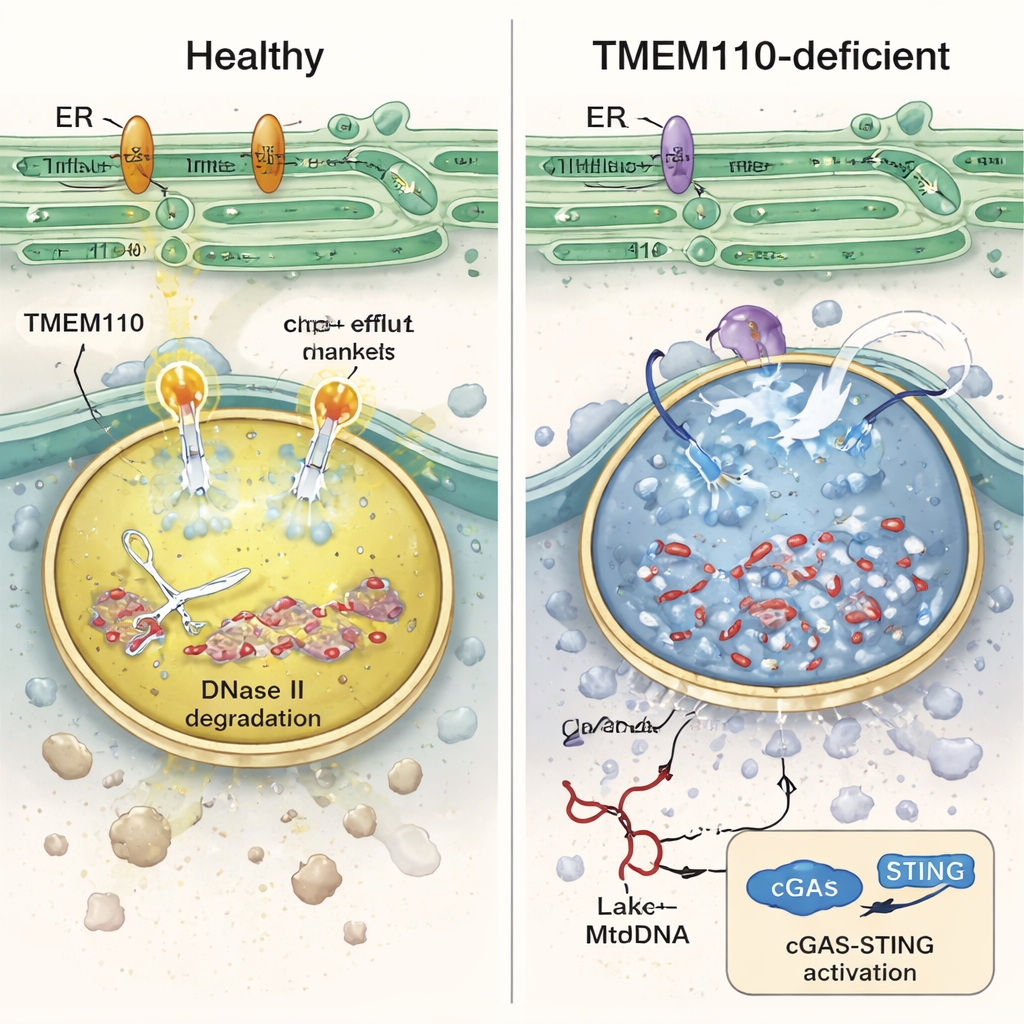
En återkopplingsslinga med cellens DNA‑larm
När mtDNA väl spills ut i cytosolen känns det igen av cGAS–STING‑vägen, cellens huvudsakliga larmsystem för främmande DNA. Intressant nog binder TMEM110 också STING i viloläge och håller det inkapslat i det endoplasmatiska retiklet, vilket förhindrar onödiga larm. När cytosoliskt DNA ackumuleras aktiveras STING och släpper sitt grepp om TMEM110. Det blottar i sin tur en annan region av TMEM110 som engagerar TRPML1 och ökar lysosomalt kalciumflöde, vilket skapar en återkopplingsslinga: igenkänning av själv‑DNA aktiverar en mekanism som förbättrar DNA‑rensning. Sjukdomsassocierade mutationer i STING som hittats i mänskliga autoinflammatoriska syndrom stör denna överlämning, fångar TMEM110 i ett hämmande tillstånd och bidrar till kronisk interferonaktivering. I möss som bar en sådan STING‑mutation ledde TBI till värre organskada och högre dödlighet, men leverans av en liten TMEM110‑fragment till lysosomer med en mRNA–lipid‑nanopartikelterapi återställde delvis kontrollen av mtDNA och förbättrade överlevnad.
Ledtrådar från patienter och vägar till nya behandlingar
Författarna vände sig sedan till en klinisk kohort om 143 personer med trauma‑relaterad hjärnskada och MODS. Patienter vars monocyter hade högre TMEM110‑nivåer tidigt efter skadan hade större sannolikhet att återfå organfunktion och överleva. De med lägre TMEM110 uppvisade mer cirkulerande mtDNA och avcellulerade mitokondrier, starkare interferonsvar, högre poäng för organsvikt och bredare autoantikroppsprofiler, inklusive antikroppar mot DNA och nukleära proteiner. Dessa mönster speglade fynden i möss och stöder idén att TMEM110‑driven kontroll av lysosomal stabilitet och mtDNA‑borttagning är en gemensam mekanism vid mänsklig sjukdom.
Vad detta betyder för patienter med svåra trauman
I vardagstermer tyder denna forskning på att efter en allvarlig skada står vårt immunsystem inför ett känsligt val: att tyst smälta flödet av själv‑DNA som släpps ut från döende celler, eller tolka det som en viral invasion och sätta in ett totalangrepp som kan skada våra egna organ. TMEM110, genom att finjustera en lysosomal jonkanal och samordna med DNA‑sensorn STING, hjälper cellerna att välja den säkrare vägen. När detta system fallerar — för att TMEM110 saknas, STING är muterat eller lysosomer är överbelastade — läcker mtDNA ut, larmet fortsätter att ljuda och multiorganskada följer. Att rikta in sig på denna TMEM110–TRPML1–STING‑axel, till exempel med lysosom‑inriktade mRNA‑terapier, skulle kunna erbjuda ett nytt sätt att förebygga eller behandla organsvikt och autoimmunliknande komplikationer efter svåra trauman.
Citering: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
Nyckelord: traumatisk hjärnskada, mitokondriellt DNA, lysosomer, typ I interferon, cGAS‑STING‑vägen