Clear Sky Science · sv
Cryo-EM-struktur av det mänskliga COP1–DET1-ubiquitinligas-komplexet
Hur celler bestämmer vilka proteiner som ska förstöras
Inuti varje cell måste tusentals proteiner ständigt byggas, omformas eller brytas ner vid rätt tidpunkt. Denna artikel undersöker en av cellens centrala ”kvalitetskontroll”-maskiner, en molekylär malningsapparat som avgör när kraftfulla genregulatorer kopplade till cancer och utveckling ska avlägsnas. Genom att avslöja dess tredimensionella struktur i nästan atomär detalj visar författarna hur maskinen kan växla mellan ett inaktivt, staplat tillstånd och en aktiv, substratbearbetande form — insikter som så småningom kan hjälpa till att designa läkemedel som antingen förstärker eller slår av den.
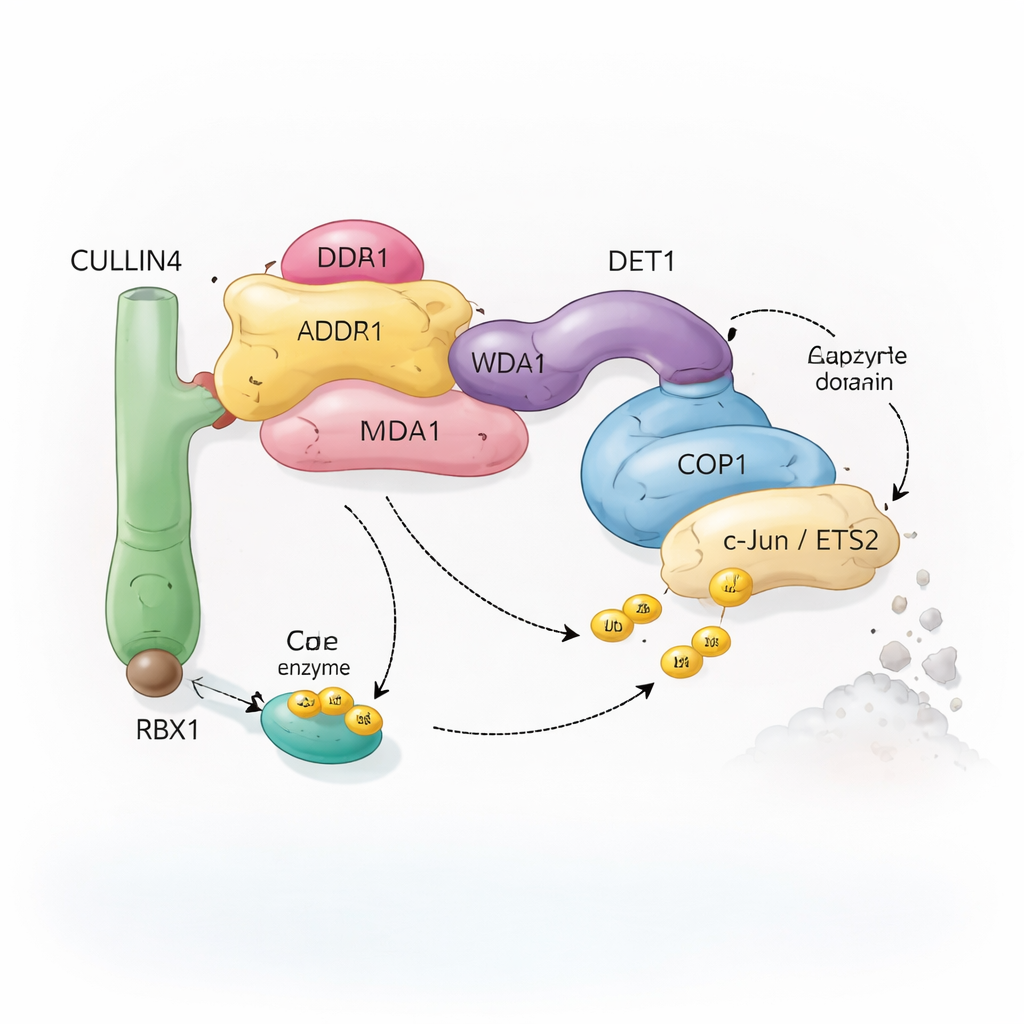
En molekylär återvinningsgrupp med många delar
Celler förlitar sig på ett system som kallas ubiquitinering för att märka proteiner för återvinning. Små molekyler av ubiquitin fungerar som avtagbara flaggor som talar om för cellen om ett protein ska modifieras, flyttas eller förstöras. Särskilda enzymkomplex, kända som ubiquitinligaser, fäster dessa flaggor på utvalda mål. Det komplex som studerats här kretsar kring COP1, ett protein som finns från växter till människor och som hjälper till att märka viktiga transkriptionsfaktorer — proteiner som styr vilka gener som slås på eller av. COP1 arbetar inte ensam: det kan ansluta till en större sammansättning byggd kring ett scaffold-protein som heter CULLIN4, plus flera adapterproteiner kallade DDB1, DDA1 och DET1. Tillsammans bildar dessa komponenter en flexibel ”återvinningsgrupp” som känner igen specifika transkriptionsfaktorer som c‑Jun och ETS2, många av dem involverade i celltillväxt och cancer.
Att fånga komplexet i 3D
För att förstå hur denna grupp fungerar använde forskarna single-particle kryo-elektronmikroskopi, en teknik som avbildar blixtfrusna proteiner och rekonstruerar deras former i hög upplösning. De återskapade det mänskliga COP1–DET1-systemet i odlade celler, renade komplexen och visualiserade flera distinkta strukturella tillstånd. Först löste de strukturen av DDB1–DDA1–DET1-modulen, som fungerar som en central navpunkt. DET1 antar en ovanlig, delvis flexibel form i stället för en styv skiva, med en utstickande ”klo” som kan gripa partnerenzym. Därefter, genom att tillsätta COP1 och en klass hjälparenzym kända som E2:or, fångade de större assembléer som visar hur alla delarna passar ihop och avslöjade både kompakta staplar och mer öppna dimeriska (två-COP1) arrangemang.
En inaktiv stapel och en aktiv dimer
En av de mest slående fynden är en staplad, filamentliknande struktur som består av upprepade lager av komplexet. I varje lager flätas åtta COP1-molekyler ihop genom sina coiled-coil-segment och bildar en diamantformad ring. Deras substratigenkännande regioner, kallade WD40-domäner, vetter alla åt samma håll och är delvis skärmade av intilliggande lager. Denna täta packning representerar sannolikt ett ”av”-tillstånd där åtkomst för målanproteiner är begränsad. Däremot, när teamet undersökte komplex som co‑uttrycktes med COP1-substrat som c‑Jun eller ETS2 såg de en annan, dimerisk form: två COP1-molekyler ordnade sida vid sida, med sina WD40-domäner utåt och tillgängliga för att binda de korta ”VP”-motiven som finns i många transkriptionsfaktorer. Biokemiska tester bekräftade att endast detta dimeriska tillstånd effektivt stöder uppbyggnaden av långa ubiquitinkedjor på c‑Jun.
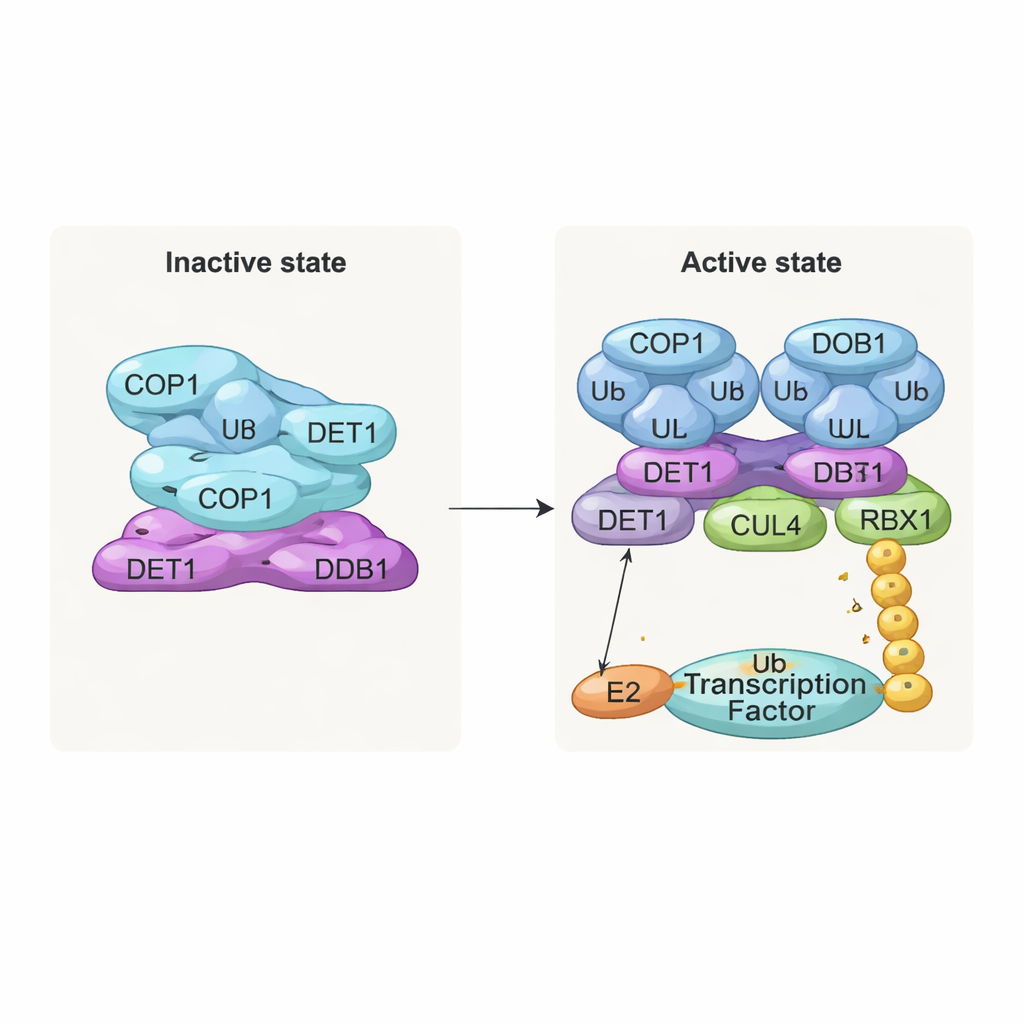
DET1 som flexibel bro och trafikdirigent
DET1 framträder som den centrala organisatören som länkar samman alla delar av maskinen. Dess N-terminala region fäster in i DDB1 och förankrar komplexet vid CULLIN4-scaffolden, medan dess klokliknande region omsluter en familj av E2-enzym som kallas Ube2e. Detaljerade mutagenesexperiment visar att det är DET1, inte COP1, som direkt griper dessa E2:or och placerar dem nära COP1:s katalytiska RING-region. I detta arrangemang tycks Ube2e hjälpa till att fästa de allra första ubiquitinflaggorna på substratet. Ett andra E2-enzym, Ube2d3, rekryteras därefter via CULLIN4–RBX1-armen för att förlänga dessa flaggor till längre kedjor som signalerar fullständig degradering. Med andra ord fungerar DET1 som en flexibel bro som presenterar en E2 för COP1, medan det större scaffoldet tar in en andra E2 för att slutföra jobbet.
Varför detta är viktigt för hälsa och sjukdom
Genom att kartlägga dessa strukturella tillstånd och deras aktiviteter förklarar studien hur samma uppsättning proteiner kan växla mellan en inaktiv, staplad form och en aktiv dimer som riktar transkriptionsfaktorer för nedbrytning. Denna växling är särskilt viktig för faktorer som c‑Jun, som driver celldelning och är starkt kopplade till cancer när de är felreglerade. Att förstå hur COP1 och DET1 samarbetar — hur DET1:s klo väljer specifika E2-enzym, hur COP1:s WD40-yta känner igen VP-innehållande substrat, och hur den aktiva dimeren bildas — ger en ritning för framtida arbete. På längre sikt kan läkemedel som stabiliserar den inaktiva stapeln eller gynnar den aktiva dimeren ge forskare nya verktyg för att ställa om genstyrningsvägar i cancer och andra sjukdomar där proteinnedbrytning går fel.
Citering: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
Nyckelord: ubiquitinligas, COP1, proteinnedbrytning, cryo-EM-struktur, c-Jun