Clear Sky Science · sv
K48-ubiquitin-beroende proteaser skär upp proteiner efter ER
Hur celler bestämmer vilka proteiner som ska förstöras
Våra celler avlägsnar ständigt utslitna eller skadade proteiner, särskilt de som sitter inbäddade i membran och fungerar som portar och sensorer. Denna artikel visar att celler använder en liten märkning kallad ubiquitin inte bara som en generell "skräp"-etikett, utan som en kod som talar om för membranproteiner exakt hur de kommer att brytas ned. Att förstå denna kod hjälper till att förklara hur celler behåller sin hälsa och kan vägleda framtida terapier som medvetet förstör sjukdomsframkallande proteiner.
En cellulär streckkod för proteinborttagning
Celler dekorerar oönskade proteiner med kedjor av ett litet protein som kallas ubiquitin. Dessa kedjor kan länkas samman på olika sätt, ungefär som pärlor trädas genom olika hål, och varje mönster kan signalera ett annat utfall. Författarna fokuserade på membranproteiner som redan lämnat det endoplasmatiska retiklet (ER) och färdas genom kompartment som Golgi och endosomer. De frågade om två vanliga kedjetyper, kallade K48-länkade och K63-länkade ubiquitin, verkligen är utbytbara etiketter eller om de styr lasten in i olika förstörelserutter.
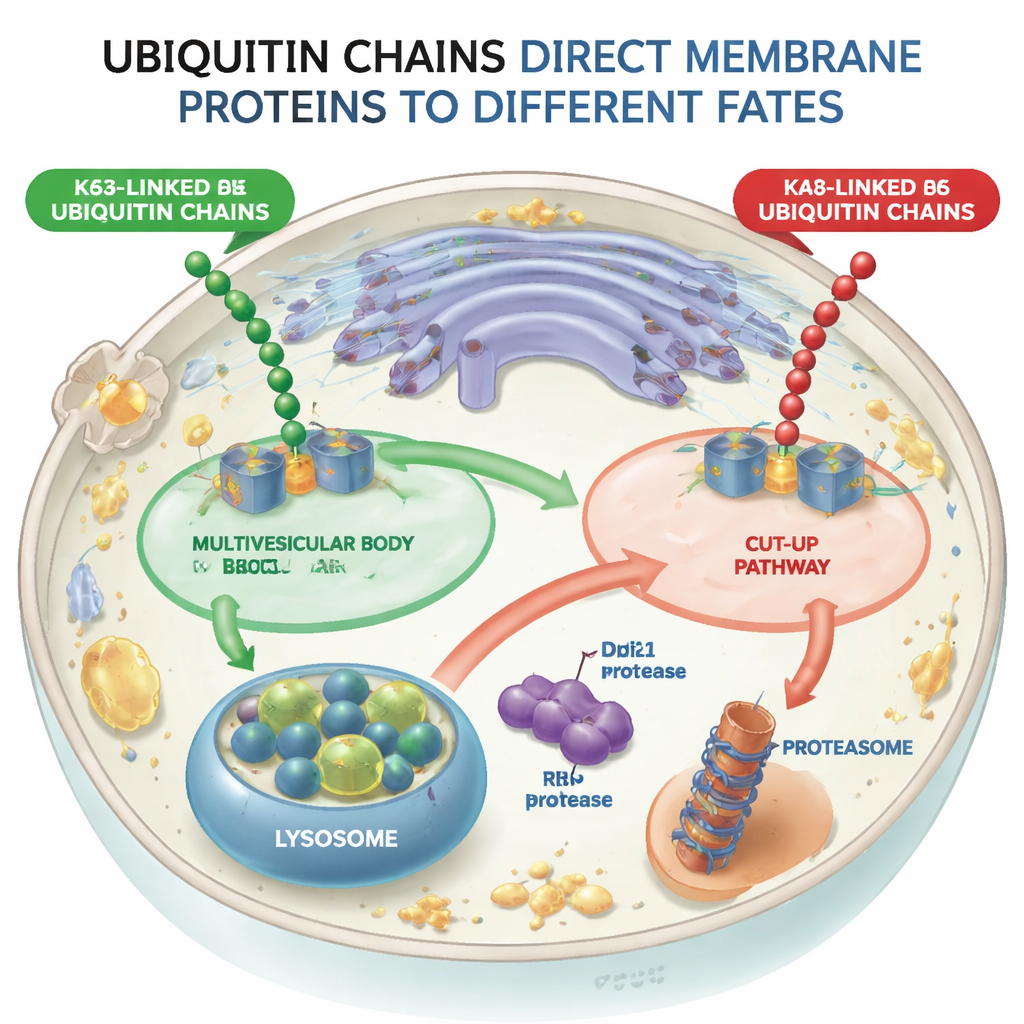
Två avvikande vägar för märkta proteiner
Genom att använda jästceller som modell konstruerade forskarna molekylära maskiner (ubiquitin-ligaset) som kunde fästa antingen K48-länkade eller K63-länkade kedjor på samma testmembranprotein, en sorteringsreceptor kallad Vps10. När Vps10 fick K63-länkade kedjor skickades det in i interna vesikler i endosomer—strukturer kända som multivesikulära kroppar—som så småningom förenas med lysosomer, cellens matsmältningskompartment. Däremot följde inte Vps10 med K48-länkade kedjor denna multivesikulära väg. Istället bröts det isär på ett helt annat sätt, vilket visar att cellen skiljer mellan dessa två kedjetyper och att den multivesikulära vägen effektivt avvisar K48-märkt last.
En "skär-upp"-väg som skivar proteiner i två
Teamet upptäckte att K48-länkade kedjor utlöser en protein-skärapathway som de kallar CUT-UP, en förkortning av Cleavage of Ubiquitinated Targets by Ubiquitin-dependent Proteases. Istället för att dra ut hela proteinet ur membranet på en gång, hugger CUT-UP det i bitar som sedan avslutas av redan existerande cellulära avfallshanteringssystem. Ett nyckelenzym, Ddi1, flyter i cytosolen och klipper av den del av membranproteinet som vetter mot cytoplasman. Den fragmentet bryts sedan ner av proteasomen, cellens huvudsakliga proteinförstärkare. Samtidigt sitter ett annat enzym, Rbd2, inne i själva membranet och skär den del av proteinet som vetter mot kompartmentets inre och frigör det i det utrymme som så småningom förbinder till lysosomen. Att blockera Ddi1, Rbd2, proteasomen och lysosomala enzymer tillsammans krävdes för att fullt ut skydda K48-märkt Vps10 från nedbrytning, vilket bekräftar att alla dessa komponenter samarbetar i CUT-UP-vägen.
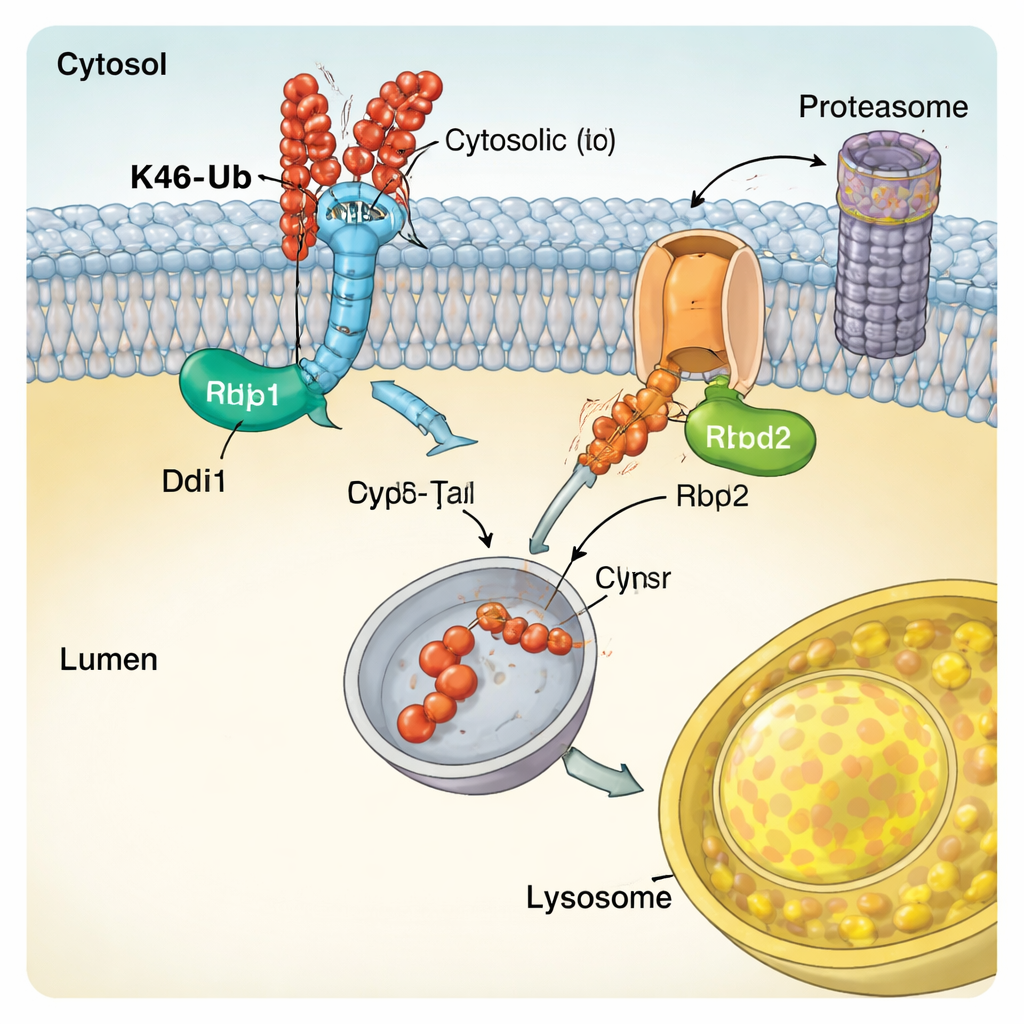
Specialiserade enzymer som läser ubiquitinkoden
För att förstå hur CUT-UP känner igen sina mål undersökte författarna Ddi1s molekylära egenskaper. De visade att Ddi1s centrala katalytiska kärna inte bara klipper proteiner utan också kan binda ubiquitin direkt, och att dess aktivitet ställs in av extra regioner som hakar fast vid ubiquitinkedjor. Ddi1 visade ett särskilt beroende av K48-länkade kedjor, i linje med dess roll i CUT-UP. Rbd2 å andra sidan är en rhomboid-proteas som spänner över membranet. Studien fann att Rbd2s aktiva säte är nödvändigt för att skära lumen-vända delar av Vps10 och att enzymet färdas genom flera sekretoriska kompartment, vilket gör att det kan verka på flera cellulära platser. Liknande enzymer finns i humana celler och har kopplats till tillstånd från neurodegeneration till cancer, vilket tyder på att CUT-UP-liknande mekanismer kan vara allmänt viktiga.
Varför detta är viktigt för hälsa och terapi
Genom att visa att olika ubiquitinkedjetyper skickar samma membranprotein in i skarpt skilda öden—antingen sortering till multivesikulära kroppar eller CUT-UP-medierad uppskärning—ger detta arbete starkt stöd för att celler använder en verklig "ubiquitin-kod" för att finjustera proteinborttagning. Upptäckten av CUT-UP klargör hur envisa membranproteiner kan demonteras bit för bit och lyfter fram Ddi1 och Rbd2 som nyckelspelare som läser och upprätthåller denna kod. För icke-specialister är slutsatsen att celler inte bara märker proteiner som skräp; de specificerar hur skräpet ska tas ut. När läkemedelsutvecklare utformar verktyg som märker skadliga proteiner med ubiquitin för att avlägsna dem, kommer förståelsen av vägar som CUT-UP vara avgörande för att förutsäga vilka fragment som bildas och hur det kan påverka cellens beteende.
Citering: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
Nyckelord: ubuitinkin-kod, proteinnedbrytning, membranproteiner, proteasom, lysosom