Clear Sky Science · sv
Förlust av Fsr‑quorum sensing främjar biofilmssbildning och förvärrar utfall vid enterokock‑endokardit
Tysta sabotörer på hjärtklaffarna
Infektiös endokardit är en livshotande infektion i hjärtklaffarna som blir allt vanligare globalt. Denna studie koncentrerar sig på en huvudmisstänkt, tarmbakterien Enterococcus faecalis, och undersöker varför vissa infektioner är särskilt svåra att behandla. Genom att avslöja hur dessa bakterier kommunicerar sinsemellan och bygger skyddande biofilmer på klaffarna visar forskarna varför vissa stammar ger mer allvarlig sjukdom och motstår antibiotika, och varför ett bakteriellt signalsystem kallat Fsr visar sig vara en överraskande broms snarare än en gas på skadan.
Hur bakterier bygger fästningar i hjärtat
Hjärtklaffarna utsätts normalt för en av kroppens snabbaste blodflöden, men om klaffytan skadas kan blodplättar och koagulationsproteiner bilda en liten koagelklump, en vegetation. Denna klump blir en landningsplats för bakterier i blodomloppet. När de väl fäster förökar sig bakterierna och väver ihop sig till en biofilm — en slemmig, strukturerad gemenskap som skyddar dem från immunceller och läkemedel. Forskarteamet använde mikroflödessystem för att efterlikna blodflöde i labbet och en råttmodell för att återskapa endokardit i levande djur, vilket gjorde det möjligt att iaktta hur E. faecalis anpassar sig när infektionen utvecklas från några utspridda celler till tjocka, mogna biofilmer. 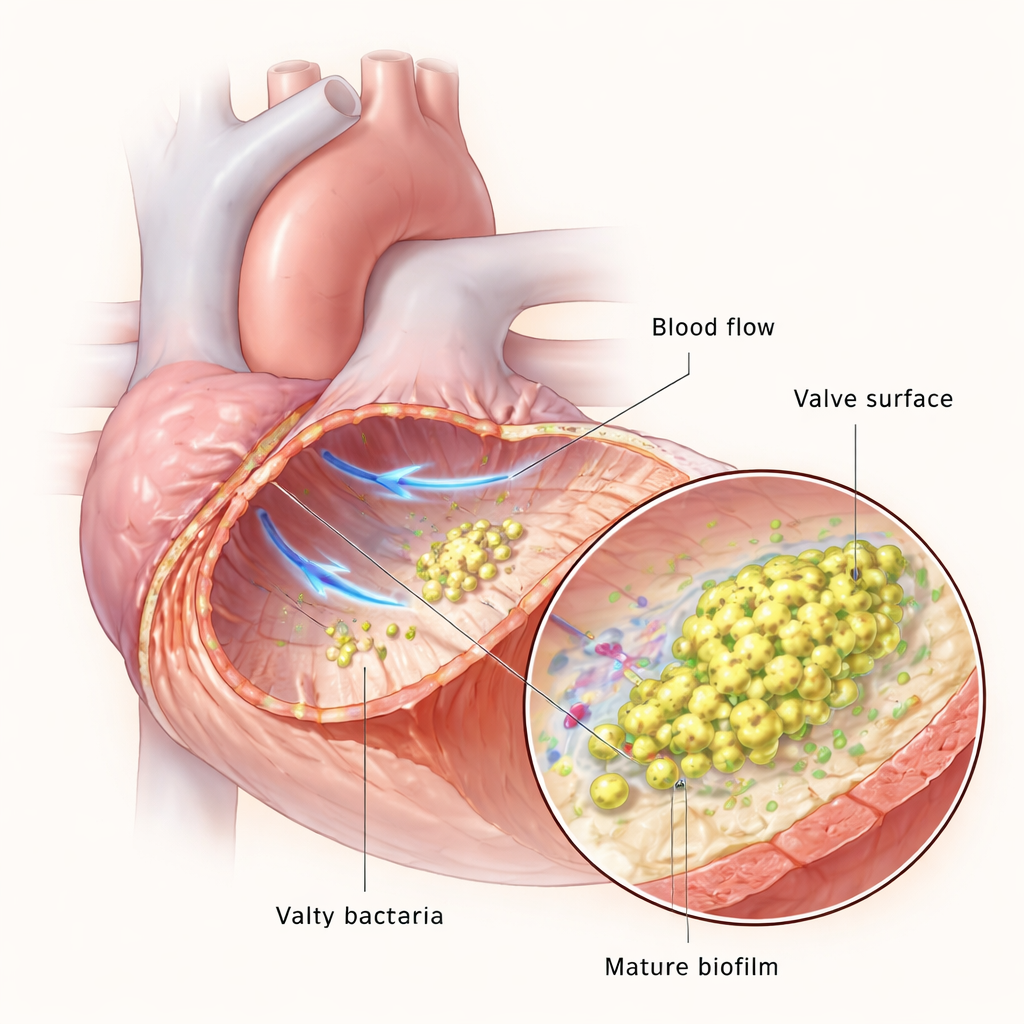
När starkt blodflöde tystar bakteriernas ”prat”
Bakterier samordnar ofta sitt beteende via quorum sensing, ett kemiskt ”omröstnings”system som slår av eller på gener när tillräckligt många celler finns på plats. Fsr är quorum sensing‑systemet som E. faecalis använder. Förvånande nog fann forskarna att kraftigt, rörligt vätskeflöde faktiskt sköljer bort de signalmolekyler som behövs för att Fsr ska aktiveras. Tidigt i infektionen, när bakterier sitter på den exponerade ytan av vegetationen och känner blodets fulla kraft, är Fsr i stort sett tyst. Först senare, när mikrokolonier växer till och blir begravda djupare inne i vegetationen — skärmade från flödet — aktiveras Fsr. Det innebär att quorum sensing i det verkliga hjärtat styrs inte bara av hur många bakterier som finns utan också var de sitter i den tredimensionella strukturen.
Att stänga av Fsr låter biofilmer växa ohejdat
För att testa vad Fsr faktiskt gör i infektionen jämförde teamet normala bakterier med mutanter som saknade hela Fsr‑systemet. I början koloniserade båda varianterna klaffarna lika väl. Men efter tre dagar hade djur infekterade med Fsr‑defekta stammar större vegetations‑massor och långt fler bakterier packade i dem. Detaljerad avbildning visade att deras biofilmer täckte mer av koagelns yta och att deras mikrokolonier var större. Förlust av Fsr slog också av två viktiga utsöndrade enzymer, GelE och SprE, som normalt hjälper till att forma biofilmen och kan begränsa överväxt. Djur infekterade med mutanter som saknade endast dessa enzymer utvecklade också klumpigare biofilmer, om än inte lika extrema som Fsr‑nullstammarna, vilket tyder på att andra Fsr‑reglerade faktorer också spelar in. 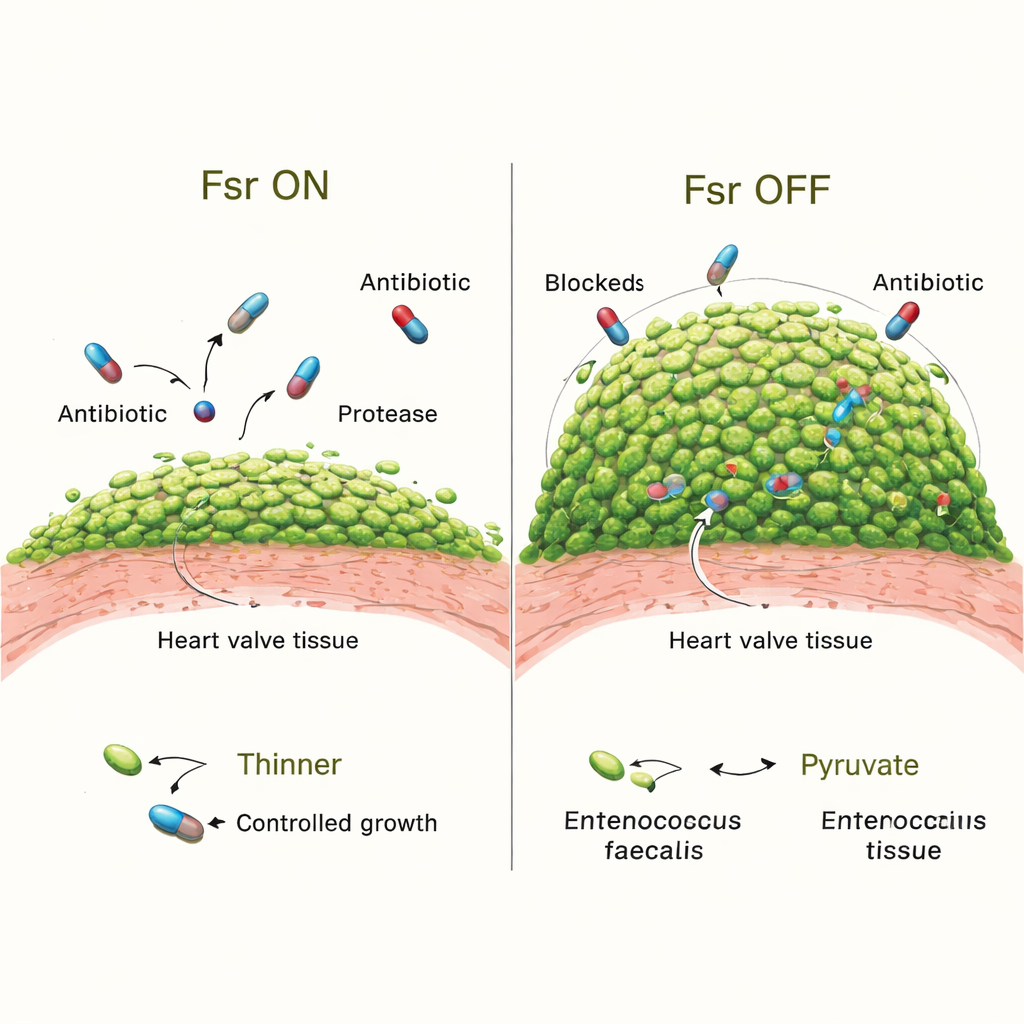
Metabol omkoppling och starkare grepp mot antibiotika
Genuttrycksprofilering av bakterier inne i infekterade klaffar visade att Fsr gör mer än att kontrollera ett par enzymer. Utan Fsr förändrades hundratals geners aktivitet, särskilt de som är involverade i upptag av socker och energiproduktion. Ett genpar, lrgA och lrgB, stack ut: de var kraftigt påslagna i Fsr‑defekta bakterier och hjälpte cellerna att bättre utnyttja pyruvat, en liten energirik molekyl som finns i blodet. När forskarna raderade lrgAB tillsammans med Fsr försvann den överdrivna biofilmsväxten, vilket pekar på en nyckelroll för denna metabola väg i att driva den överväxta infektionen. Anmärkningsvärt var att Fsr‑defekta biofilmer också var svårare att behandla. Hos råttor som fick antibiotikumet gentamicin krympte infektioner med normala bakterier och trombocytantalet — en markör för sjukdomsallvar — förbättrades. I kontrast svarade Fsr‑defekta infektioner knappt alls, trots att bakterierna i vanliga laboratorietester inte var mer läkemedelsresistenta.
En människospecifik tvist i inflammationen
Studien avslöjade också en möjlig väg som dessa bakterier kan trigga inflammation hos människor. Enzymet GelE kan klyva den mänskliga föregångaren till immunsignalen IL‑1β till en aktiv form som utlöser inflammatoriska svar. Intressant nog klyvde GelE rått‑IL‑1β annorlunda, genom att bryta ner den snarare än aktivera den, och den precisa aktiverande klyvningen saknades i rått‑ och musproteiner. Denna artspecifika effekt tyder på att GelE hos människor kan hjälpa till att rikta inflammationen precis vid biofilmens kant och därigenom förvärra vävnadsskada under endokardit.
Från bänk till vård: varför Fsr‑förlust betyder något för patienter
För att se om dessa experimentella fynd hade betydelse i verkligheten analyserade forskarna E. faecalis‑isolat från 81 patienter med infektiös endokardit i Schweiz och USA. Nästan hälften av stammarna saknade naturligt Fsr‑systemet. Patienter infekterade med dessa Fsr‑negativa stammar hade längre varande bakteriemi — fler dagar med påvisbara bakterier i blodet — och var mer benägna att hamna i en hög‑svårighetskategori som omfattade intensivvård, längre vårdtider, större hjärtingrepp eller död. Andra virulensgener kunde inte förklara detta mönster, vilket pekar direkt på Fsr‑förlust som en viktig markör för mer aggressiv sjukdom.
Varför detta spelar roll för framtida behandlingar
Tillsammans kullkastar dessa fynd den enkla uppfattningen att blockering av bakteriekommunikation alltid försvagar infektioner. Vid E. faecalis‑endokardit hämmar Fsr faktiskt biofilmsutbredning och gör bakterierna mer känsliga för antibiotika. När Fsr saknas bildar bakterier tätare biofilmer, utnyttjar blodets näringsämnen effektivare och bidrar till envisa, långdragna infektioner. För patienter innebär detta att stammar som saknar Fsr kan förutsäga svårare behandlingsfall, och att terapier som blint släcker quorum sensing kan få motsatt effekt i detta sammanhang. Istället kan riktade insatser mot metabola vägar som pyruvatanvändning, eller övervakning av Fsr‑ och GelE‑status som prognostiska markörer, erbjuda bättre sätt att hantera dessa farliga hjärtinfektioner.
Citering: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
Nyckelord: infektiös endokardit, bakteriella biofilmer, quorum sensing, Enterococcus faecalis, antibiotikatolerans