Clear Sky Science · sv
Ingenjörsdesignad VPg-saRNA uppnår kap-oberoende, lågimmunogen och precis kodning av terapeutiska proteiner in vivo
Omformar reglerna för RNA-läkemedel
Vacciner baserade på budbärar-RNA (mRNA) bidrog till att vända utvecklingen mot COVID-19, men att använda liknande molekyler för att ersätta eller komplettera saknade proteiner vid kroniska sjukdomar är mycket svårare. Kroppen tenderar att snabbt förstöra främmande RNA och att utlösa starka immunsvar, och många befintliga konstruktioner av självamplifierande RNA gör fel när de kopierar sig själva. Denna studie beskriver en ny typ av självamplifierande RNA—byggd från delar av humant norovirus—som är konstruerad för att vara långverkande, mindre inflammatorisk och ovanligt exakt, vilket öppnar dörren för mer precisa och beständiga RNA-läkemedel.
En smartare självkopierande RNA
Konventionella mRNA-läkemedel bär på ett enda ”recept” för ett protein och läses en gång av cellen innan de bryts ner. Självamplifierande RNA (saRNA) inkluderar extra viralt maskineri som låter RNA kopiera sig självt i celler, vilket kraftigt förstärker produktionen från en liten dos. De bäst studerade saRNA-systemen kommer från alfavirus, men de är otympliga, utlöser starka antivirala försvar och kopierar sina sekvenser med relativt låg noggrannhet. Författarna vände sig istället till humant norovirus, en vanlig orsak till magsjuka. De isolerade ett kompakt avsnitt av norovirusets genetiska material och byggde om det som en bärare för terapeutiska gener. I dess kärna finns VPg, ett litet viralt protein som är kemiskt bundet till RNA:ts framsida. VPg ersätter den vanliga ”cappen” som finns på humana mRNA och tillåter att RNA översätts av en annan uppsättning cellulära faktorer som är mindre känsliga för vissa stressignaler. 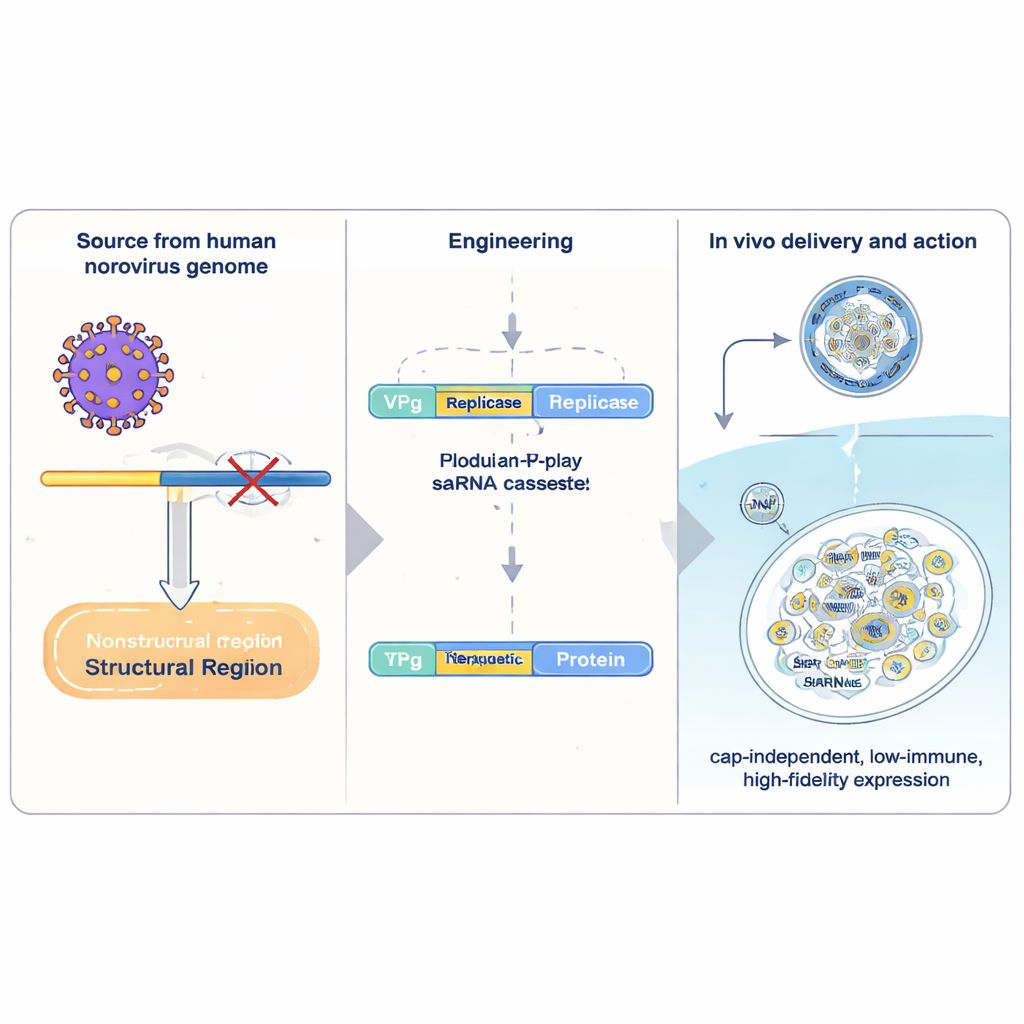
Hög noggrannhet utan att väcka immunitet
För proteinterapier spelar noggrannhet roll: även små kopieringsfel kan förändra ett läkemedels beteende eller skapa toxiska biprodukter. Teamet visade att när norovirus-VPg binder till virusets RNA-kopierande enzym (en polymeras) saktar det hastigheten med vilken felaktiga byggstenar läggs till, vilket kraftigt minskar felkvoten. De identifierade specifika aminosyror i VPg som kontaktar en nyckelkontrollregion i polymeraset och demonstrerade att störning av detta gränssnitt gör kopieringen mindre exakt. Samtidigt skapar klassiska saRNA-konstruktioner stora mängder dubbelsträngat RNA, en molekylär larmklocka som aktiverar antivirala försvar och släcker ned proteinproduktion. Genom att omdesigna polymeraset för att föredra en särskild VPg-länkad startform och genom att omarrangera genomet så att endast den terapeutiska strängen effektivt produceras, minskade författarna i hög grad bildningen av dubbelsträngat RNA. De finslipade också en svansregion av RNA så att VPg fäster på rätt ställe, vilket förhindrar korta, oavsiktliga fragment som annars kunde översättas till vandrande peptider.
Fungerar där standard-mRNA misslyckas
Den nya VPg-baserade saRNA testades sedan i krävande sjukdomssammanhang där vanlig cappad mRNA har svårt att fungera. Vid cancerassocierad kachexi—ett avmagringssyndrom där muskler och fett försvinner—stängs viktiga translationsfaktorer som känner igen den standardmässiga mRNA-cappen av, vilket gör kapberoende mRNA ineffektiva. Eftersom VPg använder en alternativ ingång till cellens translationsmaskineri fortsatte det att driva produktionen av aptit- och ämnesomslättningshormonet ghrelin i en musmodell för pankreascancer. Månatliga lågdosinjektioner hjälpte till att bevara muskel och fett, förbättrade matintag och ämnesomsättning, och förlängde överlevnaden måttligt, utan uppenbar toxicitet eller tecken på kronisk immunaktivering.
Precision mot cancer och lugnare autoimmunitet
För att testa om högfidelitetskopiering verkligen spelar roll laddade forskarna VPg-vektorn med en komplex onkolytisk konstruktion, GSDMDENG, designad för att göra hål i cancercellernas mitokondrier och stimulera tumörspecifika immunrespons. När samma konstruktion placerades på ett konventionellt alfavirus-saRNA ackumulerades mutationer över upprepade kopieringsomgångar och försvagade dess selektiva cancer-dödande och immun-primande funktioner. I kontrast bevarade VPg-systemet den avsedda sekvensen, producerade stark cancercellsdöd och utlöst hållbara T-cellsvar som bromsade eller förhindrade pankreascancer i musmodeller. Slutligen tillämpade de VPg-saRNA på en annan utmaning: kronisk graft-versus-host-sjukdom, där immunceller attackerar lungorna efter benmärgstransplantation. En VPg-saRNA som kodade för aktiverat protein C minskade skadliga antikroppsbildningar, förhindrade lungsammandragning och förbättrade andningen hos möss, medan en jämförbar alfavirusbaserad konstruktion framkallade starkare medfödd immunitet och försämrade utfallen.
Varför detta betyder något för framtida RNA-läkemedel
Sammantaget beskriver arbetet en kompakt, ”plug-and-play” RNA-plattform som kombinerar tre önskvärda egenskaper: den kopierar sig själv med hög noggrannhet, den är utformad för att minimera immunlarm, och den kringgår några av flaskhalsarna som begränsar standard-mRNA-translation. Eftersom den terapeutiska genen enkelt byts in i en fast norovirusbaserad ryggrad kan många olika proteiner—från hormoner till koagulationsreglerare till onkolytiska medel—testas på samma chassi. Medan mycket arbete återstår innan användning på människor antyder denna VPg-saRNA-metod en väg mot RNA-läkemedel som beter sig mer som stabila proteininfusioner: låg dos, längre varaktighet och anpassade för att fungera även i sjuka vävnader där vanliga mRNA-meddelanden inte kan läsas pålitligt. 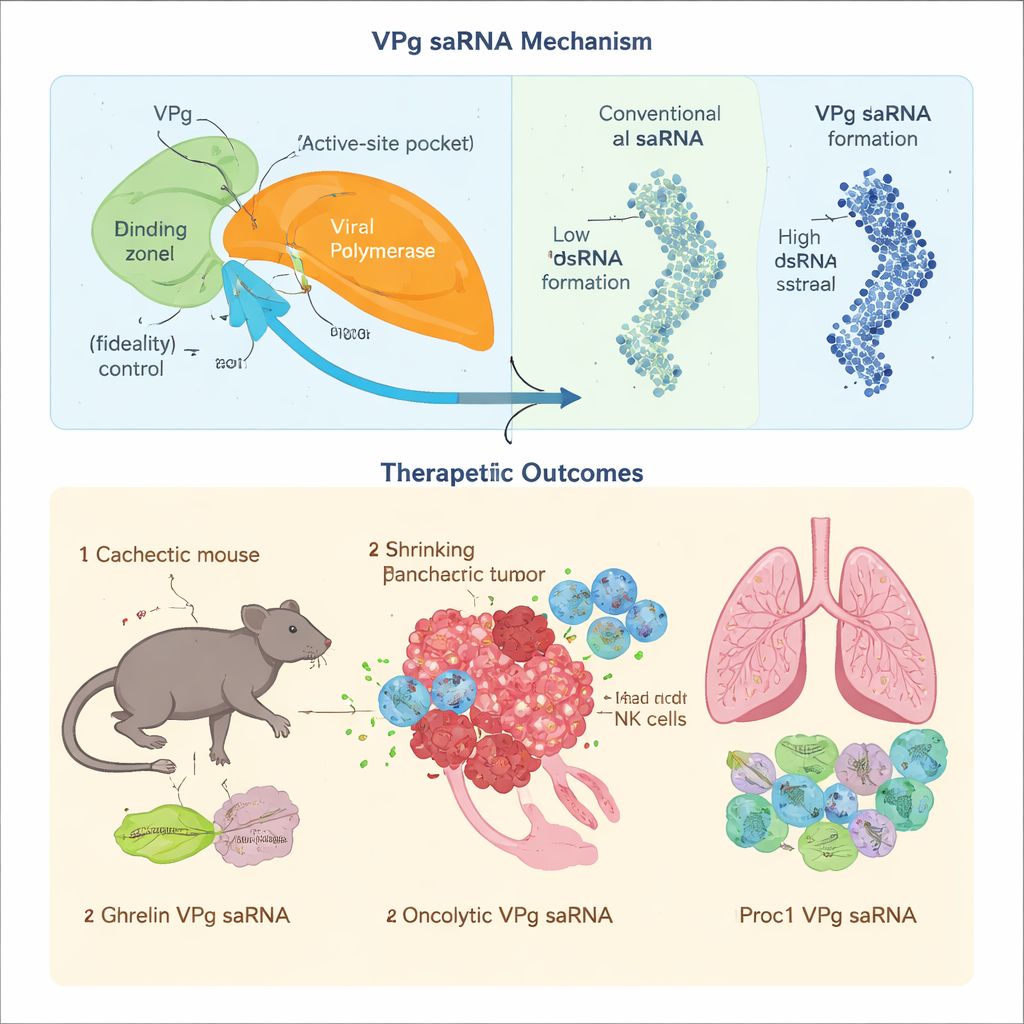
Citering: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
Nyckelord: självamplifierande RNA, mRNA-terapier, norovirus VPg, cancerkachexi, graft-versus-host-sjukdom