Clear Sky Science · sv
Transkriptomiska signaturstyrda utarmningar av intermediära alveolära epitelceller förbättrar lungsfibros hos möss
Varför ärrade lungor spelar roll
Lungsfibros är en allvarlig lungsjukdom där de känsliga luftblåsorna gradvis omvandlas till stel ärrvävnad, vilket gör varje andetag ansträngande. Läkare vet att detta ärrbildande börjar när normala reparationsprocesser spårar ur, men det har varit oklart vilka specifika celler som bär skulden och hur man kan avlägsna dem utan att skada frisk lungvävnad. Denna studie undersöker ett nytt sätt att ”läsa” de molekylära budskapen inne i lungceller, använda den informationen för att identifiera skadliga transit-celler och selektivt eliminera dem för att minska ärrbildning hos möss.
Celler fångade mitt i felaktig reparation
Efter lungskada förökar sig specialiserade surfaktantproducerande celler, kallade typ II-celler, normalt och mognar sedan till tunna typ I-celler som bekläder luftblåsorna och tillåter syre att passera till blodet. Vid fibros fastnar många av dessa celler i ett mellanläge, eller transitoriskt tillstånd, istället för att fullfölja denna omvandling. Tidigare single-cell RNA-sekvenseringsstudier hade funnit dessa intermediära celler både hos möss och människor, men det var oklart om de bara var åskådare eller nyckeldrivare i sjukdomen. Författarna fokuserade på en mus-transitionscellstyp kallad Krt8+ alveolar differentiation intermediates, och deras mänskliga motsvarigheter kända som aberranta basaloida celler, som förekommer i hög grad i ärrade lungor.
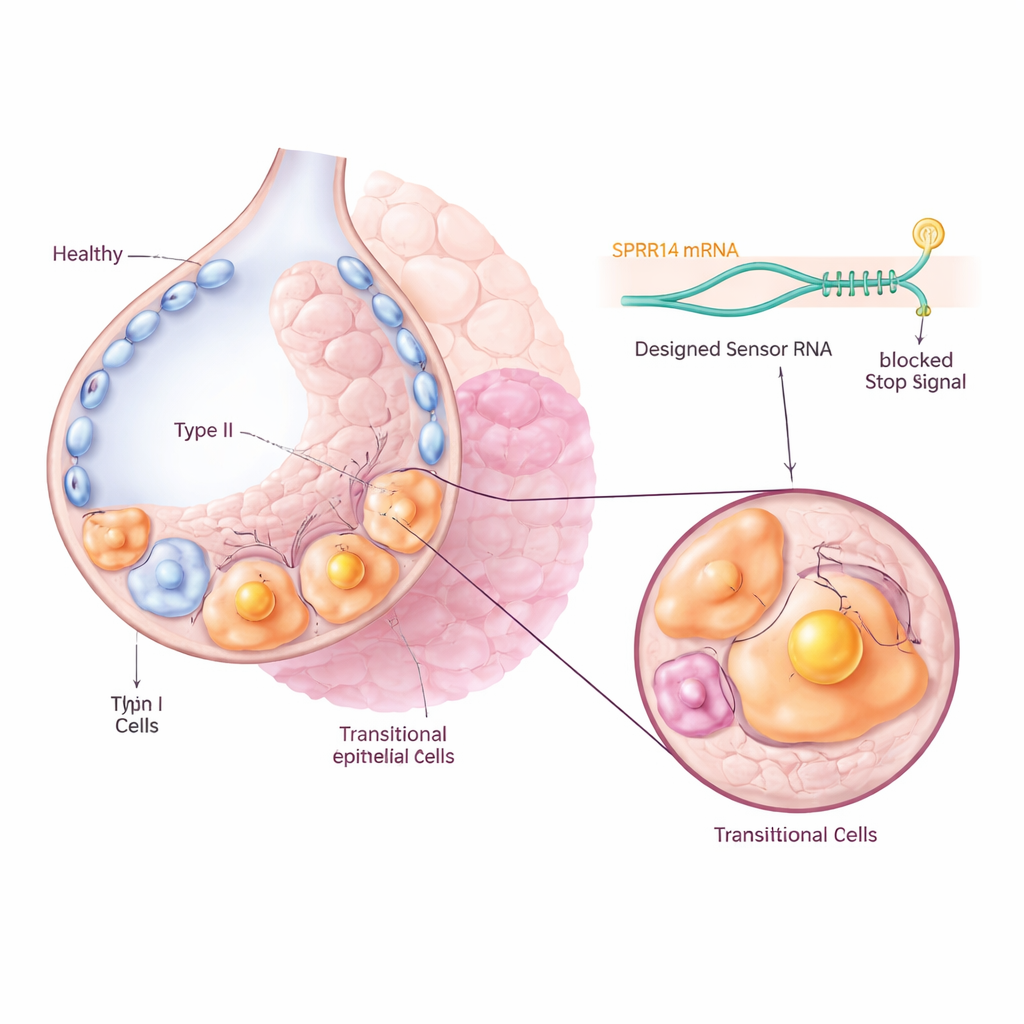
Att hitta ett unikt molekylärt namnskylt
För att rikta in sig på dessa problemceller utan att påverka deras friska grannar sökte teamet först i stora genuttrycksdatamängder efter en markör som var starkt och specifikt påslagen i den transitiva populationen. De identifierade en molekyl kallad SPRR1A som en framträdande ”namnskylt”: den var starkt berikad i Krt8+ intermediära celler i fibrotiska muslungor och i KRT5-/KRT17+ aberranta basaloida celler från patienter med idiopatisk lungsfibros, men i hög grad frånvarande i normala lungceller. Mikroskopi av både mus- och människolungvävnad bekräftade att SPRR1A främst dök upp i skadade, ombyggda regioner och inte i friska luftblåsor, vilket tyder på att den kan fungera som ett precist grepp för att identifiera de skyldiga cellerna.
Programmera celler med en RNA-sensor
Forskarna använde därefter en nyligen utvecklad teknik kallad CellREADR, som fungerar som en intern molekylär sensor. De designade korta RNA-sekvenser som kan baspara med SPRR1A-RNA inne i en cell. När sensorn upptäcker SPRR1A utlöser den produktionen av ett kopplat ”effektor”-protein, såsom en fluorescerande markör eller en receptor som gör cellen känslig för ett läkemedel. Hos möss användes virus för att leverera dessa sensor–effektor-konstruktioner till lungceller. Endast celler som aktivt producerade SPRR1A slog på den fluorescerande signalen, vilket gjorde det möjligt för teamet att spåra och isolera transitceller direkt från fibrotiska lungor. Single-cell-sekvensering visade att de märkta cellerna överensstämde väl med den kända transitiva gen-signaturen, vilket bekräftade att RNA-sensorn träffade den avsedda populationen korrekt.
Släcka farliga intermediärer
Nästa steg var att byta effektorn från ett ofarligt fluorescerande protein till difteritoxinreceptorn, så att SPRR1A-positiva celler selektivt kunde dödas genom administrering av difteritoxin. Genom att tajma behandlingen till toppmängden av transitceller efter kemiskt orsakad lungskada lyckades författarna ta bort ungefär en tredjedel av denna population. Denna riktade utarmning ledde till påtagligt mindre lungärr: det fanns mindre kollagenansamling, lägre nivåer av fibrotiska proteiner och mer normalutseende luftblåsestrukturer. Detaljerade analyser visade att de flesta SPRR1A-positiva celler bar tecken på ett stressat, åldringsliknande tillstånd, med en liten undergrupp kapabel till hög proliferation, vilket tyder på att dessa intermediärer både misslyckas med att reparera vävnaden korrekt och bidrar till att upprätthålla den fibrotiska processen.
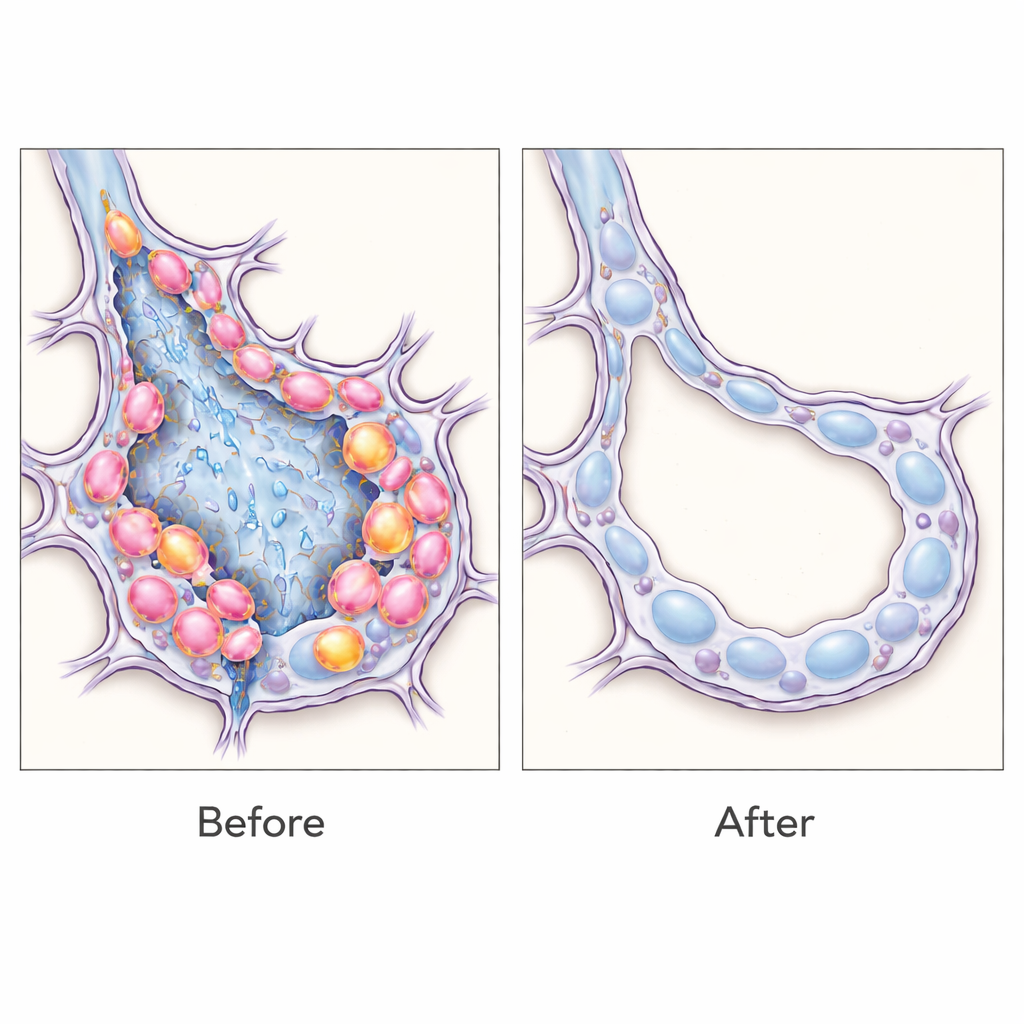
Vad detta innebär för framtida behandlingar
Dessa fynd talar för att transitiva epitelceller inte bara är markörer utan aktiva drivkrafter bakom lungsfibros, och att selektiv eliminering av dem kan återställa balansen mot en hälsosammare lungarkitektur hos möss. Mer generellt visar arbetet en flexibel strategi: genom att ”läsa” cellspecifika RNA-signaturer kan forskare märka, studera och till och med avlägsna snävt definierade cellpopulationer i levande vävnad utan att behöva skapa skräddarsydda djurmodeller varje gång. Även om mycket återstår innan sådana RNA-avkännande verktyg säkert kan anpassas för människor, öppnar detta tillvägagångssätt en väg mot precisionsbehandlingar som riktar sig mot de exakta celltyper som stjälper läkningen vid kronisk lungärrbildning och potentiellt andra fibrotiska sjukdomar.
Citering: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
Nyckelord: lungsfibros, alveolära epitelceller, single-cell RNA-sekvensering, RNA-avkänningsteknik, cellulär senescens