Clear Sky Science · sv
Atlas över enskilda kärnor i centrala amygdala avslöjar kromatin- och gentranskriptionsdynamik vid alkoholbrukssyndrom hos människa
Varför denna forskning är viktig för vardagen
Alkoholbrukssyndrom (AUD) drabbar miljontals människor och deras familjer, men vi vet fortfarande förvånansvärt lite om vad långtidsöverdrivet drickande gör med den mänskliga hjärnan på nivåer av enskilda celler. Denna studie zoomar in på en liten men kritisk region — centrala amygdala, en nod för rädsla, stress och motivation — för att kartlägga hur alkohol omformar hjärnceller och deras genetiska kontrollsystem. Genom att kombinera toppmodern ”single‑cell” sekvensering med genetiska studier av beroenderisk börjar författarna förklara varför vissa människor är mer sårbara för AUD och hur alkohol lämnar bestående molekylära ärr i hjärnan.
Noga granskning av en liten hjärnknutpunkt
Centrala amygdala är en viktig utgångsstation i hjärnans känslo- och stressnätverk och hänger starkt ihop med ångerlindring, sug och tvångsmässigt alkoholbruk. I detta arbete analyserade forskarna ungefär 175 000 enskilda cellkärnor tagna post mortem från centrala amygdala hos 50 personer — 22 med historik av alkoholbrukssyndrom och 28 utan AUD. Med en teknik som läser både genaktivitet (RNA) och kromatinåtkomst (hur ”öppet” eller ”stängt” DNA är) i samma cell byggde de en detaljerad atlas över alla större hjärncellstyper i denna region, inklusive flera typer av neuron och stödjeceller såsom astrocyter och mikroglia. De fann att inhibitoriska neuron — som dämpar eller formar hjärnaktivitet — är särskilt talrika i centrala amygdala och verkar vara särskilt påverkade hos personer med AUD. 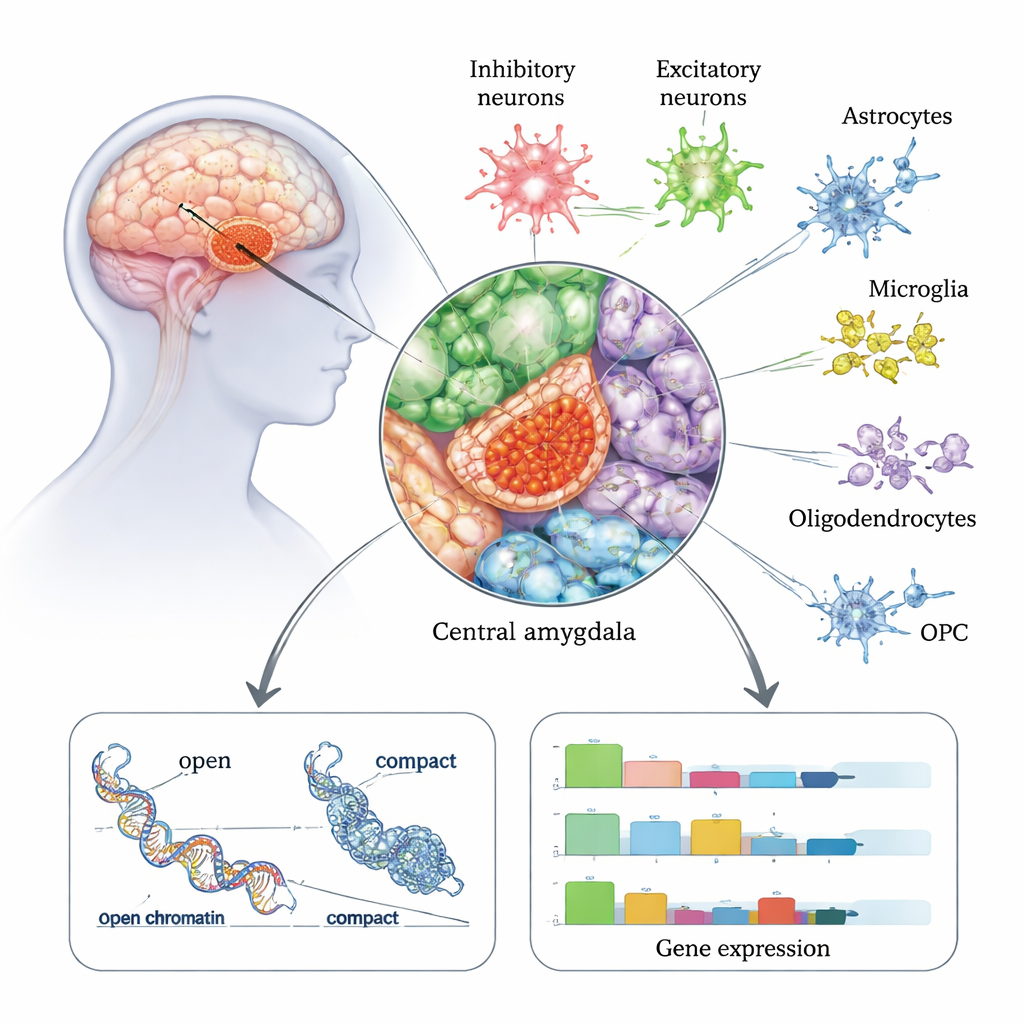
Vilka celler och gener förändras vid alkoholbrukssyndrom?
Teamet jämförde systematiskt genaktivitet hos personer med och utan AUD, celltyp för celltyp. De upptäckte mer än 1 800 gener vars aktivitet var förändrad i specifika cellpopulationer, med de största skiftena i inhibitoriska neuron, följt av excitatoriska neuron och astrocyter. En undergrupp av inhibitoriska neuron markerad av peptiden proenkephalin (PENK) visade särskilt starka förändringar. Många av de påverkade generna är inblandade i kommunikationen mellan hjärnceller, särskilt balansen mellan den excitatoriska signalen glutamat och den inhibitoriska signalen GABA. Till exempel var genen GABRA2, som hjälper till att bygga en huvudtyp av GABA‑receptor, ökad i vissa inhibitoriska neuron, medan GRM8, en glutamatreceptor, och NCAM1, ett cell‑adhesionsmolekyl viktigt för synapser, ändrades i motsatta riktningar över neuronundergrupper. Dessa mönster tyder på att finjusteringen av excitation och inhibition i centrala amygdala störs vid AUD.
Hjärnans kontrollströmbrytare: kromatin och regulatoriska element
Gener agerar inte ensamma; de styrs av DNA‑sträckor som fungerar som strömbrytare och dimrar. Genom att studera kromatin — hur DNA är paketerat — identifierade forskarna mer än en halv miljon kandidatregulatoriska element och kopplade dem till närliggande gener på ett celltypsspecifikt sätt. Nästan hälften av dessa element var unika för en enda celltyp, vilket lyfter fram hur specialiserade olika hjärnceller är. Många regulatoriska element som förändrades vid AUD var kopplade till gener involverade i kalciumhantering och glutamatsignalering, såsom CALN1, en kalciumbindande gen starkt aktiv i neuron. I inhibitoriska neuron visade CALN1 både ökad uttrycksnivå och täta kluster av regulatoriska slingor, vilket antyder att alkoholexponering omformar den lokala DNA‑arkitekturen som kontrollerar denna gen. 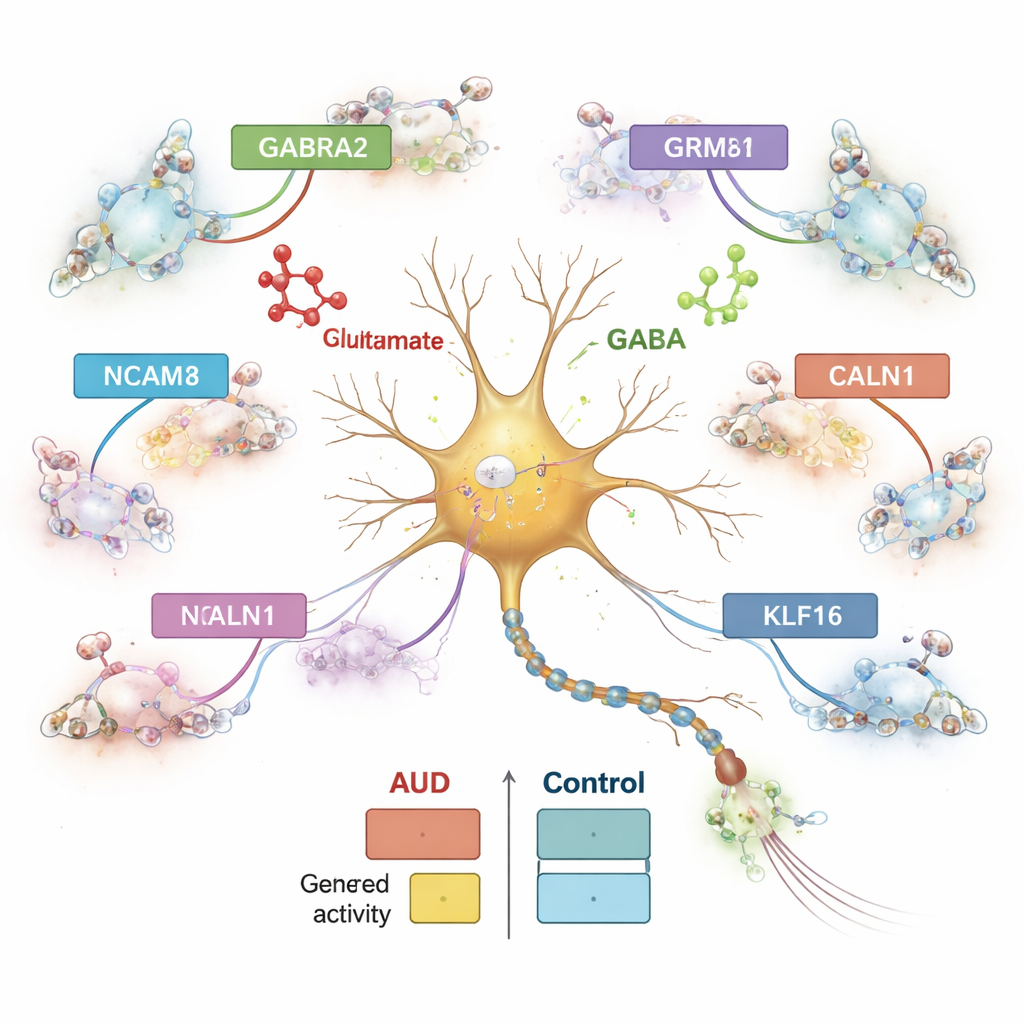
Från riskgener till verkliga hjärnförändringar
Genetiska studier har identifierat många DNA‑varianter som ökar risken för att utveckla alkoholproblem, men var och hur de verkar i hjärnan har varit oklart. Genom att lägga sina single‑cell‑kartor över stora genomewide associationsstudier av problematiskt alkoholbruk fann författarna att riskgener är oproportionerligt aktiva och dysreglerade i neuroner i centrala amygdala, särskilt i inhibitoriska sådana. De pekade ut över 200 troliga orsakliga riskvarianter som sitter inne i regulatoriska element som är öppna i specifika celltyper. Några föll i eller nära gener som redan kopplats till beroende, såsom CACNA1C och DRD2, som hjälper styra neuronal excitabilitet och dopaminsignalering. Andra, inklusive SEMA6D och NF1, framstod som nya kandidater. Teamet identifierade också en familj av transkriptionsfaktorer kallade Kruppel‑liknande faktorer (framför allt KLF16) som tycks samordna omfattande förändringar i kalcium‑ och glutamatrelaterade gener, och de bekräftade delar av detta regulatoriska nätverk i en musmodell för akut alkoholexponering.
Vad detta betyder för förståelsen och behandlingen av AUD
Enkelt uttryckt visar denna studie att alkoholbrukssyndrom inte bara är ett diffust hjärnproblem utan en högst organiserad störning koncentrerad till särskilda celltyper och molekylära vägar inom en kritisk känslonod. Inhibitoriska neuron i centrala amygdala, tillsammans med astrocyter och andra stödjeceller, uppvisar koordinerade förändringar i genaktivitet och i DNA‑strömbrytarna som kontrollerar dessa gener — särskilt i system som hanterar glutamat, GABA och kalciumsignaler. Genom att koppla dessa cellulära förändringar till genetiska riskvarianter erbjuder arbetet en karta som förbinder ärftlig sårbarhet med konkreta molekylära händelser i hjärnan. Med tiden kan sådana cell‑specifika kartor vägleda utvecklingen av mer precisa behandlingar som återställer balansen mellan excitation och inhibition, istället för att verka brett över hela hjärnan.
Citering: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
Nyckelord: alkoholbrukssyndrom, centrala amygdala, single-cell genomik, inhibitoriska neuron, genreglering