Clear Sky Science · sv
Från TDP-43/RNA-komplexbildning till sjukdomsrelaterad TDP-43-aggregatbildning genom en strukturell och cellulär metod
Varför detta hjärnprotein är viktigt
Neurodegenerativa sjukdomar som amyotrofisk lateralskleros (ALS) och frontotemporal demens kännetecknas ofta av klumpar av felveckade proteiner inne i nervcellerna. En av de vanligaste bovarna är ett protein kallat TDP-43, som normalt hjälper till att bearbeta RNA — arbetskopian av våra gener. Denna studie ställer en avgörande fråga: vad gör TDP-43 i friska celler, och vad går fel så att en nyttig RNA-hjälpare förvandlas till ett giftigt protein som bildar aggregat?
Hur TDP-43 fungerar i friska nervceller
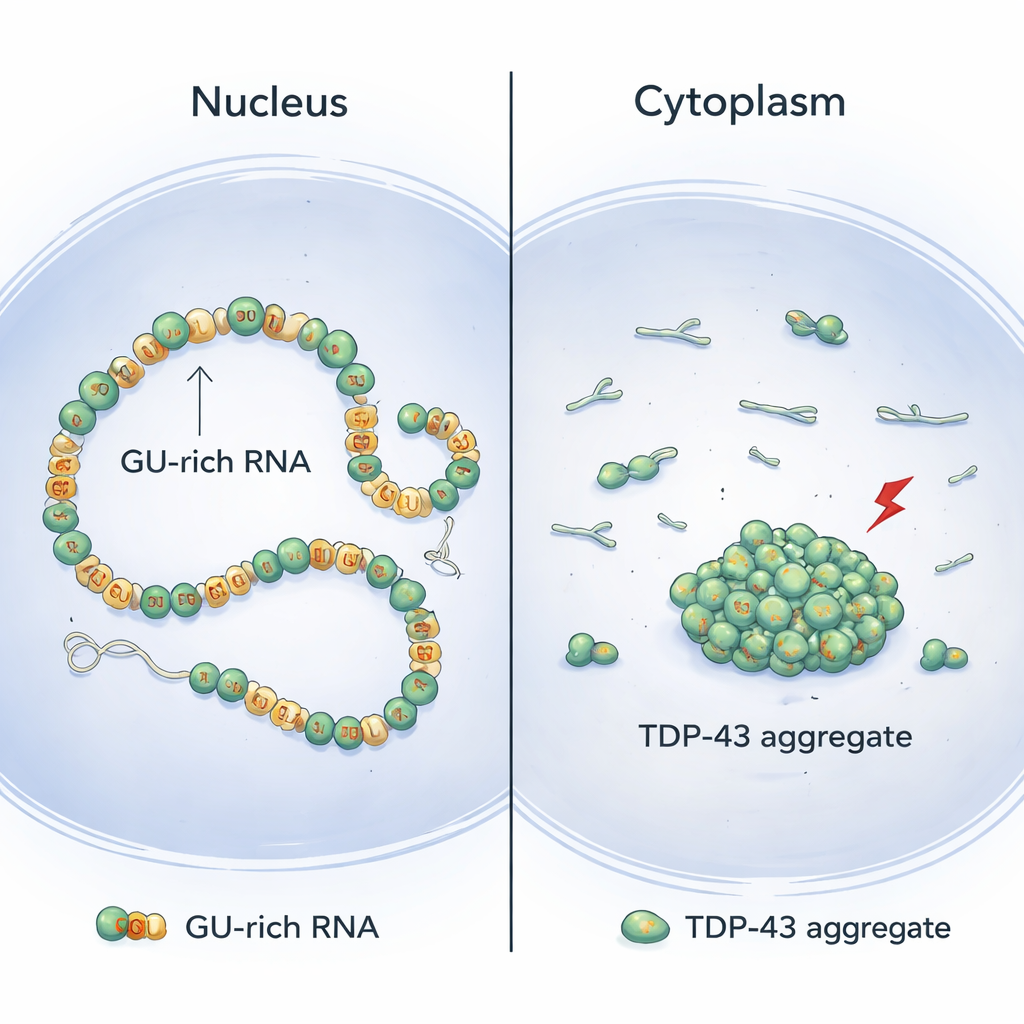
TDP-43 finns vanligen i cellkärnan, där det binder långa RNA-sekvenser rika på upprepade "GU"-byggstenar. Med en kombination av strukturell biologi och cellexperiment visar författarna att TDP-43-molekyler lägger sig på rad kooperativt längs dessa GU-rika regioner och bildar jämna, kontinuerliga kedjor på RNA:t. När de är ordnade på detta sätt hålls proteinets främre ände — dess N-terminala domän — fysiskt separerad mellan intilliggande molekyler. Som en följd förblir dessa N-terminala segment tillgängliga för att nå över och koppla ihop avlägsna GU-rika delar av samma RNA, vilket mjukt loopar och kompakta långa introner (de icke-kodande sekvenserna i gener) utan att bilda klumpar.
En inbyggd dragkamp i proteinet
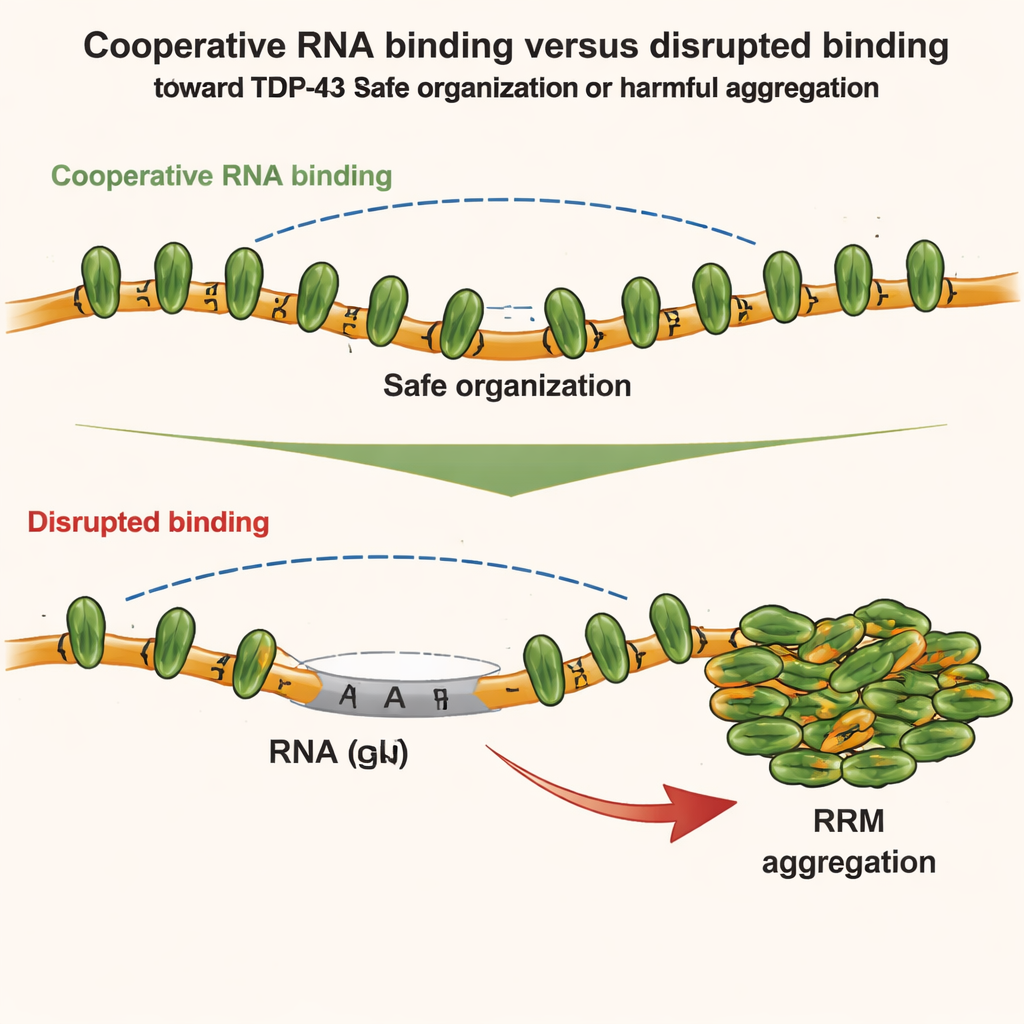
Teamet undersökte sedan hur olika delar av TDP-43 konkurrerar eller samarbetar med varandra. De fokuserade på två regioner: den N-terminala domänen, som kan fästa vid andra N-terminala domäner, och de centrala RNA-bindande modulerna, som driver kooperativ bindning längs GU-rikt RNA. Med känsliga tekniker som NMR-spektroskopi, kalorimetri och småvinkelröntgenspridning fann de att när TDP-43 binder RNA kooperativt, försvagar kedjans geometri faktiskt direkta N-terminal-till-N-terminal-kontakter mellan intilliggande molekyler. Med andra ord håller stark kooperativ RNA-bindning lokala N-terminala interaktioner i schack. Men när denna kooperativitet bryts — till exempel genom att infoga icke-GU-sekvenser i RNA eller genom att mutera TDP-43 — kommer N-terminala regioner på närliggande proteiner nära varandra och kan nu haka i varandra.
Från hjälpsam kompaktering till skadlig ocklusion
Dessa strukturella insikter testades i levande celler. Författarna använde konstruerade cellsystem för att följa hur olika TDP-43-mutanter blandar sig eller separerar inne i artificiella RNA-rika compartment. De fann att både kooperativ RNA-bindning och N-terminala interaktioner hjälper till att organisera TDP-43 i högre ordningens sammankomster, men på olika sätt. Kooperativ bindning radar upp proteiner längs GU-rikt RNA, medan N-terminala kontakter kopplar ihop avlägsna kluster. Under mild oxidativ stress skiftar dock bilden. En kemisk stressor (arsenit) orsakar specifika kemiska förändringar — acetylering — på de centrala RNA-bindande motiven, vilket gör dem benägna att klibba ihop. Om den kooperativa bindningen till RNA är intakt förblir TDP-43 till största delen lösligt. Om kooperativiteten försvagas fungerar N-terminala länkar mellan närliggande TDP-43-molekyler som ett ställverk som för samman de acetylerade kärnorna och uppmuntrar oåterkallelig aggregation.
Varför TDP-43 klumpar mer i cytoplasman
Den modell som växer fram ur detta arbete hjälper till att förklara varför TDP-43-aggregat ofta hittas i cytoplasman hos sjuka neuroner snarare än i kärnan. I kärnan är långa introner med många GU-upprepningar vanliga, vilket gynnar kontinuerlig, kooperativ bindning som håller riskfyllda N-terminala kontakter mellan grannar låga och istället tillåter säker långdistansloopning. I cytoplasman, däremot, har mogna RNA långt färre GU-rika sträckor. Det gör TDP-43-bindningen mer fläckvis och mindre kooperativ, vilket ökar chansen att intilliggande N-terminala domäner interagerar och banar väg för aggregation när stressinducerade kemiska förändringar inträffar. Som stöd för denna bild minskade konstgjort tillskott av extra GU-rika introner i kärnan TDP-43-aggregation under stress.
Vad detta betyder för framtida terapier
Enkelt uttryckt målar studien upp TDP-43 som ett protein i balans mellan hjälpsam RNA-organisation och skadlig klumpbildning, där kooperativ bindning till GU-rikt RNA fungerar som en säkerhetsmekanism. När den säkerhetsnätet brister — på grund av förändrade RNA-sekvenser, proteinmutationer eller cellulär stress — kan samma domäner som normalt kompakta långa RNA-segment istället driva bildandet av giftiga aggregat. För icke-specialister är huvudpoängen att upprätthållandet av rätt slags interaktioner mellan TDP-43 och RNA kan vara en lovande strategi för att förebygga eller bromsa den proteinklumpning som ses vid ALS och relaterade hjärnsjukdomar.
Citering: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
Nyckelord: TDP-43-aggregation, RNA-bindande proteiner, ALS, protein–RNA-interaktioner, neurodegeneration