Clear Sky Science · sv
Atomärt precis ligandteknik för guldbeläggning av nanopartiklar via fasgräns-masstransport
Varför små guldpartiklar spelar roll för hälsa
Medicinsk avbildning förlitar sig i allt högre grad på nanopartiklar — små partiklar några tusen gånger tunnare än ett människohår — för att belysa organ och tumörer djupt inne i kroppen. Denna studie visar hur forskare nu kan finjustera ytskiktet på ultrasmå guldförband nästan atom för atom, så att samma lysande kärna kan styras mot olika organ, i synnerhet förskjutas från lever och mjälte till njurarna. Sådan kontroll kan hjälpa till att utforma säkrare kontrastmedel och läkemedelsbärare som når dit läkaren vill och lämnar kroppen renare.
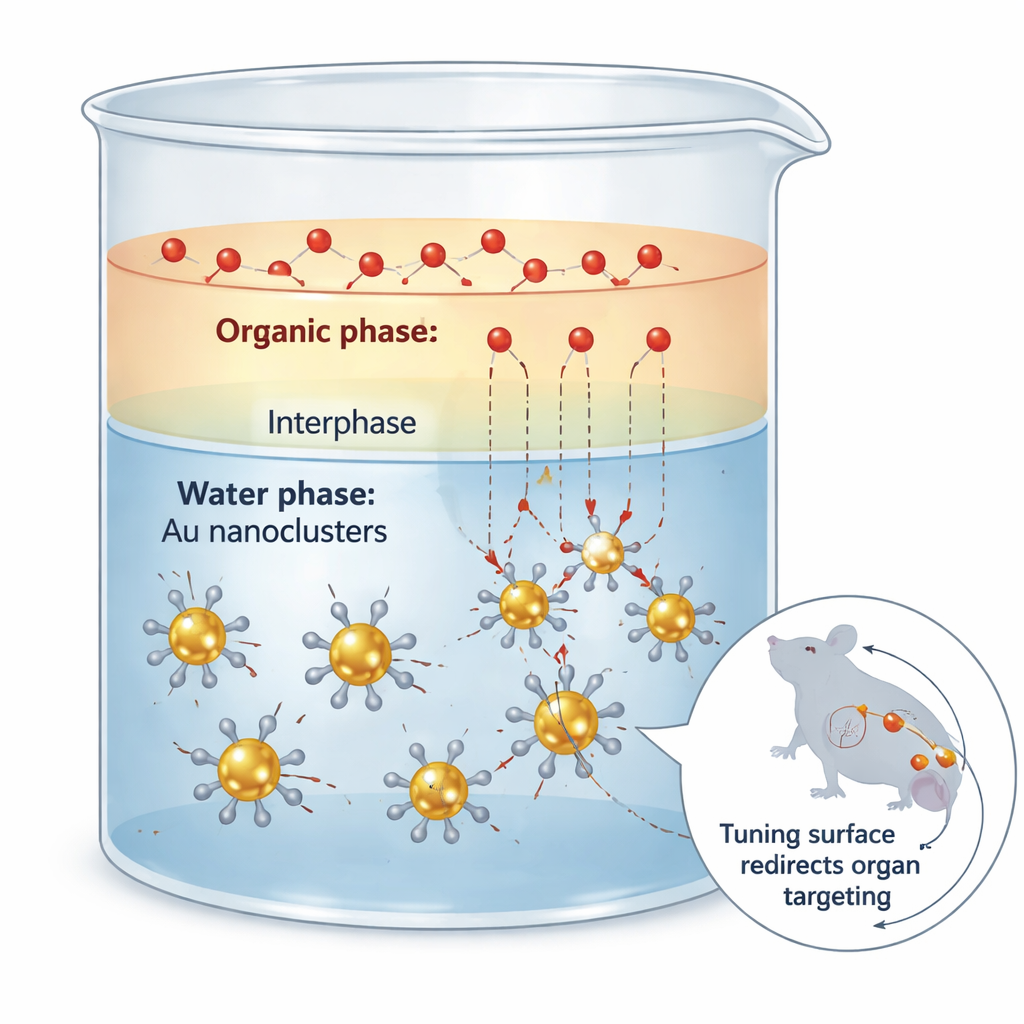
Utmaningen att klä upp små guldkluster
Guldnanokluster är ultrasmå gulpartiklar som beter sig mer som stora molekyler än som metallkorn. De kan avge ljus i det nära-infraröda II-intervallet, vilket tränger djupt in i vävnad och ger skarpa bilder med låg bakgrund. Nästan allt som bestämmer hur dessa kluster beter sig i kroppen — var de reser, hur länge de cirkulerar och hur de rensas bort — beror dock inte på guldet självt utan på de organiska liganderna, eller ”skal”-molekylerna, bundna till ytan. Traditionella sätt att ändra detta skal fungerar ofta som grov kirurgi: reaktionen går för snabbt, beläggningen blir ojämn och gulkärnan kan delvis frätas bort, vilket förstör både struktur och optiska egenskaper.
Att bromsa trafiken mellan två vätskor
Forskarna tacklade problemet genom att utnyttja en enkel fysikalisk idé: masstransportresistens vid gränsytan mellan två vätskor som inte helt blandas. De placerade guldklustren i vatten och de inkommande svavelbaserade liganderna i ett organiskt lösningsmedel som etylacetat. I det tunna skikt där de två vätskorna delvis blandas diffunderar ligander långsamt mot klustren och byter ut det ursprungliga skalet. Noggranna kinetiska mätningar visade att den oönskade ”frätningen” av gulkärnan är extremt känslig för ligandkoncentrationen, medan den önskade utbytet är mycket mindre känsligt. Genom att använda tvåfasuppställningen för att hålla fria ligandnivåer låga men kontinuerligt påfyllda, kunde teamet undertrycka frätningen med ungefär sextiofalt samtidigt som man bevarade det mesta av den nyttiga utbyteshastigheten.
Bygga ett precist molekylärt verktygslåda
Med denna interfas-assisterade metod kunde författarna byta ut ytliga ligander på en modellguldkluster, Au25, på ett mycket kontrollerat sätt. De började från kluster skyddade av en negativt laddad sulfonisk syra-ligand och bytte in en mängd nya tiol-ligander som bar karboxylsyror, aminer, hydroxylgrupper, nitrogrupper och hydrofoba aromatiska ringar. Masspektrometri visade rena, väldefinierade blandningar som Au25-kluster med specifika antal av varje ligandslag, istället för breda, röriga fördelningar. Metoden fungerade också för andra klusterstorlekar och ligandfamiljer, vilket tyder på att det är en generell strategi för att skapa robusta, skräddarsydda guldnanokluster för olika tillämpningar.
Styra nanopartiklar från levern till njurarna
Det mest slående testet av denna precision kom från in vivo-avbildning i möss. Genom att gradvis introducera en positivt laddad ligand, p-aminothiophenol, i det annars negativt laddade skalet skapade teamet en serie kluster vars totala ytladdning skiftade från starkt negativ till nära-zwitterjonisk (balanserade positiva och negativa grupper). Alla varianter lyste likartat i laboratorietester, men deras biodistribution i möss skiljde sig dramatiskt. Helt negativt laddade kluster ackumulerades huvudsakligen i lever och mjälte. När fler positiva ligander tillsattes minskade signalen i dessa organ och ökade i njurar och blåsa, vilket indikerar ökad renal utsöndring. När en neutral hydroxyl-ligand användes istället för aminen uppstod inte denna förskjutning, vilket understryker den speciella rollen positiva laddningar spelar för att omdirigera partiklarna.
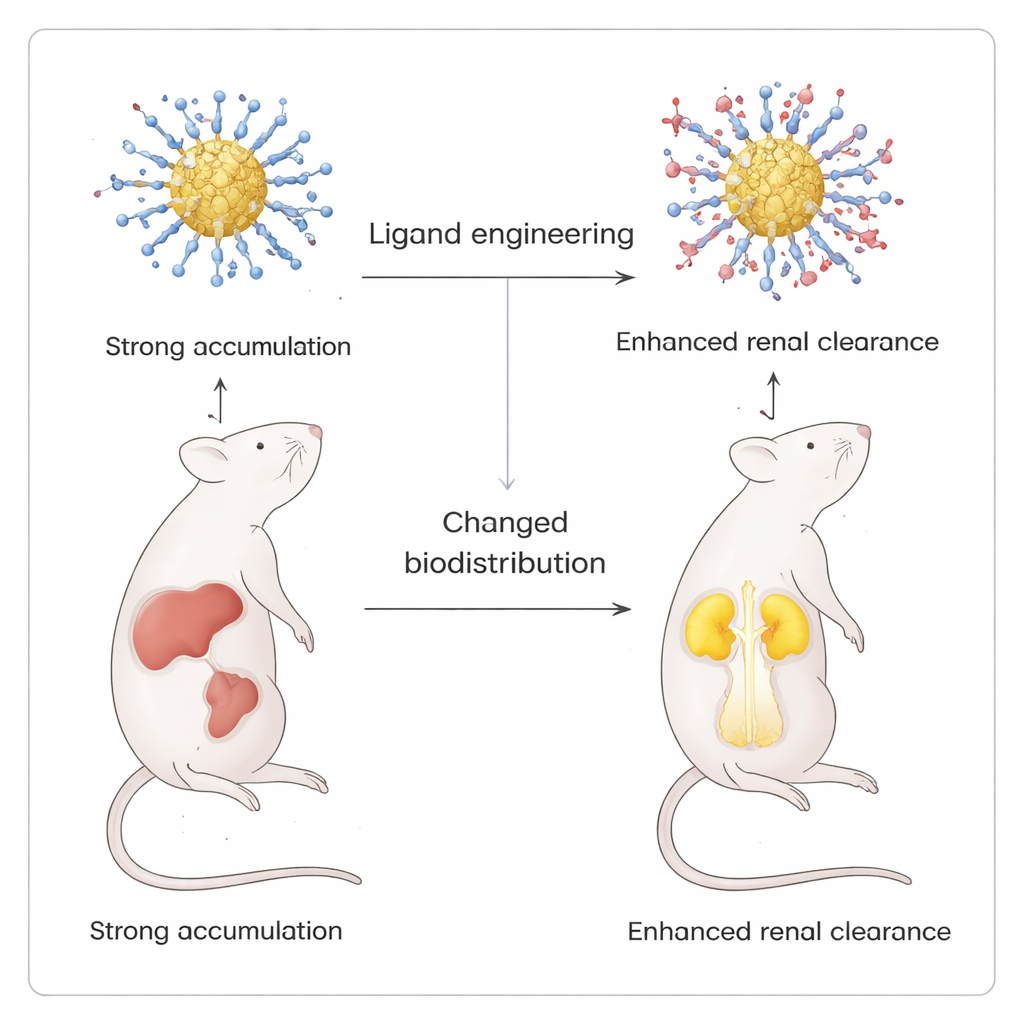
Vad detta betyder för framtida mediciner
För icke-specialister är huvudpoängen att forskare har hittat ett sätt att ”klä” lysande guldnanokluster med molekylära rockar som kan finjusteras nästan en molekyl åt gången, utan att skada partikeln under. Genom att använda en skonsam tvåvätskeskonstruktion kan de kontrollera både kemin och partiklarnas slutliga öde i kroppen. Denna nivå av kontroll gör det möjligt att designa kontrastmedel och potentiella läkemedelsbärare som belyser specifika organ och sedan lämnar via njurarna istället för att dröja kvar i lever och mjälte, vilket banar väg för säkrare och mer förutsägbar nanomedicin.
Citering: Zhang, B., Xiao, F., Song, X. et al. Atomically precise ligand engineering of gold nanoparticles via interphase mass transfer. Nat Commun 17, 1630 (2026). https://doi.org/10.1038/s41467-026-68345-z
Nyckelord: guldnanokluster, ligandteknik, bioavbildning, nanomedicin, biodistribution