Clear Sky Science · sv
Korsartsbevis för en utvecklingsmässig bakgrund till vuxen hypersomni med förlust av synaptiska adhesionsmolekyler beat-Ia/CADM2
Varför för mycket sömn kan vara ett allvarligt problem
Många avundas dem som sover tungt, men för personer med idiopatisk hypersomni kan överväldigande sömnighet förstöra arbete, skolgång och relationer. Tillståndet lämnar människor utmattade trots en hel natts sömn, och läkare förstår fortfarande inte fullt ut varför. Denna studie kombinerar mänsklig genetik med experiment i fruktflugor och zebrafiskar för att spåra överdriven sömnighet tillbaka till hur hjärnans kretsar kopplas under utvecklingen, vilket pekar på en möjlig ny behandlingsstrategi.
Att hitta sömnighetsgener i mänskligt DNA
Forskarlaget började med att gräva i stora genetiska studier av hundratusentals människor som rapporterat överdriven sömnighet på dagtid eller frekvent tupplurande. Istället för att anta att den närmaste genen till varje riskvariant var viktig, tittade de över större 3D-nabb i genomet som kallas ”topologiska domäner” för att samla alla rimliga kandidatgener. De använde sedan datorverktyg för att hitta motsvarande gener i fruktflugor och slutade upp med mer än 200 fluggener att testa. Genom att systematiskt dämpa dessa gener i alla neuroner letade de efter flugor som sov betydligt mer än normalt. Bland de starkaste träffarna fanns gener från “beaten path”-familjen, motsvarigheter till den mänskliga genen CADM2, som kodar för en molekyl som hjälper nervceller att fästa och koppla vid synapser. 
Sömniga flugor och sömniga fiskar
När flugans version av CADM2, kallad beat-Ia, minskades i neuroner sov flugorna mycket längre både dag och natt. De var inte slöa när de var vakna; istället var deras sömnperioder längre, de var svårare att väcka och föll snabbare tillbaka i sömn efter att ljuset kommit på—egenskaper som nära speglar mänsklig hypersomni. Teamet testade vidare CADM2 i zebrafiskar, en liten ryggradsdjur vars sömn kan spåras med video. Att störa fiskgenen cadm2b gjorde att fiskarna sov mer utan att minska sin rörelse när de var vakna, vilket stöder en bevarad roll för denna molekyl i att hålla djur tillräckligt alerta.
Hur tidig hjärnkoppling formar livslång sömn
En viktig insikt var att beat-Ia spelar störst roll under hjärnans utveckling, inte i vuxen ålder. Genom att slå på gen-dämpningen endast före eller endast efter att flugorna lämnat puppstadiet visade forskarna att störning av beat-Ia tidigt i livet var tillräckligt för att orsaka livslång överdriven sömnighet, medan dämpning endast i vuxna hade liten effekt. De spårade beat-Ia:s verkan till en liten uppsättning neuroner som tillverkar neuropeptid F (NPF), flugans motsvarighet till ryggsträngsdjurs neuropeptid Y (NPY). I normala flugor skickar NPF-neuroner täta synaptiska projektioner till en hjärnregion kallad suboesofageala zonen, där de kopplar till specifika hämmande (GABA-producerande) neuroner som hjälper till att stabilisera vakenhet. I flugor utan beat-Ia bildades inte de stora klustren av synapser i denna region, även om nervfibrerna fysiskt nådde området. Detta tyder på att felaktig synapsbildning, snarare än grov felkoppling, kan rubba balansen mot överdriven sömn.
Från felkopplade kretsar till ett läkemedelsmål
Med hjälp av en detaljerad kopplingskarta över flughjärnan identifierade teamet ett litet antal nedströmsneuroner i suboesofageala zonen som tar emot input från NPF-celler och förväntas vara GABAerga. Att tysta dessa celler ökade sömnen, medan aktivering främjade vakenhet, vilket stämmer med idén att NPF normalt håller djur vakna genom att driva ett lokalt hämmande nätverk. Forskarna frågade sedan om de kunde kompensera för förlorad CADM2-lik funktion genom att öka NPY-signalering. I cadm2b-defekta zebrafiskar återställde badning av larverna i ett läkemedel som aktiverar en NPY-receptorsubtyp (liknande flugans NPF-receptor) deras överdrivna sömn till normala nivåer, utan att starkt påverka normala fiskar. Detta resultat över arter tyder på att när synaptiska adhesionsmolekyler går fel under utvecklingen kan förstärkning av NPY-vägar i vuxen ålder hjälpa till att återställa en korrekt balans mellan sömn och vakenhet. 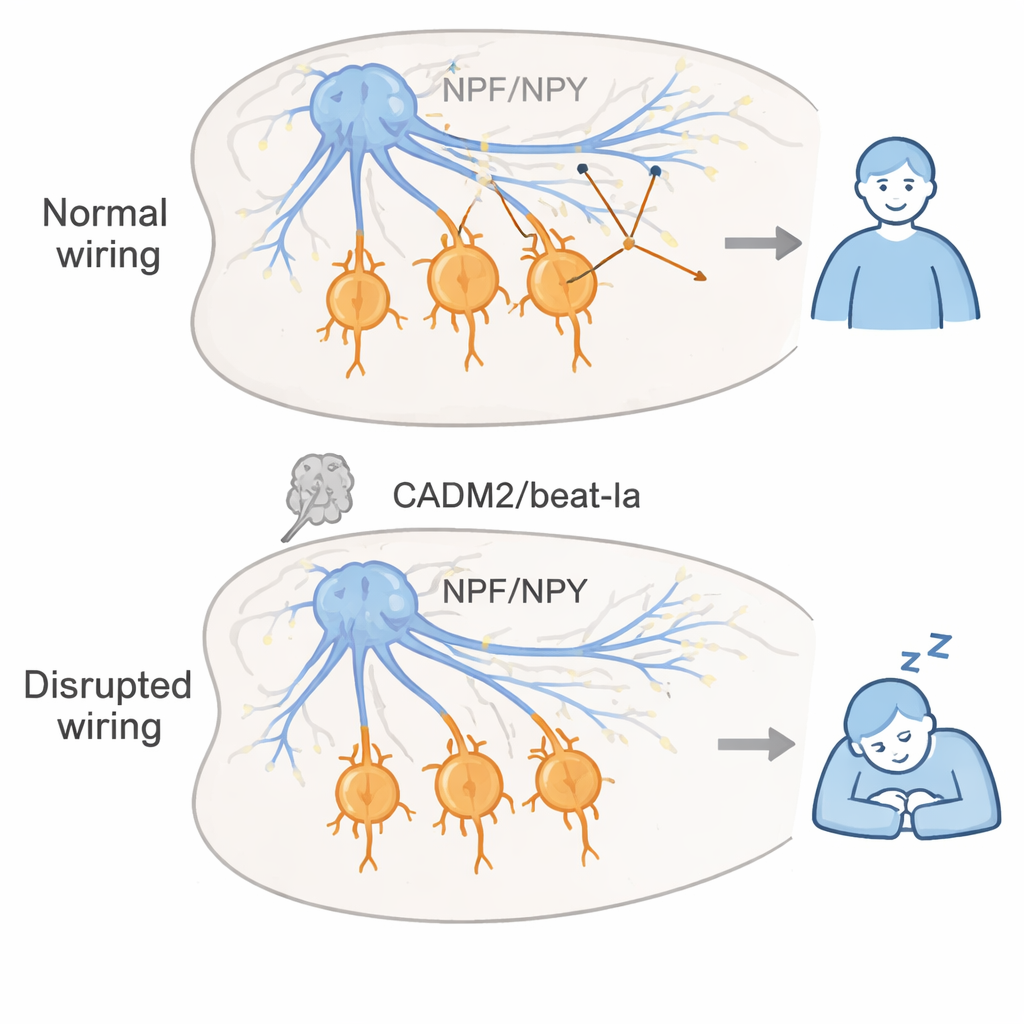
Vad detta betyder för dem som inte kan hålla sig vakna
Sammantaget föreslår arbetet att vissa former av idiopatisk hypersomni kan härröra från subtila misstag i hur vakenhetfrämjande hjärnkretsar kopplas tidigt i livet, med inblandning av CADM2 och närliggande adhesionsmolekyler. Dessa förändringar förstör inte hjärnan utan omkonfigurerar hur starkt vissa sömn- och vakenhetsbanor kommunicerar med varandra. Viktigt är att studien också visar att även om kopplingsproblemet börjar under utvecklingen kan dess effekter fortfarande vara behandlingsbara senare genom att rikta in sig på bevarade neuropeptidsystem som NPY. För patienter innebär detta möjligheten att framtida läkemedel som finjusterar dessa signalsystem kan ge mer precis lindring från försvårande sömnighet på dagtid.
Citering: Mace, K., Zimmerman, A., Chesi, A. et al. Cross-species evidence for a developmental origin of adult hypersomnia with loss of synaptic adhesion molecules beat-Ia/CADM2. Nat Commun 17, 1628 (2026). https://doi.org/10.1038/s41467-026-68343-1
Nyckelord: idiopatisk hypersomni, sömn genetiska, synaptisk adhesion, neuropeptid Y, hjärnans utveckling