Clear Sky Science · sv
Beräkningsbaserad design av generalistiska cyklopropanaser med stereodivergent selektivitet
Varför små tre‑ringade strukturer spelar roll för läkemedel
Cyklopropaner — tre‑ledade kolringar — är små, spända byggstenar som kraftigt kan förändra hur ett läkemedel beter sig i kroppen. Den exakta tredimensionella arrangemanget av atomerna (dess stereokemi) kan avgöra om en molekyl blir ett användbart läkemedel eller en inaktiv eller till och med skadlig look‑alike. Denna artikel beskriver en beräkningsstrategi för att designa enzymer som pålitligt kan framställa alla fyra möjliga 3D‑former av dessa ringar från samma utgångsmaterial, vilket öppnar för snabbare och renare utforskning av läkemedelskandidater.
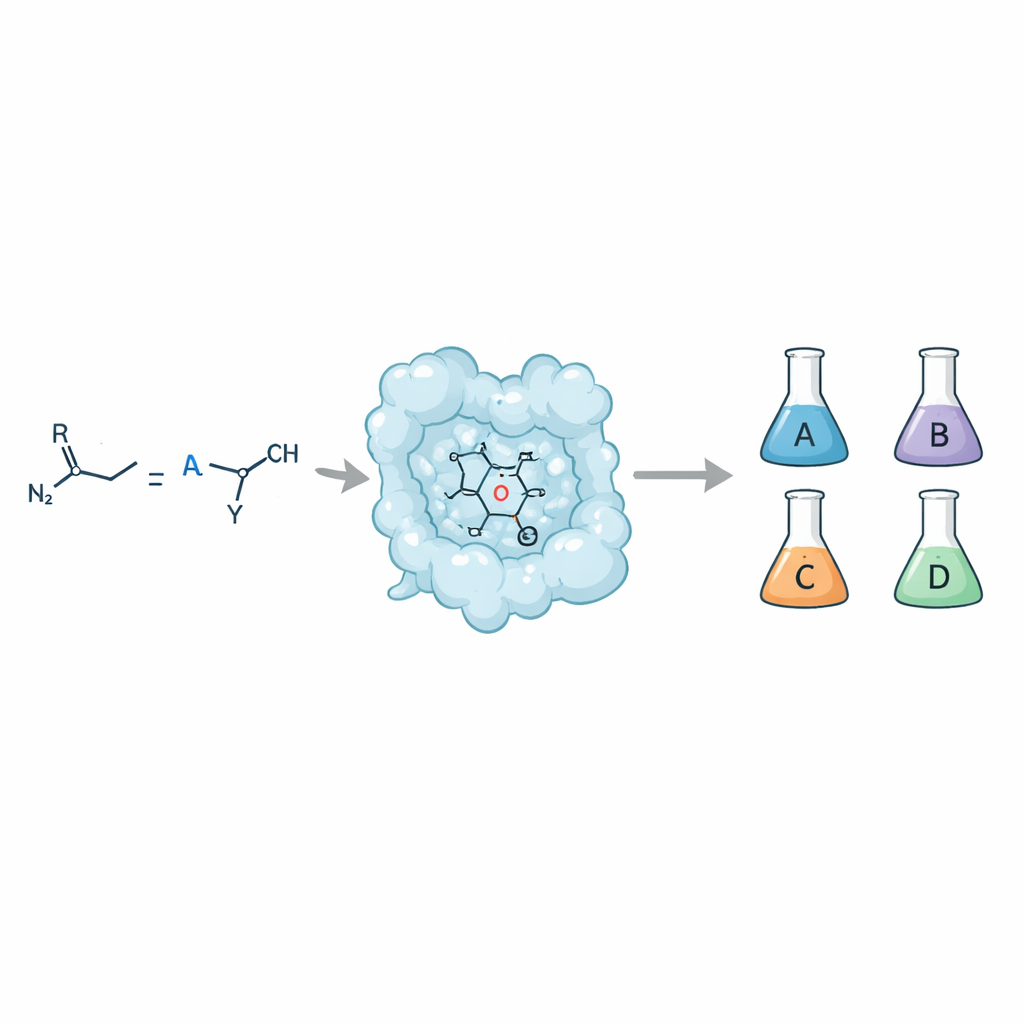
Från ett recept till fyra olika utfall
När en enkel dubbelbindning (en olefin) reagerar med en karbendonator som en diazoförening kan resultatet bli en cyklopropanring. Men den ringen kan anta fyra distinkta stereoisomeriska former, alla med samma atomer men ordnade olika i rummet. Kemiintresserade vill ha tillgång till var och en av dessa former eftersom de kan interagera mycket olika med biologiska måltavlor och påverka viktiga läkemedelsegenskaper som absorption, metabolism och säkerhet. Traditionella småmolekylära katalysatorer kan ibland ge denna kontroll, men att uppnå samma sak med enzymer — naturens egna katalysatorer — har varit svårt, särskilt när målet är både hög selektivitet och tolerans mot många olika substrat.
Designa enzymer på datorskärmen
Författarna utvecklade ett mekanismbaserat, flerstatsigt beräkningsarbetsflöde för att lösa detta problem. De använde först kvantkemiska beräkningar för att modellera de kortlivade övergångstillstånden — de högenergiska strukturerna längs reaktionsvägen — för bildandet av var och en av de fyra cyklopropan‑stereoisomererna. Dessa modeller placerades sedan i de aktiva sätena hos olika hem‑innehållande proteiner, och Rosetta‑programvaran för protein‑design användes för att utvärdera hur väl varje protein stabiliserade eller destabiliserade varje övergångstillstånd. Avgörande var att designpoängen belönade mutationer som både gynnade det önskade övergångstillståndet (positiv design) och missgynnade de konkurrerande (negativ design), vilket i praktiken lärde enzymet att "föredra" en 3D‑produkt framför de andra.
Bygga en komplett enzymverktygslåda
Med denna metod skapade teamet en familj av "generalistiska" cyklopropanaser. Med utgångspunkt i myoglobin redesignade de dess aktiva säte för att få varianter som producerar trans‑(1R,2R)‑cyklopropanen med mycket hög selektivitet och god aktivitet för mer än 20 olika olefiner, inklusive krävande oaktiverade och elektronfattiga substrat. Ett tidigare designat myoglobin stod redan för den kompletterande trans‑(1S,2S)‑produkten. För att nå de två cis‑produkterna vände sig författarna till andra hemproteiner. De omformade den bakteriellazyt P450cam för att få varianter som selektivt ger cis‑(1S,2R)‑produkten, och de omdirigerade det humana indolamin‑2,3‑dioxygenas‑1 (IDO1) — tidigare inte använt för karbenkemi — för att favorisera cis‑(1R,2S)‑produkten. Tillsammans kan dessa fyra biokatalysatorer leverera varje stereoisomer av samma cyklopropanproduktserie, ofta med upp till 99 % kontroll av både diastereomer och enantiomer.
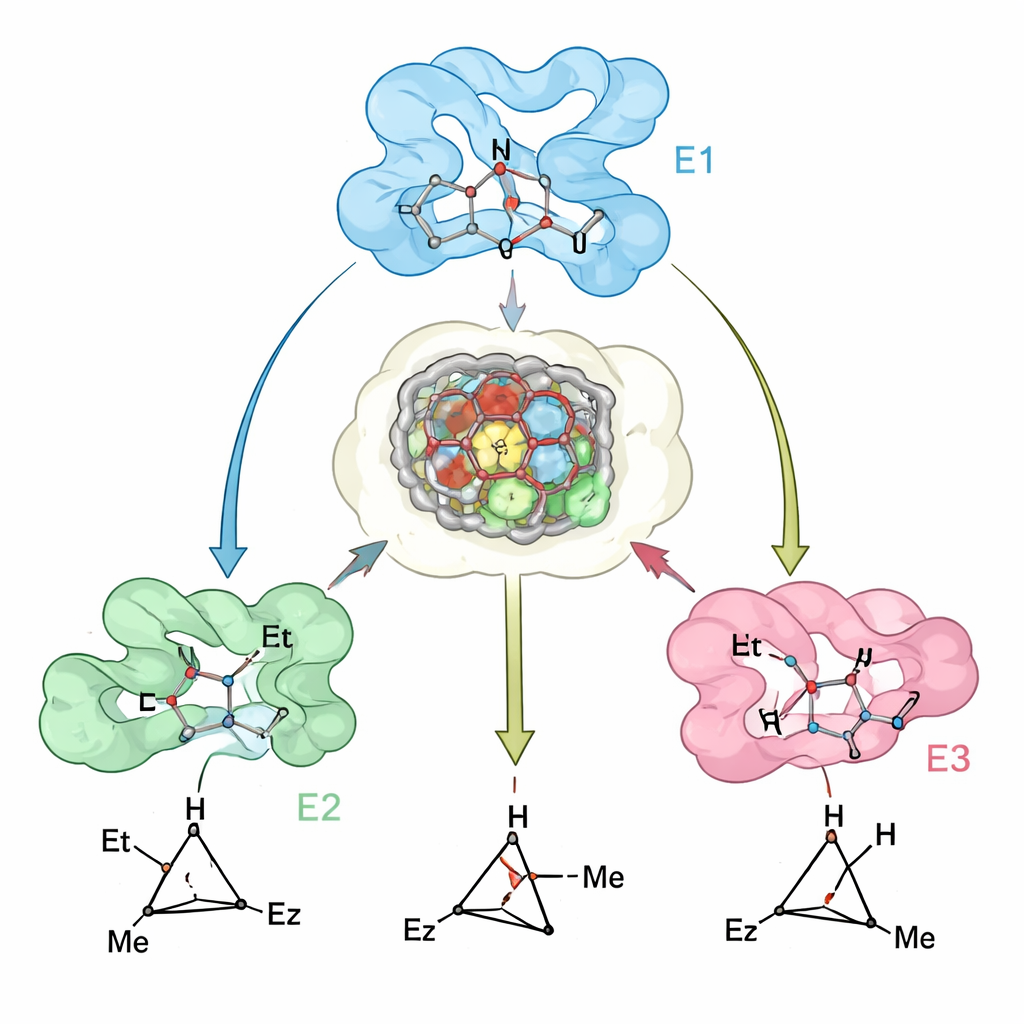
Se hur design stämmer med verkligheten
För att testa hur väl deras beräkningsmodeller speglade verkliga enzymer löste forskarna kristallstrukturer av en nyckelvariant av myoglobin och jämförde dem med de förutsagda strukturerna. Överensstämmelsen var nära, och de experimentella uppgifterna framhävde en subtil men viktig egenskap: det proteinaktiva sätet är förorganiserat för att ta emot det föredragna övergångstillståndet, medan små förskjutningar i närliggande slingor och helixar gör bindning av det "felaktiga" övergångstillståndet energimässigt oförmånligt. Där förutsägelserna var mindre exakta — till exempel för några stora substrat — kunde avvikelserna spåras till ryggradens rörelser som inte fångades fullt ut i modelleringen, vilket pekar på tydliga vägar för att förbättra framtida designmetoder.
Vad detta betyder för framtida läkemedel och katalysatorer
Genom att kombinera fysikbaserad övergångstillståndsmodellering med smart proteomdesign visar detta arbete att stereokemiska utfall av enzymkatalyserade reaktioner kan programmeras i förväg, snarare än att enbart upptäckas genom trial‑and‑error‑evolution. Den resulterande uppsättningen cyklopropanaser erbjuder kemister ett praktiskt sätt att tillverka kompletta set av cyklopropanstereoisomerer från ett brett spektrum av startolefiner, vilket kraftigt förenklar struktur‑aktivitet‑studier i läkemedelsupptäckt och syntes av naturprodukter. Samma strategi bör kunna anpassas till andra enzymtyper och reaktionsklasser och på så sätt påskynda skapandet av biokatalysatorer som ger precis 3D‑kontroll över komplexa molekyler.
Citering: Shen, Z., Siriboe, M.G., Ren, X. et al. Computational design of generalist cyclopropanases with stereodivergent selectivity. Nat Commun 17, 1620 (2026). https://doi.org/10.1038/s41467-026-68327-1
Nyckelord: biokatalys, cyklopropanering, enzymdesign, stereokemi, hemproteiner