Clear Sky Science · sv
Mutant KRAS-vaccin med dubbel checkpoint-blockad vid resecerad pankreascancer: en fas I-studie
Nya förhoppningar mot en dödlig cancer
Pankreascancer är en av de mest dödliga cancerformerna, främst eftersom den sprider sig tidigt och ofta återkommer även efter operation och cytostatika. Denna studie undersöker ett nytt slags ”träningsprogram” för immunförsvaret: ett vaccin som är byggt för att känna igen vanliga mutationer i det cancerdrivande genen KRAS, i kombination med två moderna immunterapiläkemedel. För personer som redan fått sina pankreastumörer borttagna syftar denna strategi till att utplåna osynliga cancerceller innan de får fäste igen.
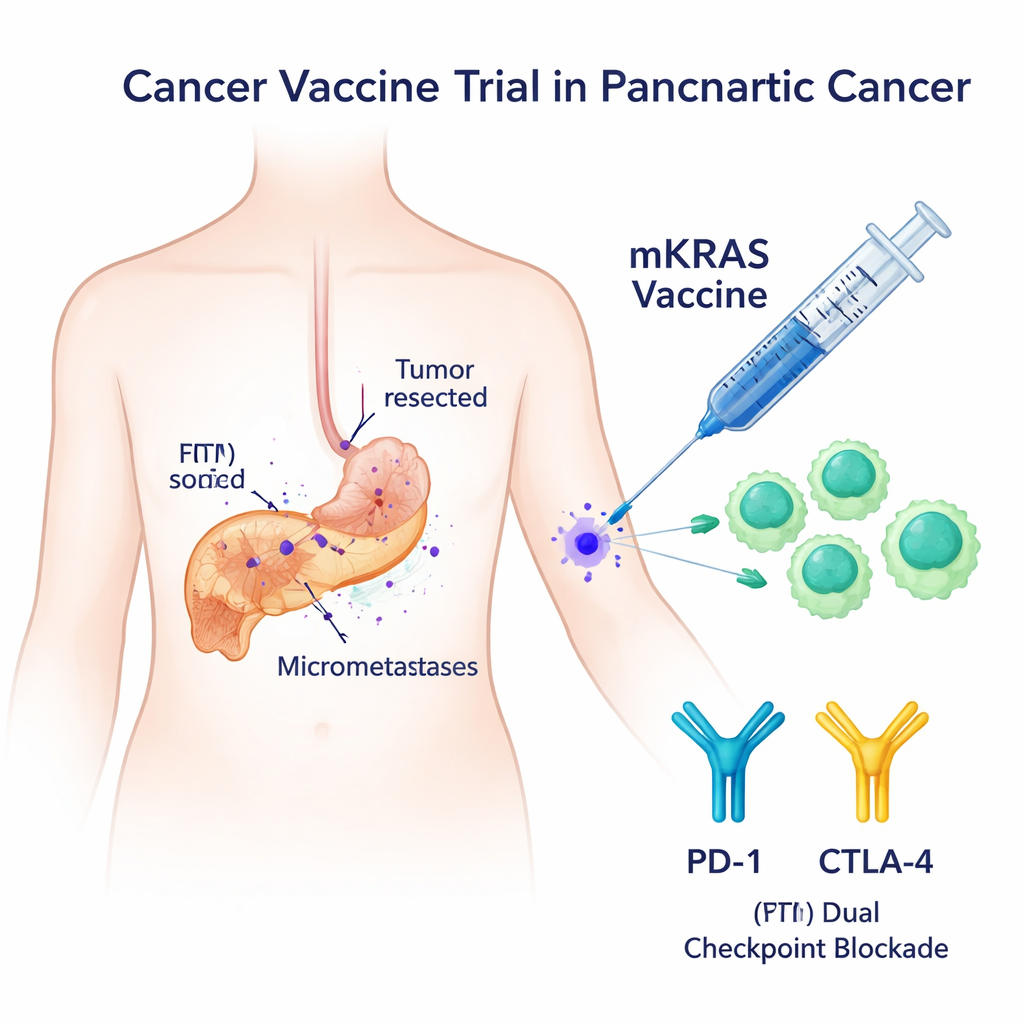
Ett skarpt mål: mutant KRAS
De flesta pankreastumörer bär förändringar i KRAS-genen som fungerar som en fastknäppt gaspedal för celltillväxt. Dessa mutanta varianter—såsom G12V, G12D, G12R, G12C, G12A och G13D—finns nästan aldrig i frisk vävnad, vilket gör dem till särskilt attraktiva mål för immunsystemet. Tidigare försök med KRAS-riktade vaccin gav endast måttliga immunsvar och fokuserade i allmänhet på en eller två mutationer. I denna fas I-studie testade forskarna ett bredare vaccin, kallat mKRAS-VAX, som kombinerar sex långa peptidfragment som representerar de vanligaste KRAS-mutationerna och parar dem med två ”checkpoint”-läkemedel, nivolumab och ipilimumab, som hjälper till att frigöra T‑celler som annars kunde hållas tillbaka.
Utformning och leverans av vaccineringsstrategin
Studien inkluderade 12 personer vars pankreastumörer hade opererats bort och som hade avslutat standardiserad cytostatikabehandling, men som fortfarande stod inför hög risk för återfall. Varje deltagares tumör bar en av de sex KRAS-mutationerna som ingick i vaccinet. Under en initial ”priming”-fas fick patienterna fyra rundor av peptidcocktailen blandad med en immunstimulerande adjuvans, tillsammans med de två checkpoint-läkemedlen. Detta följdes av booster-doser, och vissa patienter som förblev fria från cancer efter ett år fortsatte med endast vaccinboosters. De viktigaste frågorna var om denna kombination var säker och om den märkbart ökade KRAS-riktade T‑celler i blodet.
Träning och spårning av immunceller
Blodprover tagna före och efter vaccination exponerades för varje KRAS-peptid för att se hur många T‑celler som producerade interferon-gamma, en nyckelbudbärare för immunaktivitet. Resultaten var anmärkningsvärda för en liten studie: 11 av 12 patienter visade en signifikant ökning av T‑celler som kände igen de mutanta KRAS-peptiderna överlag, och 10 av 12 utvecklade ett starkt svar mot just sin tumörs specifika KRAS-mutation. Många patienter svarade mot flera av de sex KRAS-varianterna, och vissa T‑celler kunde känna igen mer än en mutation, vilket tyder på en viss användbar korsreaktivitet. Detaljerad profilering visade att de flesta av dessa vaccine‑inducerade celler var ”hjälpar”-CD4‑T‑celler med minnesdrag, understödda av en mindre men viktig grupp cytotoxiska CD8‑T‑celler med förmåga att döda. Teamet kartlade och klonade också hundratals KRAS‑specifika T‑cellsreceptorer, inklusive några ”publika” receptorer som delades mellan olika patienter, vilket kan vara värdefullt för framtida cellbaserade terapier.
Tidiga kliniska signaler och skillnader mellan mutationer
Även om studien inte var tillräckligt stor för att bevisa någon överlevnadsfördel, fanns uppmuntrande tecken. Patienter vars KRAS‑riktade T‑cellsvar rankades i de övre tre fjärdedelarna tenderade att förbli fria från påvisbar cancer längre än de med svagare svar. Efter ungefär tre års uppföljning var en tredjedel av deltagarna fortfarande fria från sjukdom. Alla fyra patienter som fortfarande var cancerfria vid senaste kontrollen bar KRAS G12V- eller G12R‑tumörer, och deras KRAS‑specifika T‑celler kvarstod i mer än ett år, särskilt minnestypen av CD4‑celler. Däremot svarade tumörer med G12D‑mutationen inte bara svagare på immunologisk nivå utan hade också högre benägenhet för återfall, vilket ekar andra studier som kopplar G12D till mer aggressiv sjukdom. Viktigt är att vaccinskyldiga biverkningar var lindriga (mest ömhet, trötthet och feber), och allvarligare immunrelaterade komplikationer berodde mer på checkpoint‑läkemedlen än på vaccinet självt.
Vad detta kan betyda för framtida patienter
Enkelt uttryckt visar denna studie att ett ”färdigt” vaccin riktat mot flera mutanta KRAS‑mål, när det kombineras med moderna checkpoint‑läkemedel, säkert kan väcka ett brett och varaktigt T‑cellsvar hos de flesta personer med högrisk pankreascancer. Även om många patienter fortfarande såg sin sjukdom återkomma, tenderade de med starkare KRAS‑fokuserade immunsvar att klara sig bättre, vilket antyder att förstärkning av dessa svar—eller att påbörja vaccinering tidigare—kan förbättra utfallet. Den rika katalogen av KRAS‑specifika T‑cellsreceptorer som upptäcktes här öppnar också dörren för konstruerade T‑cellsbehandlingar. Tillsammans tyder dessa fynd på att göra KRAS från en ökänd cancerdrivare till en igenkännbar flagga för immunsystemet kan bli en viktig strategi för att förhindra att pankreascancer återkommer.
Citering: Huff, A.L., Haldar, S.D., Gergis, A.A. et al. Mutant KRAS vaccine with dual checkpoint blockade in resected pancreatic cancer: a phase I trial. Nat Commun 17, 1538 (2026). https://doi.org/10.1038/s41467-026-68324-4
Nyckelord: vaccin mot pankreascancer, mutant KRAS, immunterapi, T-cellsrespons, checkpoint-blockad