Clear Sky Science · sv
Strukturen hos SHOC2-KRAS-PP1C-komplexet avslöjar RAS-isoformspecifika bestämningsfaktorer och insikter om att rikta in komplexets uppbyggnad med RAS-hämmare
Hur celler bestämmer när de ska växa
Våra celler förlitar sig på ett internt ledningssystem för att avgöra när de ska växa, dela sig eller förbli tysta. I centrum för detta system finns RAS-proteiner, små molekylära strömbrytare som ofta går fel vid cancer. Denna studie granskar ingående hur en särskild grupp proteiner—SHOC2, RAS och PP1C—sammansätts för att vända en viktig tillväxtbrytare, och hur moderna cancerläkemedel kan justeras för att blockera den processen mer effektivt och hindra tumörer från att kringgå behandlingen.
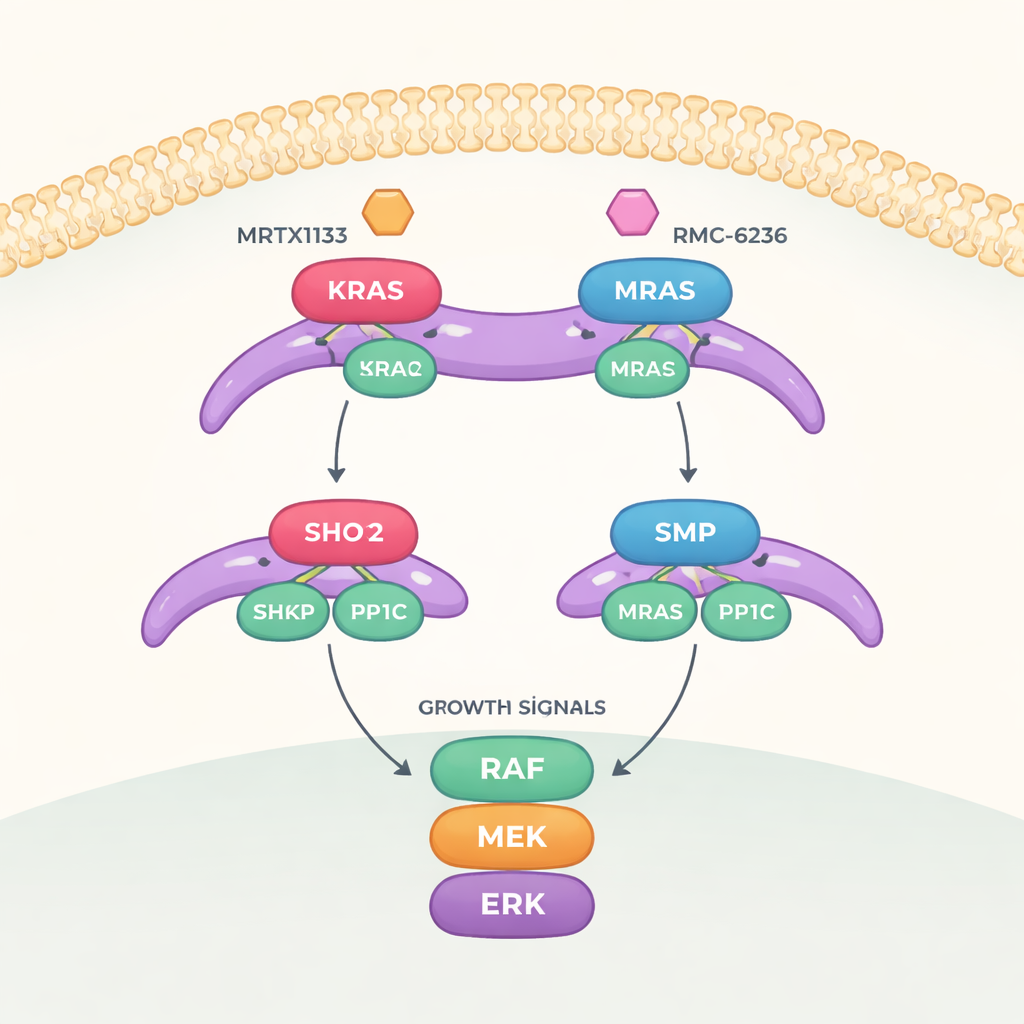
En tillväxtbrytare med tre kritiska delar
Arbetet fokuserar på en signalväg kallad MAPK-vägen, som för tillväxtsignaler från cellens yta ner till kärnan. För att slå på denna väg fullt ut måste ett annat protein som kallas RAF växlas från ett "av"-läge till ett "på"-läge. Den växeln kontrolleras av ett trekantskomplex bestående av SHOC2 (en stomme som håller ihop komponenterna), PP1C (ett enzym som avlägsnar en fosfatgrupp) och ett aktivt RAS-protein. När detta trio är sammansatt tar det bort en specifik fosfatmarkering från RAF, vilket frigör det att aktivera den nedströms liggande tillväxtkaskaden.
Varför en partner med lägre affinitet ändå är viktig vid cancer
Det finns flera typer av RAS-proteiner. MRAS bildar ett mycket stabilt komplex med SHOC2 och PP1C, medan de mer välkända cancerdrivarna KRAS, HRAS och NRAS bildar svagare varianter av samma komplex. Överraskande nog visar det sig att cancerceller drivna av muterat KRAS, HRAS eller NRAS är starkt beroende av SHOC2, trots att deras komplex är mindre stabila. Stora genetiska screeningdatamängder visar att många tumörer med vissa RAS-mutationer—särskilt de som påverkar nyckelpositioner som Q61 och G13—är mycket känsliga för att förlora SHOC2, vilket innebär att denna sammansättning är avgörande för deras överlevnad.
Avslöjandet av KRAS-komplexets form
Tidigare hade forskare endast sett en högupplöst struktur av det täta MRAS-baserade komplexet. Den svagare KRAS-versionen föll sönder för lätt för att kunna fångas. I denna studie använde författarna sjukdomsassocierade mutationer som subtilt stärker kontakter mellan komponenterna för att stabilisera SHOC2–KRAS–PP1C-komplexet tillräckligt länge för att avbildas med kryo-elektronmikroskopi. De fann att den övergripande arkitekturen i hög grad överensstämmer med MRAS-komplexet, men KRAS saknar flera små strukturella egenskaper som MRAS använder för att greppa SHOC2 och PP1C mer bestämt. Som ett resultat begraver KRAS-uppsättningen mindre kontaktarea och bildar färre bindningar, vilket förklarar varför den är inneboende mindre stabil, även om den förblir mycket viktig i tumörer där KRAS är överaktivt.
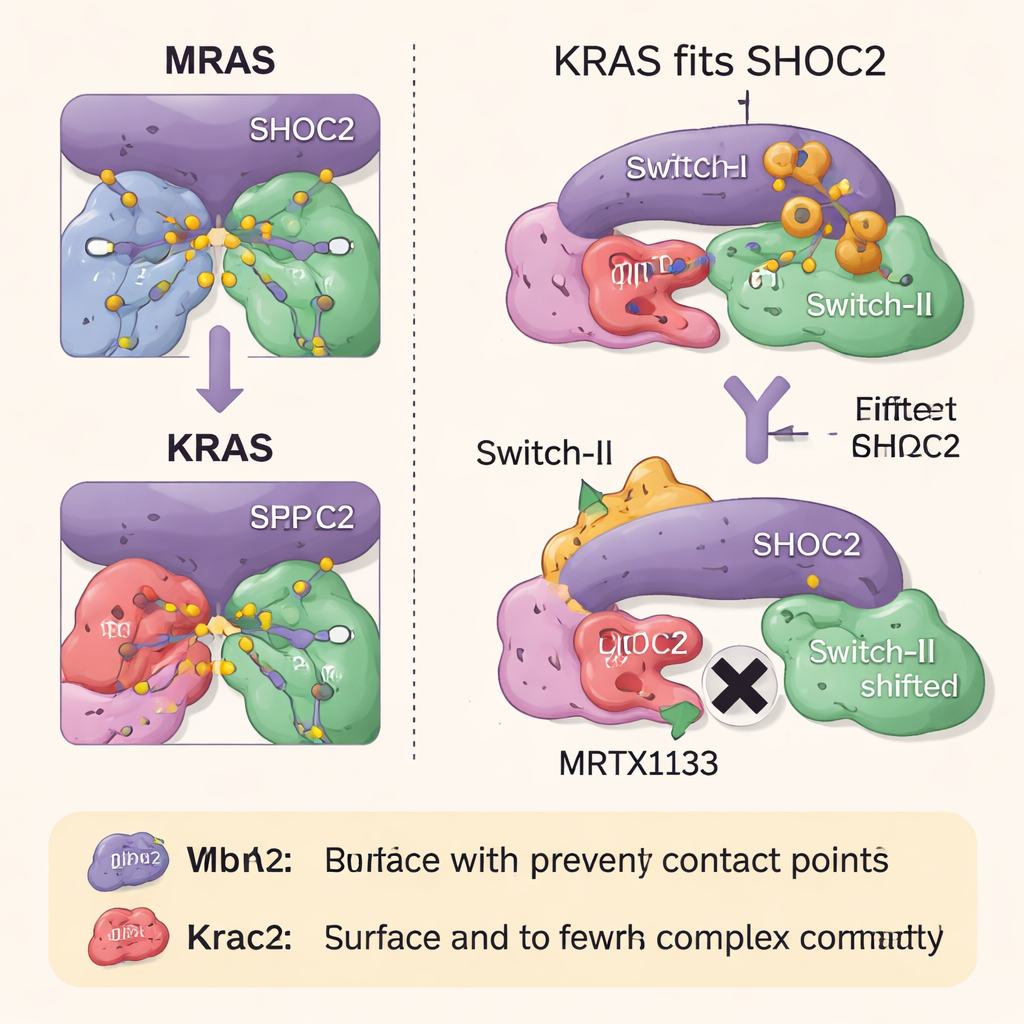
Hur RAS-läkemedel blockerar komplexbildning
Forskarna undersökte sedan hur två klasser av RAS-riktade läkemedel påverkar detta trekantskomplex. MRTX1133, utformat för att binda en ficka nära ett flexibelt område av KRAS känt som Switch-II, låser detta område i en form som krockar med SHOC2:s yta. Detta förhindrar starkt att nya SHOC2–KRAS–PP1C-komplex bildas, även om det är mindre effektivt på att bryta upp komplex som redan existerar. Ett andra läkemedel, RMC-6236, verkar tillsammans med ett hjälpprotein (cyclophilin A) och blockerar också samma KRAS-yta som krävs för SHOC2-bindning. Inget av läkemedlen binder dock naturligt MRAS, så det högaffiniteta MRAS-komplexet förblir intakt och kan hjälpa till att återaktivera tillväxtvägen när KRAS hämmas.
Mot dubbelriktade strategier för att förhindra resistens
För att testa om dubbelriktning är möjlig konstruerade forskarna en version av MRAS vars Switch-II-ficka ändrats så att MRTX1133 nu kunde binda. Denna mutant bildade fortfarande ett starkt komplex med SHOC2 och PP1C, men läkemedlet blockerade nu dess sammansättning och minskade dess förmåga att slå på RAF i provrörstester. Tillsammans med data om SHOC2-bindande föreningar visar dessa resultat att det är realistiskt att designa läkemedel som stänger ner både KRAS-baserade och MRAS-baserade komplex. För en lekmannlyssnare är huvudbudskapet att cancerceller använder flera, nära besläktade brytare för att hålla tillväxtsignalerna igång, särskilt när en brytare blockeras av läkemedel. Genom att förstå de precisa formerna och kontakterna inom dessa proteinsamlingar kan forskare nu planera terapier som träffar båda backup-vägarna samtidigt, vilket gör det svårare för RAS-drivna cancerformer att anpassa sig och utveckla resistens mot behandling.
Citering: Bonsor, D.A., Finci, L.I., Potter, J.R. et al. Structure of SHOC2-KRAS-PP1C complex reveals RAS isoform-specific determinants and insights into targeting complex assembly by RAS inhibitors. Nat Commun 17, 1614 (2026). https://doi.org/10.1038/s41467-026-68319-1
Nyckelord: RAS-signalering, KRAS-hämmare, MAPK-vägen, proteinkomplex, läkemedelsresistens