Clear Sky Science · sv
Dynamisk enkelcells‑transkriptomik avslöjar lsamp‑styrd neural nätverksbildning hos hanliga S. japonicum som driver honlig reproduktion
Varför en parasits kärleksliv spelar roll
Schistosomiasis är en parasitsjukdom som gör över 250 miljoner människor sjuka, främst i fattigare områden med begränsad sjukvård. Sjukdomen drivs inte av maskarnas bett eller toxiner, utan av de enorma mängder ägg som honor lägger inne i kroppen. Förvånansvärt nog kan honmaskar endast mogna och börja lägga ägg efter parning med en hane. Denna studie ställer en enkel men avgörande fråga: vad gör hanen exakt för att slå på honans fertilitet — och kan den strömbrytaren stängas av för att stoppa sjukdomen?
Kartläggning av en dold värld cell för cell
För att svara på detta byggde forskarna en detaljerad ”cellatlas” för blodflugan Schistosoma japonicum under det viktiga fönstret då hanar och honor parar sig och blir sexuellt mogna. Med hjälp av enkelcells‑RNA‑sekvensering, en teknik som läser vilka gener som är aktiva i enskilda celler, analyserade de mer än 100 000 celler från maskar insamlade vid fyra tidpunkter efter infektion i möss. De identifierade 76 distinkta celldyper, inklusive många slags nervceller, stamceller och reproduktionsceller. Detta gjorde det möjligt att följa hur specifika cellpopulationer växer, krymper eller ändrar identitet när maskarna utvecklas och börjar reproducera sig.
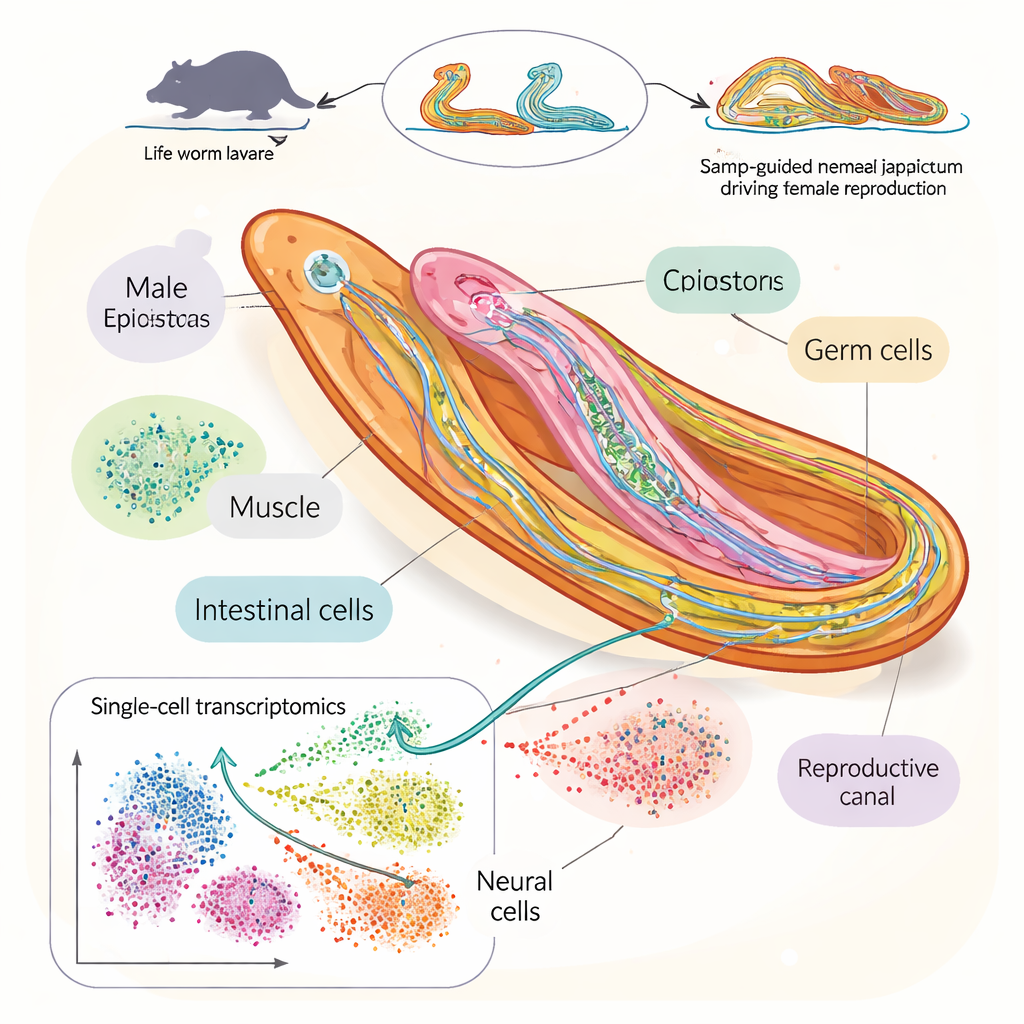
Följa ökningen av ägg och spermier
Genom att zooma in på celler från testiklar, äggstockar och närliggande vävnader rekonstruerade teamet den stegvisa utvecklingen av spermier och ägg. De visade hur germinella stamceller ger upphov till sena stadier av spermier och ägg genom skilda genaktiveringsprogram hos hanar respektive honor. Hos honor betonas gener som stöder äggtillväxt kring proteinproduktion och paketering, medan hanarnas gener fokuserar mer på strukturer som cilier och mikrotubuli som hjälper spermierna att röra sig. Studien kartlade också hur det massiva äggstödsorganet hos honor, vitellaria, utvecklas genom intermediära stadier och identifierade nya genetiska markörer som visar hur mogna respektive reproduktionsvävnad är.
En hanligbart nervkrets i ett omfamningskanal
En av de mest slående upptäckterna kom från nervsystemet. Istället för en lös samling nervceller visade atlasen fem tydliga neuronala linjer, inklusive flera som skiljde sig mellan hanar och honor. Tre neurontyper — benämnda N2.2, N3.2 och N4.3 — var starkt berikade hos hanar och klustrade inne i gynekophoralkanalen, en specialiserad fåra som hanen använder för att hålla honan. Bland dessa stack N4.3‑neuronerna ut eftersom de uttryckte en gen kallad nrps, som kodar för enzymet som producerar BATT, en liten peptidferomon som tidigare visats stimulera honlig sexuell utveckling. Med andra ord är dessa N4.3‑celler hanens ”signalsationer” för att slå på honans fertilitet.
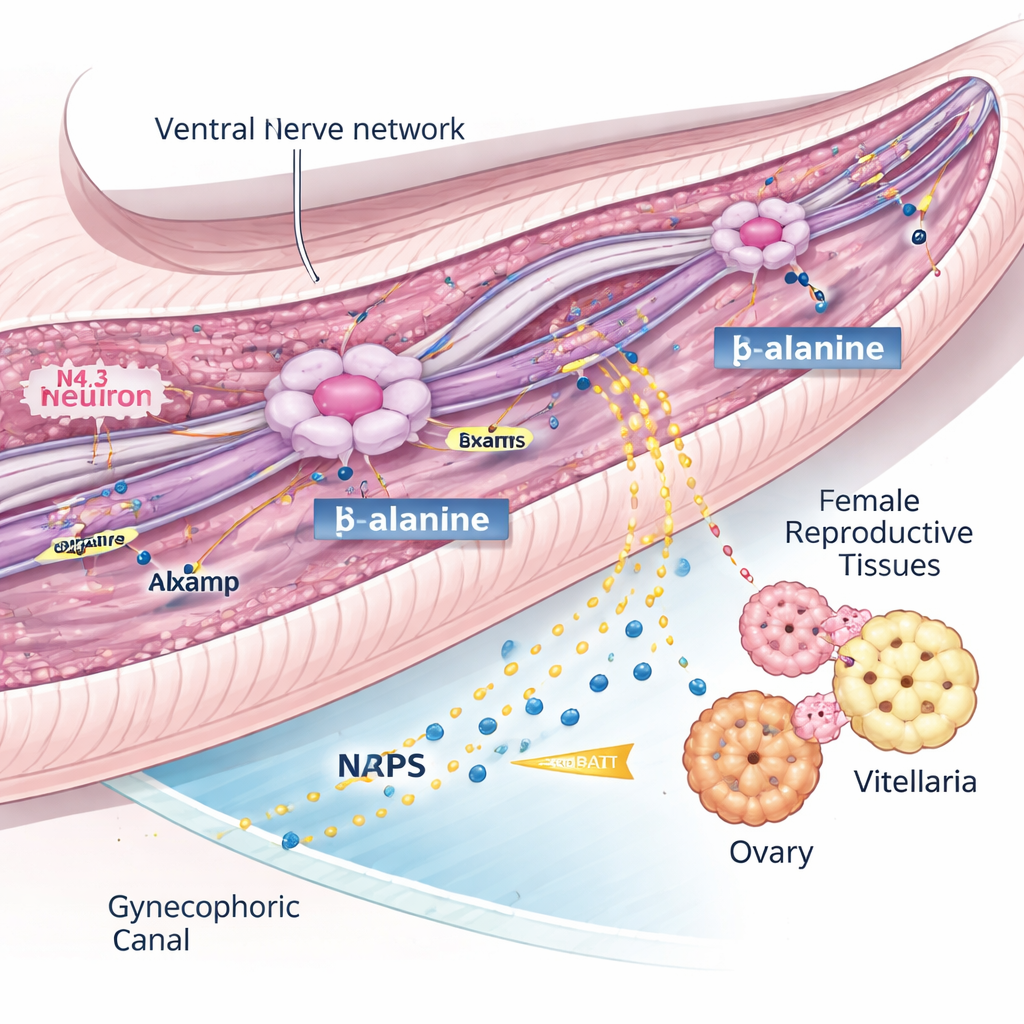
En vägledande molekyl som håller signalen igång
För att förstå hur dessa N4.3‑neuroner fungerar sökte forskarna efter gener som verkade styra deras utveckling och funktion. De fokuserade på lsamp, en gen känd i andra djur för att hjälpa nervceller att kopplas samman och upprätthålla sina axoner. I hanflukor var lsamp påslagen i samma N4.3‑neuroner som producerar BATT‑enzymet, och dess aktivitet steg kraftigt när maskarna mognade. Genom RNA‑interferens för att sänka lsamp i hanar fann teamet att parade honor inte utvecklade sina äggstockar och vitellaria fullt ut och lade nästan inga ägg. Ändå fanns N4.3‑neuronerna kvar, nrps‑genen var fortfarande aktiv och de råa kemiska ingredienserna för BATT var oförändrade. Istället visade lsamp‑defekta hanar skadade nervfibrer och störd vesikeltransport längs stabiliserade mikrotubuli, och de producerade mycket mindre BATT både inuti sina kroppar och i omgivande medium. Detta tyder på att lsamp är avgörande för att upprätthålla ett ventralt nervnätverk som levererar en viktig prekursor, sannolikt β‑alanin, till N4.3‑neuroner så att de kan syntetisera tillräckligt med feromon för att aktivera honan.
Att dämpa reproduktionsbrytaren
För icke‑specialister är huvudbudskapet att denna parasits förmåga att ge upphov till sjukdom beror på en intim dialog mellan han‑ och honmaskar, förmedlad via ett specialiserat nervnätverk och ett litet feromon. Studien visar att en enda vägledande molekyl, lsamp, hjälper till att bygga och underhålla hanens ventrala nervkopplingar; när den kopplingen sviktar kan hanen inte längre sända en tillräckligt stark kemisk signal för att helt mogna honans reproduktionsorgan, och äggproduktionen sjunker kraftigt. Genom att kartlägga parasitens celler i hög upplösning och avslöja denna han‑specifika neurala krets pekar arbetet på nya sätt att blockera äggproduktion — vilket erbjuder en möjlig strategi för att begränsa schistosomiasis där dagens behandling vilar på ett ensamt åldrande läkemedel.
Citering: You, Y., Cheng, S., Chen, X. et al. Dynamic single-cell transcriptomics reveals lsamp-guided neural network formation in male S. japonicum driving female reproduction. Nat Commun 17, 1602 (2026). https://doi.org/10.1038/s41467-026-68305-7
Nyckelord: schistosomiasis, enkelcells‑transkriptomik, parasitreproduktion, neuronala kretsar, feromon‑signalering