Clear Sky Science · sv
Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals
Hur viruset överlistar viktiga antivirala läkemedel
COVID-19-viruset tillhör en ovanlig grupp RNA-virus som kan korrekturläsa sitt genetiska material, vilket gör det ovanligt bra på att motstå vissa av våra mest effektiva antivirala läkemedel. Den här studien går på atomnivå in på hur SARS‑CoV‑2 upptäcker och tar bort en ofta använd läkemedelsklass kallad nukleotidanaloger, och förklarar varför läkemedel som fungerar väl mot andra virus ofta presterar sämre mot coronavirusinfektioner.
En dragkamp om det virala RNA:t
SARS‑CoV‑2 kopierar sitt ~30 000‑bokstäver långa RNA‑genom med en stor molekylär maskin kallad replikations–transkriptionskomplexet. I dess kärna sitter RNA‑beroende RNA‑polymeras (RdRp), som bygger nya RNA‑strängar, och en separat enhet, exonukleas (ExoN), som korrekturläser och trimmar bort fel. Många antivirala tabletter, inklusive läkemedel ursprungligen utvecklade för hepatit C, imiterar de naturliga RNA‑byggstenarna tillräckligt nära för att RdRp ska sätta in dem, men med subtila förändringar som stoppar kopieringen eller inför fel. Tyvärr har coronavirus ExoN, som kan känna igen dessa bedragare när de väl sitter i RNA‑kedjan och klippa bort dem, vilket räddar viral replikation.
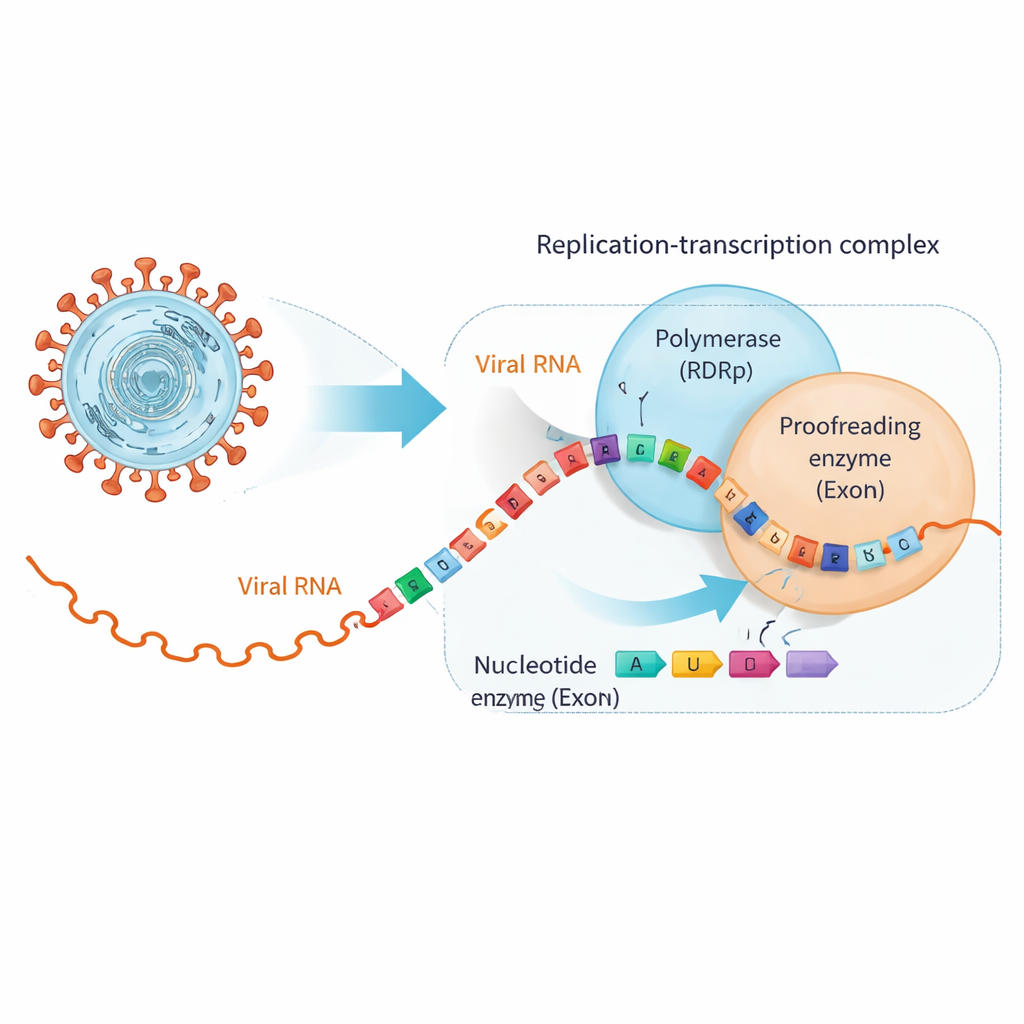
När hjälpande läkemedel får RNA att byta partner
Forskarna fokuserade på två kliniskt viktiga antivirala medel, bemnifosbuvir och sofosbuvir, båda designade för att fungera som defekta RNA‑byggstenar. De visade först att SARS‑CoV‑2:s polymeras utan problem inför dessa analoger i slutet av en RNA‑sträng och därefter i stort sett slutar förlänga kedjan, som avsett. Bindningstester avslöjade emellertid en twist: när en analog sitter i RNA:ts ände fäster RNA:t inte lika hårt vid polymeraset utan binder i stället tätare till ExoN. I praktiken knuffas det läkemedelsmodifierade RNA:t bort från kopieringsmaskinen och överlämnas till korrekturläsaren, som då får möjlighet att klippa bort den problematiska nukleotiden och låta replikationen fortsätta.
Korrekturläsning som saktas men inte stoppas
Biokemiska tidsförloppsexperiment visade att ExoN faktiskt avlägsnar bemnifosbuvir och sofosbuvir från RNA, men långsammare än när det tar bort normala nukleotider. I cellfria reaktioner blockerade båda analogerna starkt fortsatt RNA‑syntes—men när ett aktivt ExoN tillsattes räddades och förlängdes en betydande andel av de fastnade RNA‑kedjorna. En inaktiverad ExoN‑mutant kunde inte göra detta, vilket bekräftar att korrekturläsningsaktiviteten står för att åtgärda mycket av läkemedlens effekt. När polymeras fanns närvarande tillsammans med ExoN ökade borttagningen av analogerna faktiskt i hastighet, vilket tyder på att de två virala enzymerna samarbetar för att rensa hinder och hålla replikationen igång.
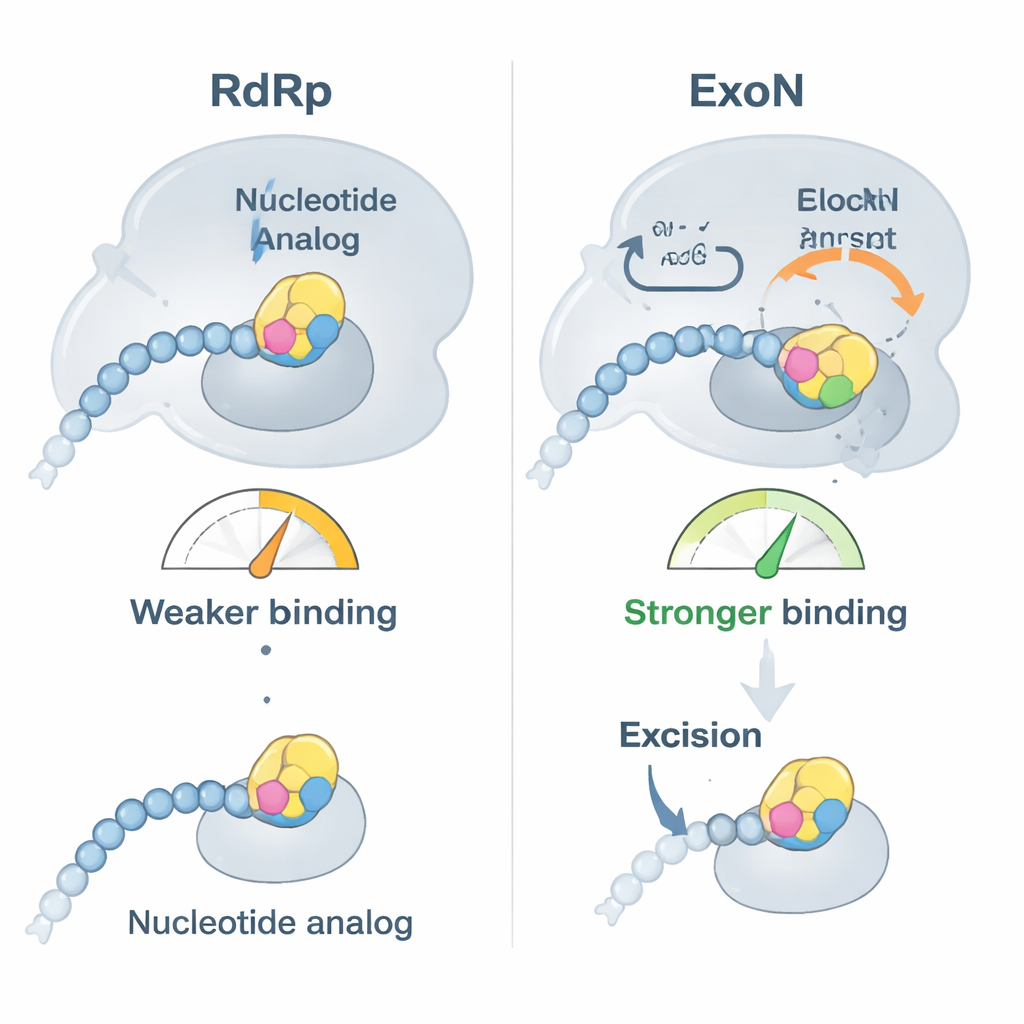
Att iaktta korrekturläsaren i atomär upplösning
För att förstå hur ExoN känner igen och reagerar på dessa läkemedel använde teamet högupplöst kryoelektronmikroskopi för att lösa strukturer av ExoN‑komplexet bundet till RNA‑strängar som slutar i antingen bemnifosbuvir eller sofosbuvir. Dessa strukturer, tillräckligt skarpa för att se individuella kemiska grupper, visade att den modifierade socker‐ringen i varje läkemedel passar in i en hydrofob ficka som bildas av en kort slinga i ExoN‑proteinet. Denna extra täta passform förklarar den starkare bindningen av läkemedelsinnehållande RNA till ExoN. Men det har också en oväntad bieffekt: genom att dra i den slingan stör läkemedlen den precisa ordningen i en närliggande katalytisk slinga som håller en nyckelhistidin på plats. När denna histidin svänger bort från klippstället blir ExoN:s aktiva centrum delvis inaktiverat, vilket saktar ner men inte helt förhindrar excision av analogen.
En inbyggd strömbrytare som ställer in viral korrekturläsning
Att mutera enskilda aminosyror inom den känsliga slingan bekräftade dess betydelse. Förändringar i fyra bevarade rester minskade kraftigt ExoN:s förmåga att klippa både standard RNA‑ändar och läkemedels‑terminerade ändar, och ändrade också vilken sista nukleotid ExoN föredrar att ta bort. Detta identifierar slingan som en allosterisk regulator—en inbyggd mekanisk strömbrytare som känner av vilken typ av nukleotid som sitter i RNA‑ändan och justerar enzymets aktivitet. Strukturerna visar vidare att ExoN känner igen olika baser (A, U, C eller G) genom flexibla vätebindningar, men har svårast att rymma guaninliknande baser, vilket är relevant eftersom bemnifosbuvir imiterar guanosin.
Vad detta betyder för framtida COVID‑19‑piller
För icke‑specialister är huvudbudskapet att SARS‑CoV‑2 bär på en sofistikerad ”stavningskontroll” som kan dra ut vissa läkemedel ur dess genom efter att de gjort sitt jobb med att stoppa replikation. Bemnifosbuvir och sofosbuvir försvagar visserligen virusets kopieringsmaskin, men samtidigt styr de RNA:t mot korrekturläsaren som delvis kan upphäva deras effekter. Genom att visa exakt hur den virala korrekturläsaren greppar dessa läkemedel, och hur en liten regulatorisk slinga växlar enzymet mellan aktiva och mindre aktiva tillstånd, erbjuder detta arbete en karta för att designa nya antivirala nukleotider som antingen binder dåligt till ExoN, låser det i en inaktiv konformation eller utnyttjar dess svårigheter med guaninliknande strukturer. Sådana nästa generations molekyler skulle kunna vara mycket svårare för viruset att ”radera”, vilket förbättrar vår förmåga att behandla COVID‑19 och framtida coronavirusutbrott.
Citering: Liu, C., Li, Y., Cao, X. et al. Mechanism of SARS-CoV-2 resistance to nucleotide analog-based antivirals. Nat Commun 17, 1601 (2026). https://doi.org/10.1038/s41467-026-68304-8
Nyckelord: SARS-CoV-2, antiviral resistance, nucleotide analogs, RNA proofreading, coronavirus replication