Clear Sky Science · sv
Lewis-syra-utlöst hydroxylspillover möjliggör selektiv elektrooxidation av urea till nitrit med samtidig energibesparande väteproduktion
Att omvandla avfall till användbara kemikalier och ren bränsle
Urea är mest känt som en beståndsdel i urin och gödselmedel, men i avloppsvatten blir det en motsträvig förorening. Den här studien visar hur urea kan förvandlas från en belastning till en resurs: med en genomtänkt katalysatordesign omvandlar författarna urea till nitrit, en värdefull kemikalie för gödsel och läkemedel, samtidigt som de producerar vätgas med mindre elförbrukning än vid konventionell vattenspaltning. Arbetet visar en möjlig framtid för reningsverk som rengör vatten, framställer användbara produkter och genererar ren energi på samma gång.
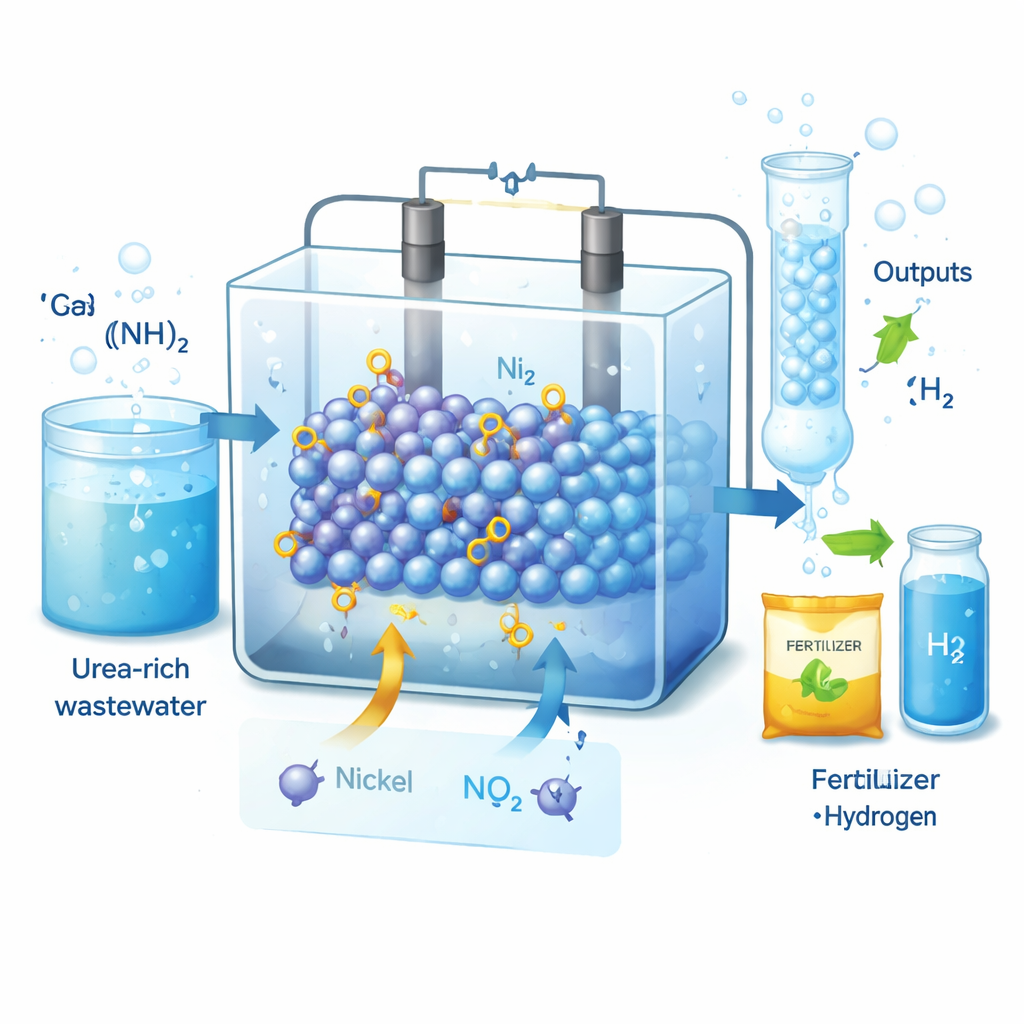
Varför nitrit och väte är viktiga
Nitrit är en viktig ingrediens inom jordbruk, livsmedelskonservering och läkemedel, och den globala efterfrågan mäts i miljoner ton per år. Idag framställs det mesta nitriten via Ostwald-processen, som körs vid hög temperatur, förbrukar stora mängder energi och släpper ut förorenande kväveoxider. Samtidigt innehåller avloppsvatten från hushåll och industri stora mängder urea, som står för 70–80 % av kväveföroreningarna. Om den urean kunde uppgraderas elektrolytiskt till nitrit samtidigt som vätgas genereras, skulle vi kunna både rena vatten och leverera två högvärdiga produkter—förutsatt att processen är tillräckligt effektiv och selektiv.
Styra reaktionerna längs rätt bana
När urea oxideras i alkalisk lösning kan den följa två huvudsakliga vägar. Den ena leder till ofarligt kvävgas och koldioxid; den andra, mer önskvärda vägen leder till nitrit och nitrat, som är marknadsbara kemikalier. Problemet är att de flesta nickelbaserade katalysatorer, som är arbetshästarna i denna reaktion, inte är särskilt kräsna—de tenderar att ge en blandning av produkter och slösar också energi på att driva syrgasutvecklingsreaktionen (OER), som bildar syrgas men ingen intäkt. Författarna gav sig därför i kast med att omforma katalysatorytan så att hydroxidjoner, den reaktiva OH⁻-arten i alkalisk media, koncentreras och styrs på ett sätt som gynnar brytning av kol–kväve-bindningar och bildning av nitrit snarare än att låta kväveatomer paras ihop till N₂.
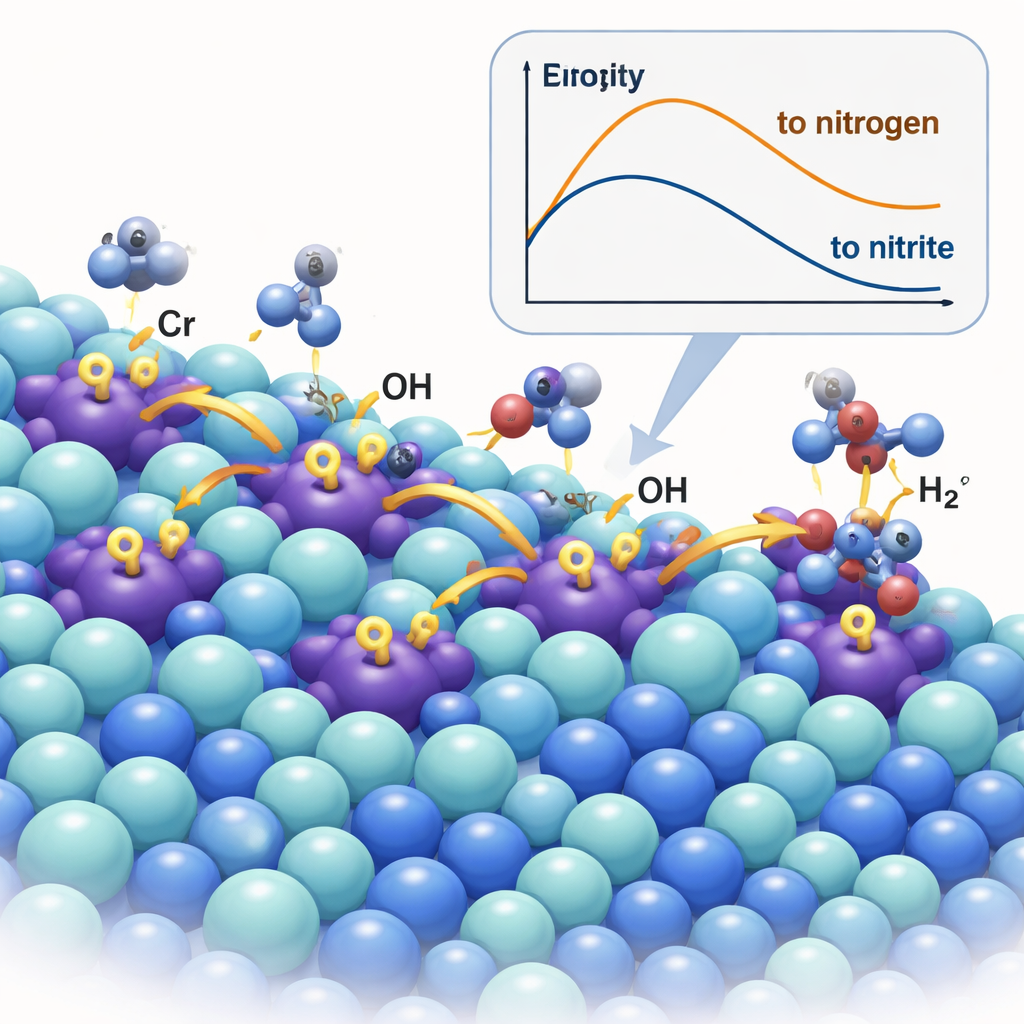
En katalysator som pumpar reaktiva arter
Teamet skapade ett nytt material genom att doppa nickelsulfid (Ni₃S₂) med en liten mängd krom och bilda Cr–Ni₃S₂. Kromjoner fungerar som så kallade Lewis-syraplatser—elektronfattiga centra som starkt attraherar hydroxidjoner. Med hjälp av avancerad mikroskopi, röntgentekniker och spektroskopi bekräftade forskarna att kromatomerna sitter i nickelsulfidens kristallgitter och subtilt krymper och förvränger det, vilket förändrar hur elektroner fördelas. Under reaktionsförhållanden agerar kromplatserna som små pumpar: de fångar upp OH⁻ och "spillover" överför det till närliggande nickelplatser, där den faktiska ureaoxidationen sker. In situ Raman- och infraröda mätningar, liksom isotopmarkeringsexperiment, följde direkt detta spillover av hydroxid från Cr till Ni och visade att det påskyndar bildandet av aktiva nickeloxyhydroxid (NiOOH)-platser som driver den önskade kemin.
Höga utbyten, lägre energi och god stabilitet
Eftersom OH⁻ levereras effektivt till rätt platser omvandlar Cr–Ni₃S₂-katalysatorn urea till nitrit med imponerande selektivitet. Vid industriellt relevanta strömtätheter uppnår den en nitritproduktion på cirka 121 milligram per timme per kvadratcentimeter med faradaisk effektivitet för nitrit över 80 %, samtidigt som konkurrerande syrgasutveckling hålls under 1,5 %. Katalysatorn förblir stabil under hundratals timmars kontinuerlig drift med försumbar kromutlakning. Samma material sänker också dramatiskt den spänning som behövs när det paras med en väteutvecklande katod i en ureaassisterad vattenspaltare, vilket minskar elkostnaden för vätgasproduktion till ungefär 3,7 kilowattimmar per kubikmeter H₂—mindre än konventionell alkalisk elektrolys. En teknisk-ekonomisk analys antyder att vid 400 milliampere per kvadratcentimeter kan behandling av ett ton urea i detta system ge ett nettovärde på ungefär 1 200 dollar när både nitrit och väte räknas in.
Från laboratoriecell till praktiska energienheter
För att demonstrera verklig potential byggde författarna en flowcell för kontinuerlig ureaassisterad vattenspaltning och ett Zn–urea–luftbatteri. I batteriet minskade ersättningen av den vanliga syrgasutvecklingsreaktionen under laddning med ureaoxidationen laddningsspänningen med nästan 0,3 volt samtidigt som stabil prestanda bibehölls i mer än 100 timmar. Det innebär att enheten både kan rena ureahaltiga strömmar och fungera som energilagring med högre energieffektivitet. Samma Lewis-syradesign fungerade också när andra metaller som tenn och titan eller en annan värd som kopparsulfid användes, vilket tyder på att tillvägagångssättet är brett gångbart.
En enkel idé bakom en komplex reaktion
För icke-experter är huvudidén att forskarna har lärt sig hur man styr var och hur en vanlig reaktiv ingrediens—hydroxid—landar och rör sig på en katalysatoryta. Genom att tillsätta kromplatser som fungerar som starka attraherare och mellanhänder för OH⁻ gör de det lättare för ureamolekyler att klyvas till nitrit istället för att fullständigt oxideras till kvävgas. Samtidigt kräver denna väg mindre elektrisk energi och producerar naturligt vätgas. I huvudsak visar arbetet att noggrann atomskalig utformning av katalysators "trafikmönster" kan göra avloppsvatten till en källa för både kemikalier och ren energi.
Citering: Fan, C., Zhang, M., Li, Y. et al. Lewis acid-triggered hydroxyl spillover enables selective urea electrooxidation to nitrite with concurrent energy-saving hydrogen production. Nat Commun 17, 1585 (2026). https://doi.org/10.1038/s41467-026-68302-w
Nyckelord: ureaoxidation, nitritproduktion, vätegenerering, elektrokatalys, avloppsvattenvärdering