Clear Sky Science · sv
Integrerad multi-omisk atlas avslöjar hierarkin i de rumsligt- tidsmässiga regleringsnäten under musgastrulation
Hur ett embryo bygger sin kroppslayout
Varje däggdjur, inklusive människor, börjar livet som en liten cellkula som snabbt måste organisera sig till en komplex kropp med huvud, svans, rygg, buk och inre organ. Denna dramatiska omformning sker under ett kort fönster kallat gastrulation. Den här artikeln sammanfattar ett detaljerat, flerskiktat kartläggningsarbete av processen i musembryon och visar hur gener, DNA-regulatorer och kemiska signaler samverkar i rum och tid för att styra celler mot sina framtida öden.
Att följa tusentals cellers val
För att observera gastrulation i handling analyserade forskarna mer än 35 000 enskilda celler från musembryon över fem tätt liggande stadier, från tidig till sen gastrulation. För varje cell mätte de inte bara vilka gener som var aktiva, utan också vilka DNA-regioner som var öppna och tillgängliga—ett tecken på att de kan fungera som regulatoriska brytare. Med dessa data identifierade de 31 distinkta celltyper och följde hur tidiga, flexibla celler gradvis förgrenar sig till de tre huvudsakliga groddlagren—ektoderm, mesoderm och endoderm—som så småningom bildar alla vävnader och organ. De utvecklade också en ny beräkningsmetod, BioCRE, för att mer precist koppla gener till deras styrande DNA-element, vilket visade att många viktiga brytare ligger långt från de gener de reglerar.
Bygga en 3D-molekylär atlas i verkligt embryonalt rum
De flesta single-cell-metoder förlorar den ursprungliga positionen för varje cell i embryot, men läget är avgörande för att förstå mönsterbildning. Teamet övervann detta genom att slå samman sina single-cell-data med en befintlig tredimensionell karta över genaktivitet i musembryon. Resultatet är ST-MAGIC, ett ”digitalt embryo” där varje liten plats annoteras med troliga celltyper, generna de uttrycker och tillgängligheten hos omgivande DNA. Denna atlas visar till exempel hur olika mesoderm-subtyper—framtida hjärta, muskel och stödjande vävnader—uppstår i skilda regioner och hur brett uttryckta gener som Otx2 använder olika regulatoriska element på embryots yttre (epiblast) och inre (visceral endoderm) ytor.
När symmetrin bryts och vänster blir olikt höger
En iögonfallande egenskap i kroppsplan är att vänster och höger sida inte är identiska—tänk på hur hjärtat ligger något åt vänster. Författarna använde sin spatiala atlas för att zooma in på lateral mesoderm, där vänster–höger- skillnader först framträder. De fann subtila men konsekventa asymmetrier i vilka celltyper som är förhöjda på varje sida och i vilka DNA-regioner som är mer öppna. På höger sida var regioner kopplade till en tillväxtsignalväg kallad BMP mer tillgängliga; på vänster sida gynnades regioner associerade med gener som behövs för segmentbildning och hjärtstrukturer. Några av dessa DNA-element, inklusive nyligen upptäckta sådana som reglerar genen Lefty2, blir öppna innan synliga genuttrycksskillnader uppstår, vilket tyder på att tidig ”priming” av kromatinlandskapet förbereder varje sida av embryot att tolka signaler olika.
En stafett av faktorer vägleder kroppens mittlinje
Studien fokuserar sedan på axial mesendoderm, en cellpopulation som kommer att bilda notokorden—en stavliknande struktur längs mittlinjen som hjälper till att organisera ryggraden och nervsystemet. Med sina kombinerade verktyg (ST-MAGIC och en utökad version kallad ST-MAGIC (+)) följde författarna hur dessa celler uppstår från den anteriora primitiva strimman och delar sig i två grenar: nodceller, som bygger en cilierad struktur viktig för vänster–höger-sinne, och anterior mesendoderm, som bidrar till mittlinjevävnader. De avslöjade en hierarkisk stafett av transkriptionsfaktorer—proteiner som styr genaktivitet. Tidiga faktorer, såsom EOMES, och intermediära faktorer, inklusive FOXA2 och LHX1, öppnar först nyckelregioner i DNA och etablerar responsivitet inför stora signaler som WNT och NODAL. Senare, ”terminala” faktorer såsom NOTO, SOX9 och en nyligen implicerad faktor POU6F1 slår på specialiserade genprogram, till exempel de som behövs för cilier eller extracellulär matrix.
Signaler, kromatin och sent verkande specialister
Genom att integrera offentliga dataset om var WNT- och NODAL-signalernas effektorfaktorer binder DNA visade författarna att embryots responsivitet på dessa signaler skiftar i rummet innan signalernas källor själva förflyttas. I regionen som är förberedd att bli axial mesendoderm öppnas DNA-ställen som svarar på NODAL och WNT tidigt, och många bär motiv för FOXA2, Zfp281 och andra regulatorer, vilket antyder samverkande kontroll. Experimentell deletion av sena faktorer NOTO och POU6F1 i möss störde uttrycket av nodspecifika och cilierelaterade gener och förkortade nodcilierna, men det underliggande öppna DNA-landskapet förblev i stort sett intakt. Detta indikerar att tidigare faktorer lägger den epigenetiska grunden, medan sena faktorer främst finjusterar genuttrycket utan att omstrukturera kromatinet.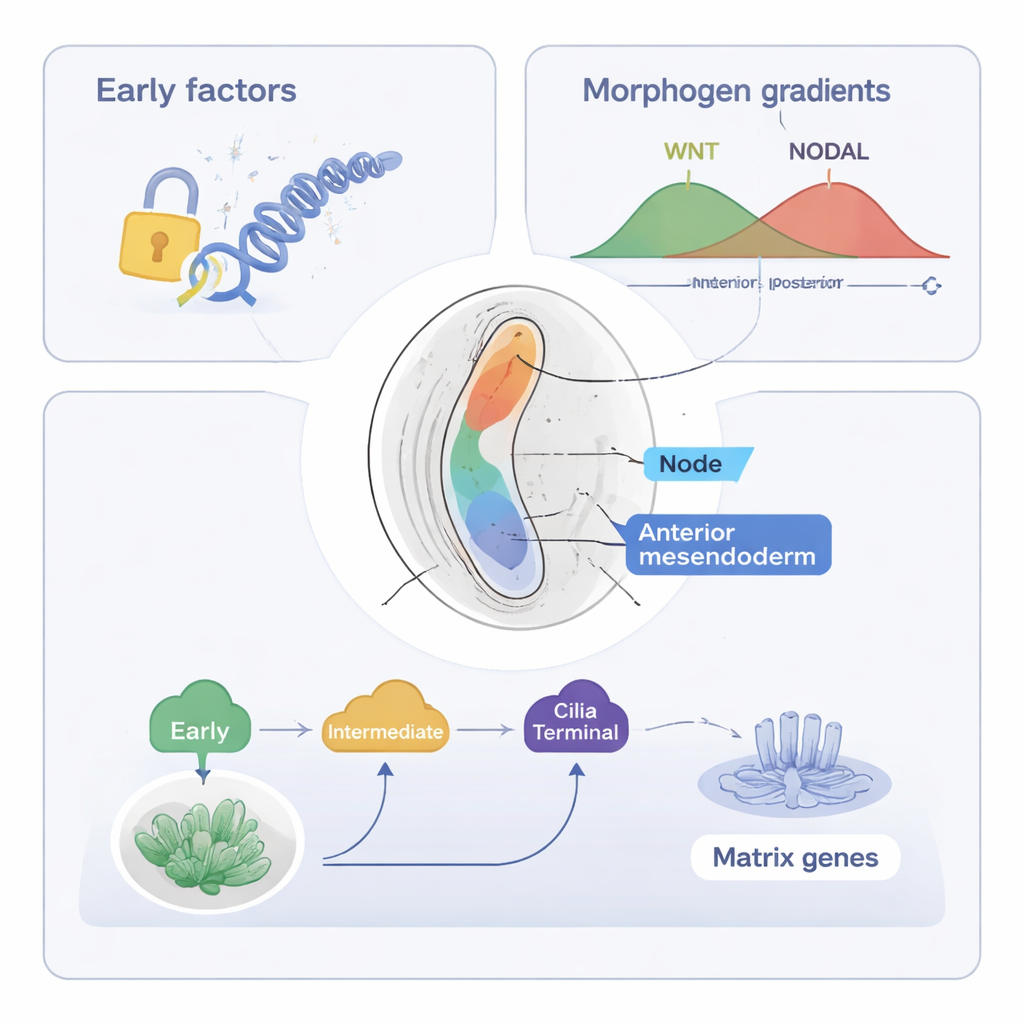
Varför detta är viktigt för förståelsen av utveckling
För en icke-specialist kan detta arbete ses som uppbyggandet av ett högupplöst ”kopplingsschema” för hur ett embryo anlägger sin kroppslayout. Författarna visar att cellödesval under gastrulation inte bara styrs av vilka signaler som är närvarande, utan också av när och var DNA-brytare öppnas och vilka transkriptionsfaktorer som verkar i sekvens. Deras ST-MAGIC och ST-MAGIC (+) atlaser utgör en resurs för att utforska dessa relationer över rum och tid och erbjuder en ram som kan informera studier av medfödda missbildningar, stamcellsbaserade embryomodeller och i förlängningen aspekter av mänsklig utveckling.
Citering: Yang, X., Xie, B., Shen, P. et al. Integrated multi-omic atlas reveals the hierarchy of spatiotemporal regulatory networks of mouse gastrulation. Nat Commun 17, 1572 (2026). https://doi.org/10.1038/s41467-026-68291-w
Nyckelord: gastrulation, genregleringsnätverk, single-cell multi-omics, embryomönstring, musutveckling