Clear Sky Science · sv
De novo-varianter i splitsningsfaktorn SF3B1 är förenade med neurodevelopmentella störningar
När ett enda genfel rubbar hjärnans tidiga ritning
Varför utvecklar vissa barn inlärningssvårigheter, anfall eller ätproblem även när graviditet och förlossning verkar ha varit normala? Denna studie undersöker en enskild gen, SF3B1, som hjälper celler att bearbeta genetiska budskap. Forskarnas resultat visar att nya, spontana förändringar i denna gen kan subtilt rubba hur hjärnceller läser DNA-instruktioner, vilket leder till ett tidigare oigenkänt neurodevelopmentellt syndrom.
En huvudredaktör för genetiska budskap
Varje cell i vår kropp måste omvandla rå genetisk text till tydliga instruktioner innan den kan tillverka proteiner. Detta redigeringssteg, känt som RNA-splitsning, tar bort icke-kodande segment och fogar ihop de användbara bitarna. SF3B1 är en central del av cellens "splitsningsmaskin." Hittills har förändringar i SF3B1 mest känts igen för sin roll vid cancer, där tumörceller förvärvar mutationer i denna gen under livet. Det nya arbetet ställer en annan fråga: vad händer när en skadlig förändring i SF3B1 finns från befruktningen i varje cell i kroppen?
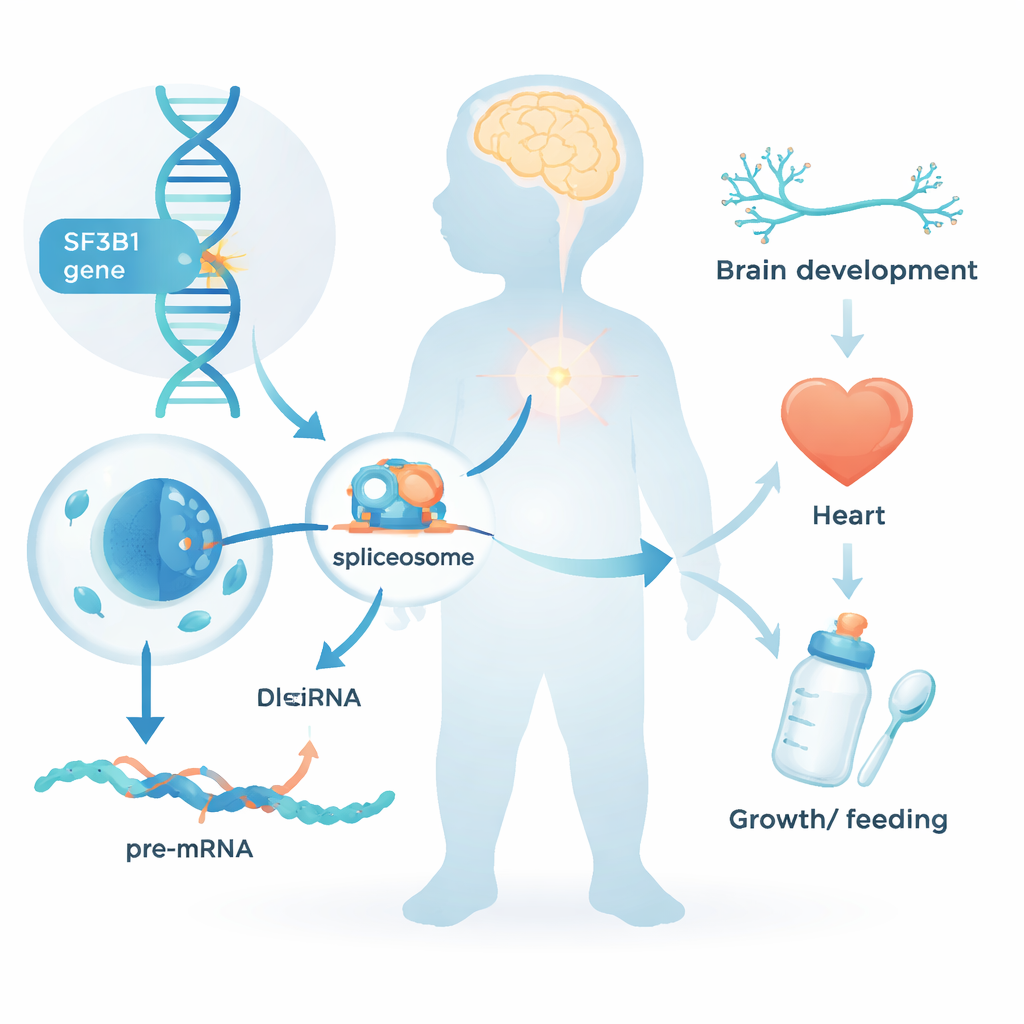
En nyupptäckt barndomssyndrom
Teamet samlade data från 26 barn och unga vuxna som alla bar på sällsynta SF3B1-varianter, främst uppkomna de novo — det vill säga inte ärvda från någon förälder. Nästan alla hade neurodevelopmentella problem: försenad utveckling i att sitta, gå eller tala; intellektuell funktionsnedsättning som oftast var mild till måttlig; och hos ungefär hälften anfall. Många hade låg muskeltonus och behövde extra hjälp vid matning, ibland via en gastrostomi. Ansiktsdrag var lätt ovanliga men inte identiska mellan barnen; ett påtagligt och vanligt tecken var hög eller klyftad gom. Flera deltagare hade också hjärtanomalier, tillväxthämning eller litet huvudomfång, vilket visar att påverkan av SF3B1-förändringar sträcker sig bortom hjärnan.
Två klasser av genetiska förändringar, två kliniska mönster
Forskarna skiljde mellan två breda typer av SF3B1-varianter. Den ena gruppen omfattade "loss-of-function"-förändringar, såsom för tidiga stoppsignaler, vilka förväntas minska mängden fungerande SF3B1-protein. Den andra gruppen innehöll missense-varianter, där en enda aminosyra i proteinet ändras. Genom att klustra barnens medicinska drag observerade teamet att de med missense‑varianter tenderade att ha mer uttalade och komplexa problem, inklusive högre förekomst av hjärt- och mag-tarm‑anomalier, kortvuxenhet och mikrocefali. Loss-of-function‑varianter var däremot ibland ärvda från en mildt påverkad eller till och med till synes frisk förälder, vilket tyder på att en reducerad mängd SF3B1 i vissa individer kan vara förenlig med relativt lindriga symtom.
Finjusteringsfel snarare än komplett kollaps
För att förstå vad missense‑varianterna gör inne i cellerna återskapade forskarna dem i laboratorieceller. Överraskande nog kunde dessa förändrade SF3B1-proteiner fortfarande utföra den grundläggande splitsningsuppgiften tillräckligt väl för att rädda celler där det normala SF3B1 tystats. Det uteslöt en enkel loss-of-function‑förklaring. Med djup RNA-sekvensering undersökte gruppen sedan hela uppsättningen cellulära budskap. De fann att missense‑varianterna subtilt försköt splitsningen av hundratals gener, särskilt genom att ändra vilka splitsningsställen som väljs vid exonändar och genom att orsaka episodiska exonskippningar. Störningens omfattning var mindre än den som setts med den klassiska cancerassocierade SF3B1‑mutation K700E, men ändå betydande: många påverkade gener är involverade i hjärnans utveckling, nervkopplingar och grundläggande processer såsom RNA‑hantering och proteinsyntes.
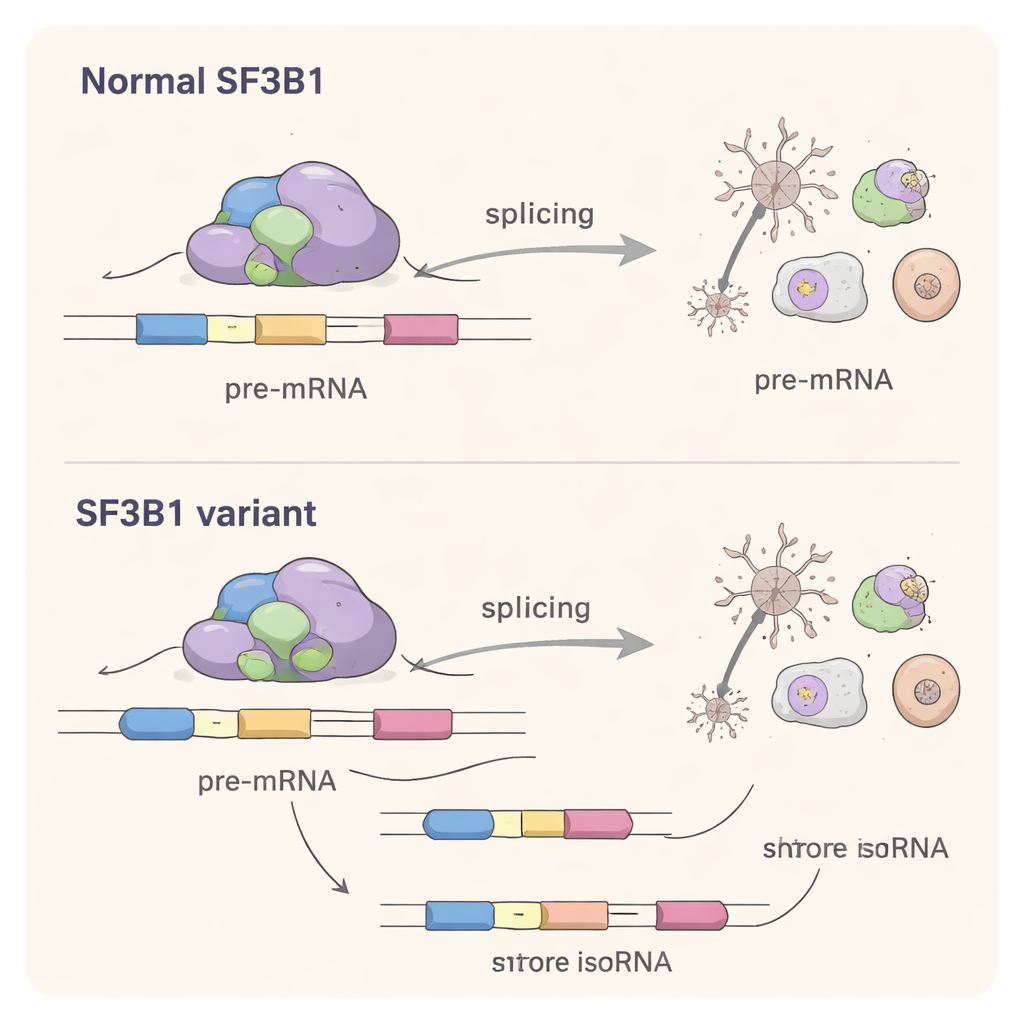
En gemensam mekanism mellan cancer och hjärnstörningar
Även om de flesta neurodevelopmentella SF3B1‑varianter förekommer på andra positioner än de välkända cancerrmutationerna, stör de samma kärnprocess: precis igenkänning av splitsningsställen i RNA. Studien visar att dessa utvecklingsrelaterade varianter har en egen "splitsningssignatur", där alternativa splitsningsställen väljs som ofta ligger närmare de normala än de som favoriseras i cancer. Detta talar för en change‑of‑function‑mekanism, där det muterade proteinet konkurrerar med den normala kopian och skjuter splitsningsmaskineriet mot måttligt felaktiga val i många gener samtidigt.
Vad detta betyder för familjer och framtida forskning
För drabbade familjer identifierar arbetet SF3B1 som en ny orsak till neurodevelopmentella störningar som nu kan testas i genetiska kliniker, vilket potentiellt kan avsluta långa diagnostiska sökande. Mer övergripande lägger det till SF3B1 till en liten men växande grupp av splitsningsgener vars förändringar kan driva både cancer och barndomsrelaterade hjärnstörningar, beroende på när och hur genen ändras. Genom att kartlägga hur specifika SF3B1‑varianter omformar RNA‑splitsning lägger studien grunden för framtida terapier som syftar till att korrigera felaktig splitsning på ett riktat sätt.
Citering: Uguen, K., Bergot, T., Scott-Boyer, MP. et al. De novo variants in the splicing factor gene SF3B1 are associated with neurodevelopmental disorders. Nat Commun 17, 1569 (2026). https://doi.org/10.1038/s41467-026-68284-9
Nyckelord: RNA-splitsning, SF3B1, neurodevelopmentella störningar, de novo-varianter, splicesomopatier