Clear Sky Science · sv
Viskoelastiskt hydrogel‑primade CAR‑makrofager för behandling av lungfibros
Att förvandla kroppens städare till precisa reparationslag
Lungfibros är en förödande lungsjukdom där normal, fjädrande lungvävnad gradvis ersätts av stel ärrvävnad. Människor får svårt att andas, och dagens läkemedel bromsar oftast bara försämringen. Denna studie undersöker en ny idé: att omvandla kroppens egna städceller, makrofager, till konstruerade ”smarta städare” och sedan förstärka deras kraft med en särskilt utformad mjuk gel. Tillsammans hjälper dessa metoder cellerna att jaga upp de ärrbildande bovarna och till och med luckra upp den styva vävnaden i skadade lungor.
När läkning blir skadlig
I friska lungor hjälper fibroblaster till att upprätthålla det känsliga kollagennätverket som stöder alveolerna. Vid lungfibros blir dessa celler överaktiva och avsätter tjocka kollagentrådar som kväver luftutrymmena. Befintliga läkemedel kan dämpa dessa processer men sällan vända dem. Författarna fokuserar på en ytmolekyl kallad fibroblastaktiveringsprotein (FAP), som är riklig på överaktiva fibroblaster men sällsynt i normal vävnad. Om immunceller kunde tränas att känna igen FAP, skulle de kunna selektivt avlägsna de ”okontrollerade” fibroblasterna som driver ärrbildning samtidigt som friska grannar sparas.
Omskolning av makrofager för att rikta in sig på ärrbyggare
Makrofager är patrullerande immunceller som normalt sveper upp döda celler, mikrober och cellulärt skräp. Forskargruppen utrustade dem med en kirimär antikroppsreceptor (CAR) som känner igen FAP och skapade CAR‑makrofager (CAR‑M). I odlingsskålar åt dessa CAR‑M effektivt FAP‑rika fibroblaster och dödade dem, samtidigt som de i hög grad ignorerade celler med låg FAP‑nivå. De bröt också ner kollagenrika geler mer kraftfullt än omodifierade makrofager, vilket tyder på en dubbel fördel: eliminera cellerna som skapar ärr och direkt bryta ner ärrmatrisen. Dessa effekter gällde både i standardcellinjer och i primära musmakrofager, som ligger närmare situationen i vävnader. 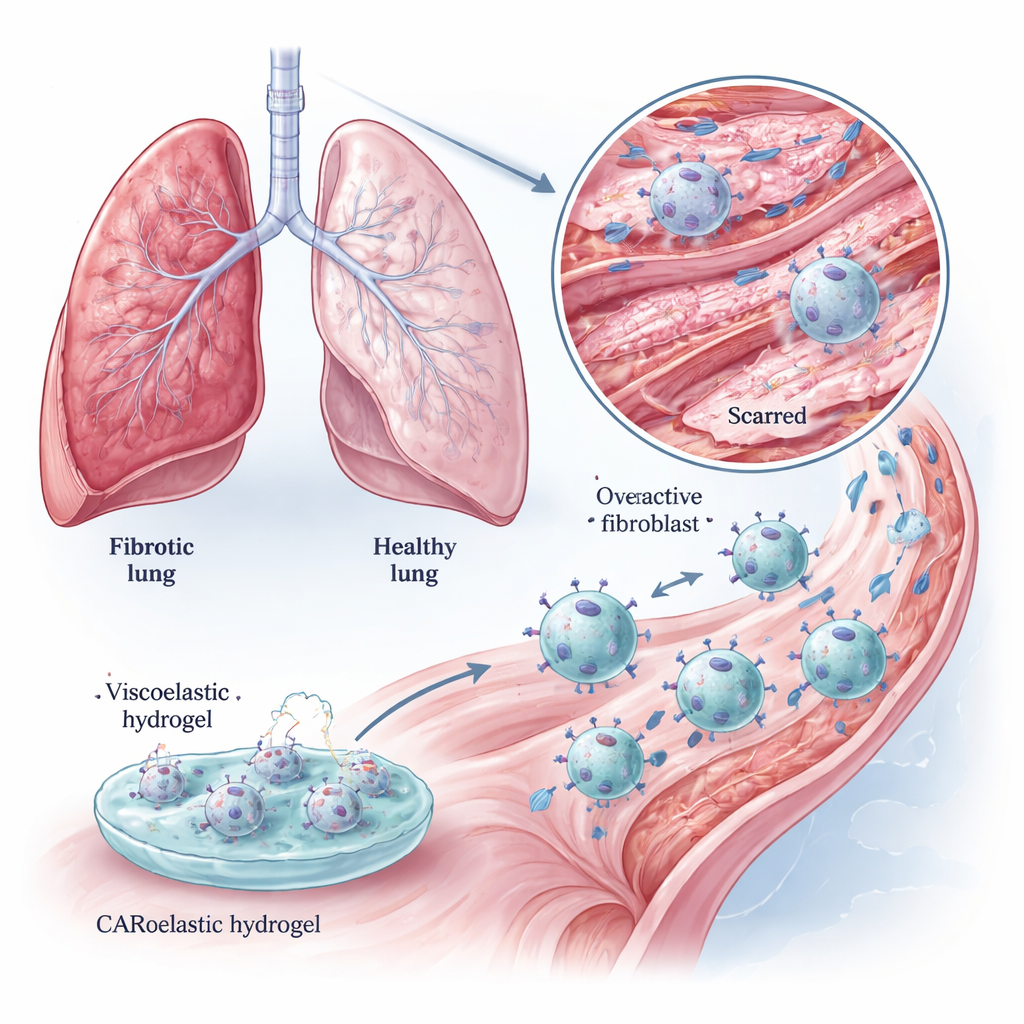
Priming av immunceller med en mjuk, viskoelastisk gel
Genetisk modifiering av celler är kraftfull men komplex. Forskarna frågade därför om en rent fysisk signal — ett mjukt, viskoelastiskt hydrogel — kunde finjustera CAR‑M‑beteendet ytterligare. De byggde ett gelatinalginate‑hydrogel vars ”loss modulus”, ett mått på hur det långsamt relakserar under belastning, kunde ställas in noggrant utan att ändra den totala styvheten. När CAR‑M kortvarigt odlades på geléer med rätt viskoelasticitet ökade deras förmåga att döda mål‑fibroblaster mer än vid vanliga kemiska stimulanser, och effekten kvarstod i minst två dagar. Dessa ”Gel‑CAR‑M” aktiverade också gener kopplade till immunaktivering och vävnadsombyggnad, samtidigt som gener associerade med fibros nedreglerades, vilket antyder att gelupplevelsen präglade cellerna mot en mer anti‑ärr identitet.
Hur en mjukare yta omkopplar cellbeteende
För att förstå varför gelen spelade roll undersökte teamet den fysiska tillståndet för CAR‑receptorerna på cellsytan. En fluorescerande probe avslöjade att hydrogel‑primade CAR‑M hade lägre membrantension — cellens yttre skikt var mer avslappnat. Under dessa förhållanden spred sig CAR‑molekylerna från täta kluster till mer isolerade singlar och par. Biokemiska tester visade att dessa dispergerade receptorer gynnade former som lättare utlöste intern signalering, särskilt längs banor som ERK som styr aktivering och dödande förmåga. Att efterlikna spänningsfallet med en liten molekyl reproducerade samma receptorutbredning och förbättrad målcellsdöd, vilket stöder idén att mekanisk avslappning av membranet räcker för att ”för‑beväpna” cellerna innan de ens möter sina mål. 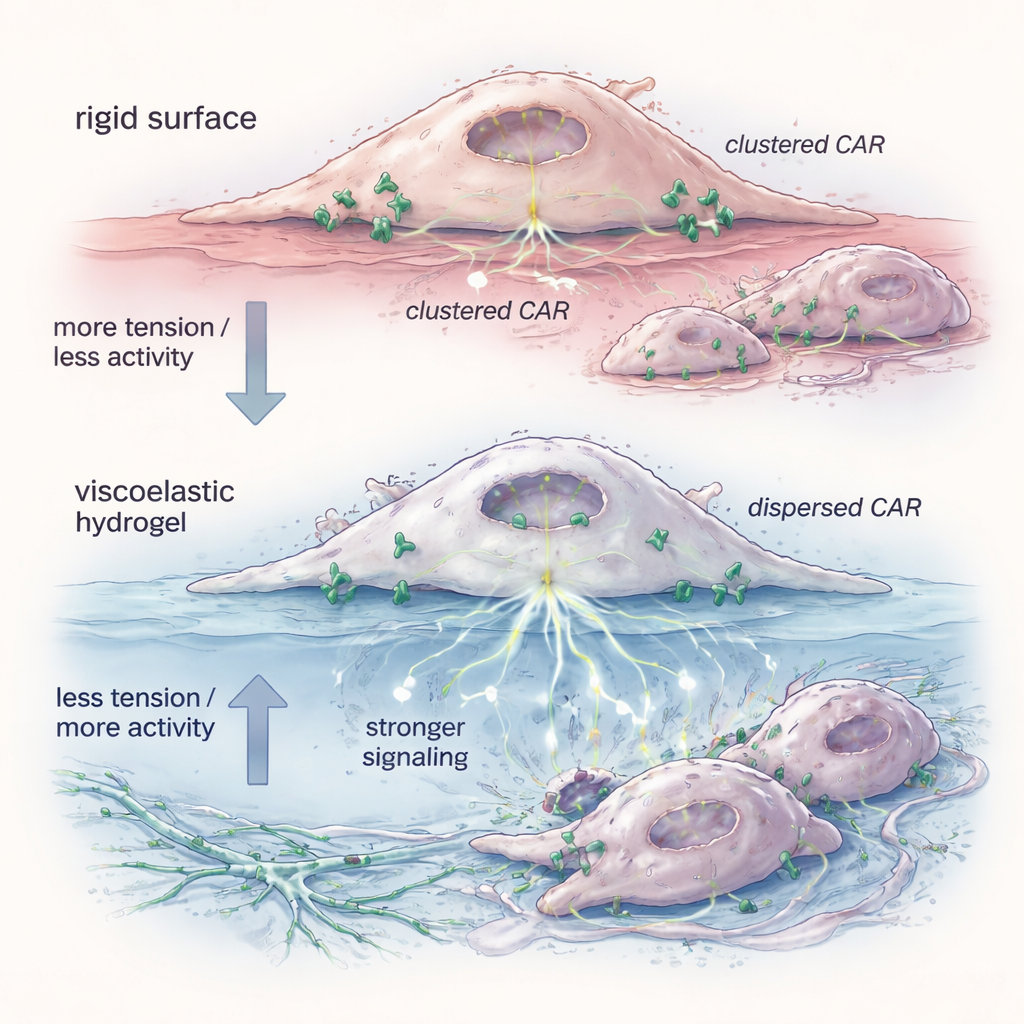
Reparera ärrade lungor hos möss
Det slutgiltiga testet var en musemodell för läkemedelsinducerad lungfibros. Djuren fick antingen vanliga makrofager, standard CAR‑M eller hydrogel‑primade Gel‑CAR‑M. Alla behandlade möss förbättrades jämfört med obehandlade kontroller, men Gel‑CAR‑M gav bäst resultat: deras lungor innehöll mindre kollagen, mer normala luftutrymmen och färre FAP‑positiva fibroblaster. Genutläsningar från lungvävnad visade att Gel‑CAR‑M dämpade inflammatoriska signaler och minskade uttrycket av ärrrelaterade gener mer effektivt än standard CAR‑M. Spårade celler kvarlevde i lungan i minst en vecka, och förlängda säkerhetskontroller över 12 veckor visade inga stora organskador, blodavvikelser eller tecken på autoimmunitet.
En ny riktning för cellbaserade antifibrosbehandlingar
För icke‑specialister är huvudbudskapet att kombinationen av riktad cellengineering och smarta material kan förvandla medfödda immunceller till mycket effektiva, men inte onödigt genetiskt komplicerade, ärrbekämpande verktyg. Genom att kort vila de konstruerade makrofagerna på en noggrant justerad mjuk gel, ”förinställde” forskarna mekaniskt deras ytreceptorer till ett mer responsivt läge. I möss med lungfibros översattes detta till bättre avlägsnande av skadliga fibroblaster, nedbrytning av överskott av kollagen och partiell återställning av normal lungstruktur — utan uppenbara säkerhetsproblem. Mycket arbete återstår innan mänskliga försök, men strategin antyder att finjustering av den fysiska miljön för terapeutiska celler en dag kan göra behandlingar mot fibrotisk lungsjukdom både mer potenta och mer precisa.
Citering: Zhang, Y., Liu, Z., Kong, W. et al. Viscoelastic hydrogel primed CAR-macrophage for pulmonary fibrosis treatment. Nat Commun 17, 1663 (2026). https://doi.org/10.1038/s41467-025-68033-4
Nyckelord: lungfibros, CAR‑makrofagterapi, viskoelastiskt hydrogel, fibroblastaktiveringsprotein, cellmekanobiologi