Clear Sky Science · sv
Molekylär grund för hämningen av nybildning av DNA‑metylering av TCL1A
Hur celler bestämmer vad de ska komma ihåg
Varje cell i din kropp bär i huvudsak samma DNA, men nervceller, blodceller och hudceller beter sig mycket olika. Ett sätt som celler "kommer ihåg" sin identitet är genom kemiska märken som läggs till DNA, en process som kallas DNA‑metylering. Denna studie avslöjar, i atomär detalj, hur ett litet protein kallat TCL1A kan stänga av de enzymer som skriver dessa metylmärken. Eftersom både DNA‑metylering och TCL1A är kopplade till cancer och reproduktionsstörningar kan förståelsen av detta molekylära dragkamp till sist inspirera nya terapier.
Cellens maskineri för att märka DNA
DNA‑metylering fungerar som ett blyertsstreck i genomets marginaler och hjälper till att tysta vissa gener och stabilisera genomet när celler utvecklas. Två enzymer, DNMT3A och DNMT3B, är huvud"skrivarna" som placerar nya metylmärken under tidig utveckling och när stamceller differentierar. Om dessa enzymer är muterade eller felreglerade kan mönstret av DNA‑märken bli förvrängt och bidra till utvecklingssyndrom och blodcancer. TCL1A är ett protein mest känt för sin roll i immuncellscancer, där det ofta överproduceras. Tidigare arbete antydde att TCL1A kan binda DNMT3A och DNMT3B och dämpa deras aktivitet, men ingen visste exakt hur detta block uppnås.
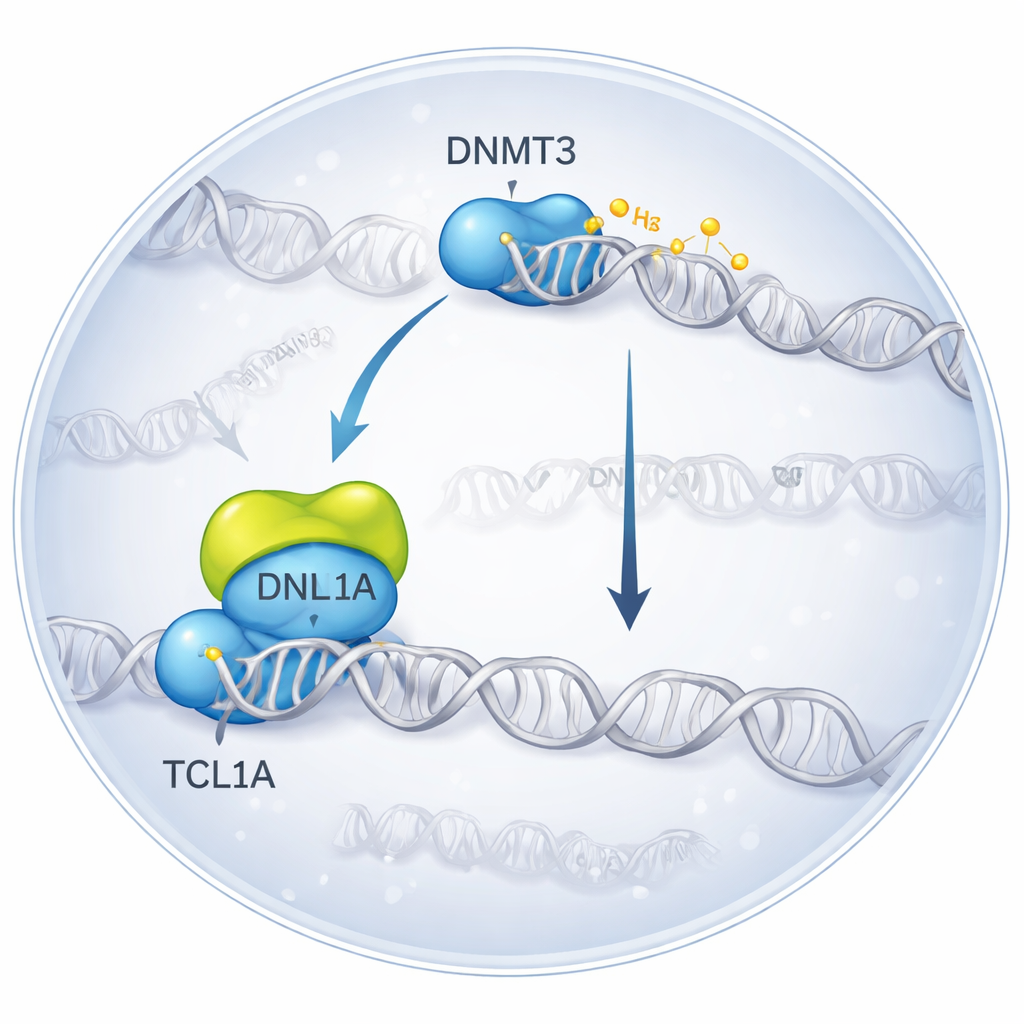
Frysa ett molekylärt möte i 3D
Forskarna använde kryo‑elektronmikroskopi, en teknik som avbildar blixtfrysta molekyler, för att visualisera komplexet som bildas när DNMT3A binder TCL1A. De fann att två DNMT3A‑molekyler parar ihop sig, och på varje sida dockar ett TCL1A‑dimer på den katalytiska delen av DNMT3A — just den region som normalt interagerar med hjälpproteiner och DNA. Denna bindningsyta överlappar med den plats där en annan partner, DNMT3L, vanligtvis fäster för att öka DNMT3A:s aktivitet. I biokemiska tester minskade tillsats av TCL1A kraftigt förmågan hos både DNMT3A och DNMT3B att metylera DNA, även i närvaro av DNMT3L, vilket bekräftar att det strukturella komplexet motsvarar ett starkt inhiberat tillstånd.
En formförändring som låser enzymerna
När forskarna tittade närmare såg de att TCL1A‑bindning inte bara lägger sig ovanpå det aktiva sätet som ett lock. Istället utlöser den en subtil men långtgående förändring i DNMT3A:s form. Två flexibla regioner av enzymet, kända som måligenkänningsloopen och den katalytiska loopen, svänger bort från de positioner de intar när DNMT3A är bunden till DNA. I den aktiva formen ligger dessa loopar intill DNA och bildar ett fack för en liten molekylbränsle kallad SAM, som donerar metylgruppen. När TCL1A är fäst viker sig den katalytiska loopen istället in i SAM‑facket och blockerar det, samtidigt som det blir svårare för DNA att nå enzymet. Bindningsmätningar bekräftade att DNMT3A i komplex med TCL1A inte längre kan greppa DNA eller SAM på ett detekterbart sätt.
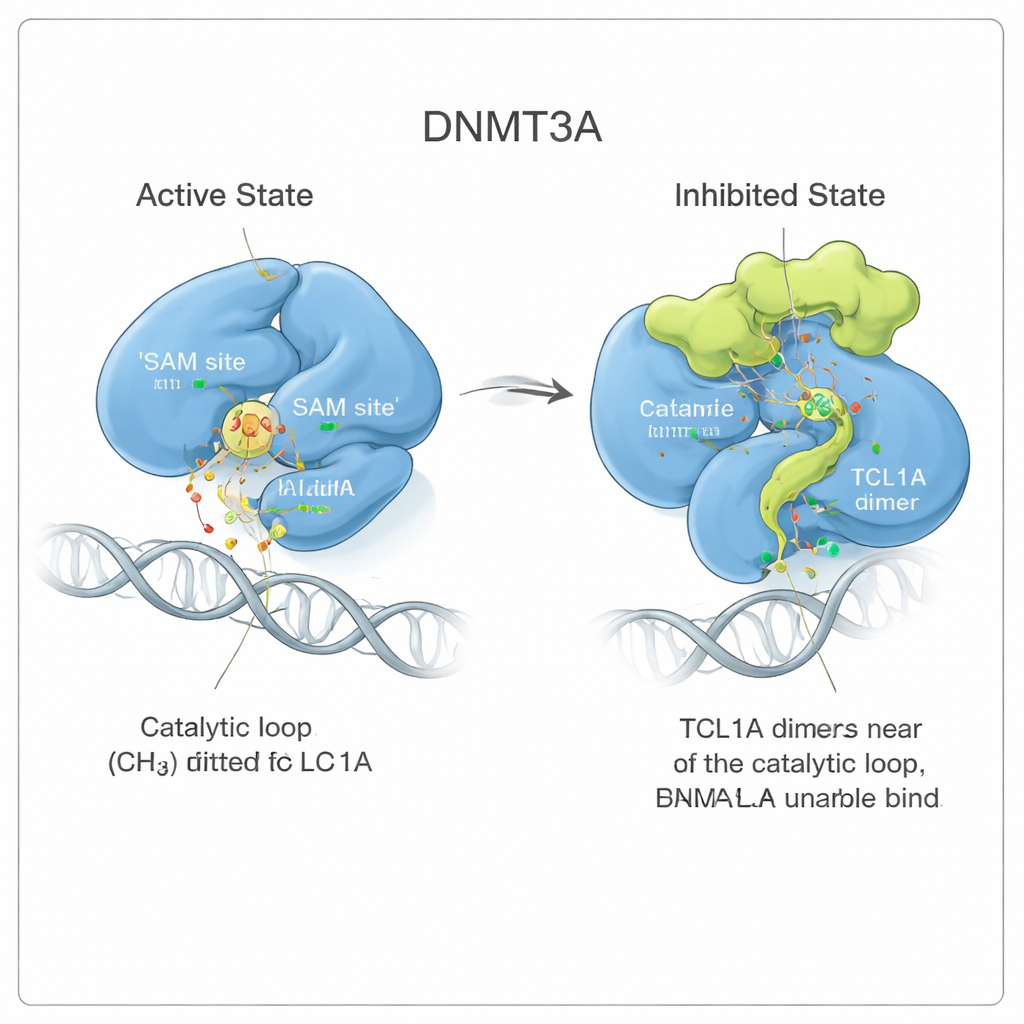
Att se ett dynamiskt block i rörelse
För att förstå hur stabil denna inhiberade konformation är körde författarna långa molekylärdynamiska simuleringar, i praktiken fysikbaserade filmer av molekylerna i lösning. När DNMT3A var bunden till sin aktivator DNMT3L höll sig den katalytiska loopen kvar i sin aktiva position. När TCL1A var närvarande blev den loopen mycket mer rörlig, fladdrade omkring men ockuperade upprepade gånger SAM‑facket som sjögräs som virvlar och ändå stoppar en avlopp. Denna ständiga rörelse krympte det tillgängliga utrymmet för SAM mer än tiofaldigt, vilket stöder en modell där TCL1A utnyttjar DNMT3A:s naturliga flexibilitet för att ålägga en dynamisk, snarare än stel, form av hämning.
Konsekvenser för utvecklande celler och sjukdom
Teamet frågade sedan vad denna molekylära blockad betyder för verkliga celler. De konstruerade musens embryonala stamceller för att producera mänskligt TCL1A under en fas då cellerna normalt uppreglerar DNA‑metylering när de börjar differentiera. Genomomfattande metyleringskartläggning visade att celler som överuttryckte TCL1A misslyckades med att uppnå den vanliga höga nivån av DNA‑metylering, vilket nära liknade celler där både Dnmt3a och Dnmt3b‑gener hade slagits ut. En mutant version av TCL1A som binder DNMT3‑enzymer dåligt hade liten effekt, vilket understryker att den fysiska interaktionen är avgörande. Dessa fynd knyter den strukturella mekanismen till omfattande epigenetiska förändringar över genomet.
Vad detta betyder för hälsa
Tillsammans visar arbetet hur TCL1A kan agera som en kraftfull broms på de enzymer som lägger ner nya DNA‑metylmärken. Genom att docka vid ett kritiskt gränssnitt ompositionerar TCL1A flexibla loopar i DNMT3A och DNMT3B så att de inte längre kan binda sitt DNA‑mall eller sitt kemiska bränsle, vilket leder till en global förlust av metylmärken i celler. I normal utveckling kan denna typ av finjusterad kontroll hjälpa till att balansera när och var metylering läggs till. När TCL1A är felplacerat eller överproducerat, som i vissa blodcancerformer och sällsynta reproduktionsstörningar, kan samma mekanism rubba cellens epigenetiska program. Att förstå denna interaktion i atomär upplösning öppnar möjligheter att designa molekyler som efterliknar eller motverkar TCL1A:s effekter och potentiellt återställer friska DNA‑metyleringsmönster.
Citering: Liu, Q., Li, J., Wang, X. et al. Molecular basis for the inhibition of de novo DNA methylation by TCL1A. Nat Commun 17, 2159 (2026). https://doi.org/10.1038/s41467-025-67710-8
Nyckelord: DNA‑metylering, DNMT3A, TCL1A, epigenetik, cancer