Clear Sky Science · sv
Exempel på leveransmetoder för protein‑röntgenkristallografi med särskilt fokus på provförbrukning
Att iaktta molekyler i arbete
Röntgenkristallografi låter forskare se hur atomerna i proteiner är ordnade — de små maskinerna som driver livet. En nyare metod, kallad seriekristallografi, går ett steg längre: den kan fånga ”molekylfilmer” av proteiner i rörelse, till exempel enzymer som bearbetar ett läkemedel eller fotosyntetiska proteiner som klyver vatten. Men det finns en hake. Många viktiga proteiner är svåra att producera och kristallisera, och nuvarande experiment kan förbruka milligram till gram av dyrbart material. Denna översiktsartikel ställer en till synes enkel fråga: hur kan vi leverera kristaller i kraftfulla röntgenstrålar samtidigt som vi slösar så lite prov som möjligt?
Varför seriekristallografi behöver bättre leverans
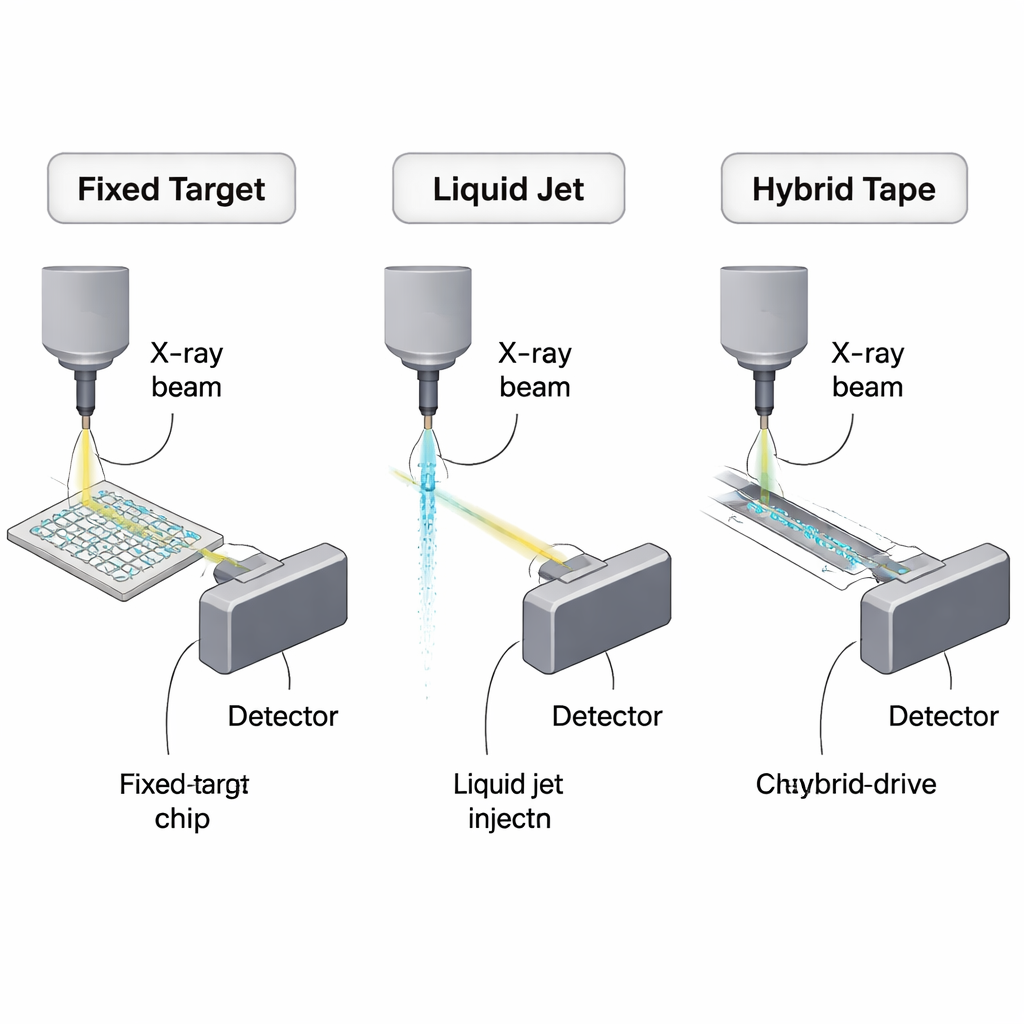
Traditionell kristallografi byggde på en enda stor kristall som roterades i en röntgenstråle. Seriekristallografi vänder på konceptet: i stället för en stor kristall används tusentals mikrokristaller, var och en bara en gång, som skjuts eller skannas genom ultrastarka röntgenpulser från synkrotroner eller röntgen‑frielektronlaser (XFEL). Detta möjliggör datainsamling i rumstemperatur och snabba ”ögonblicksbilder” av kemiska reaktioner, men det innebär också ett konstant behov av att ersätta kristaller i takt med röntgenpulsernas frekvens, som kan nå upp till miljontals pulser per sekund. Mycket av kristallsuspensionen möter aldrig strålen och kasseras, så att minska provförbrukningen har blivit en central teknisk och ekonomisk utmaning för fältet.
Fixerade mål: små chip som tömmer varje droppe
En viktig strategi är att immobilisera mikrokristaller på små solida bärare som kallas fixerade mål. Istället för att spraya kristaller förbi strålen ordnar forskare dem i matriser på kisel‑ eller polymerchip och flyttar chippet så att varje kristall förs in i röntgenfokus en gång. I bästa tänkbara fall, i ett tankeexperiment, skulle omkring 10 000 mikrokristaller av ett modellprotein i princip kunna ge en komplett dataset med bara cirka 450 nanogram protein. Verkliga enheter är ännu inte så sparsamma, men de minskar redan behovet till tiotals mikrogram upp till några tiondels milligram — flera ordningar bättre än tidiga serieexperiment. Översikten jämför kiselnät, ultratunna polymerfilmer och flerskikts plastchip och väger deras styrkor (låg bakgrundsspridning, möjlighet till kristalltillväxt på chip, kompatibilitet med studier i rumstemperatur) mot praktiska problem som uttorkning, oönskad spridning från chipmaterialet och extra ”dött volym” som introduceras av manuell pipettering.
Flytande jetstrålar och viskösa strömmar: snabba men hungriga
En annan familj metoder håller kristaller suspenserade i vätska och levererar dem kontinuerligt genom strålen. Gasdynamiska virtuella munstycken skapar hårfina jetstrålar som kan följa snabba XFEL‑pulståg, vilket gör dem till ett arbetsdjur för tidsupplösta studier och mix‑och‑injicera‑experiment där reaktioner triggas genom snabb blandning strax innan exponering. Eftersom jetstrålar körs kontinuerligt möter dock det mesta av strömmen aldrig en röntgenpuls. Även med noggrann justering förbrukar praktiska experiment långt mer protein än det teoretiska minimumet — typiskt tiotals till hundratals mikroliter koncentrerad kristallsuspension. För att lindra detta har forskare utvecklat effektivare konstruktioner, såsom dubbelströmningsmunstycken som omsluter kristallströmmen med en uppoffrande vätska, elektrospunna ”MESH”‑injektorer som fungerar vid lägre flöden, och högviskösa extrudrar som pressar kristaller inbäddade i geler eller lipidisk kubisk fas vid mikroliter‑per‑minut eller långsammare. Dessa viskösa metoder är särskilt värdefulla för ömtåliga membranproteiner och för studier i rumstemperatur vid synkrotroner, men deras tjockare strömmar ökar bakgrundsspridningen och är mindre lämpade för de allra snabbaste röntgenkällorna.
Droppar, tejper och hybrider: matcha pulser en för en
En tredje, alltmer kreativ, klass av ”hybrida” angreppssätt kombinerar solida bärare med kontrollerad vätske‑ eller droppleverans. Tejpdrivna system avsätter till exempel droppar eller tunna vätskestrimmor på en rörlig polymerfilm som passerar genom strålen; genom att tajma rörelsen kan reaktionssteg eller gasexponering undersökas vid bestämda fördröjningar. Drop‑on‑demand‑system går längre och använder akustiska eller piezoelektriska enheter för att skjuta ut nanoliter‑ eller till och med pikoliterdroppar först när en röntgenpuls förväntas, vilket dramatiskt minskar spill. Vissa konstruktioner blandar en ligantdropp i en förplacerad dropp innehållande kristaller på tejpen strax innan den når strålen, vilket möjliggör tidsupplöst enzymologi med noggrant tilldelade reagenser. Andra hybrider, som LAMA‑på‑chip‑metoden, tillsätter små substratdroppar direkt på kristaller förmonterade på fixerade mål. I dessa designs varierar rapporterad proteinanvändning brett — från nivåer nära milligram ner till några milligram för fulla tidsserier — vilket visar både löftet och de nuvarande ingenjörsutmaningarna med att synkronisera droppar, kristaller och röntgenpulser.
Hur nära är vi det teoretiska minimumet?
Genom att jämföra dussintals publicerade experiment över fixerade mål, flytande injektorer och hybrida system visar författarna att ingen befintlig metod kommer nära det ideala 450‑nanogramsmärket; även de bästa enheterna överskjuter med ungefär två ordningar av storlek. Ändå framträder tydliga trender. Fixerade mål använder vanligtvis minst protein och är attraktiva när tidsupplöst blandning inte är nödvändig eller kan konstrueras på chip. Flytande jetstrålar dominerar fortfarande de mest krävande tidsupplösta XFEL‑studierna men förblir provintensiva, särskilt när många tidpunkter krävs. Hybrida dropp‑och‑tejpscheman erbjuder några av de största relativa besparingarna, särskilt när dropparnas timing är tätt synkroniserad med röntgenkällan. Framåtblickande argumenterar artikeln för att ytterligare framsteg kommer från bättre mikrofluidisk kontroll, automatisering för att eliminera spilliga hanteringssteg, och användning av kompakta röntgenkällor samt datadriven optimering för att samskapa experiment och leveranssystem som pressar proteinanvändningen allt närmare det teoretiska gränsvärdet.
Citering: Manna, A., Doppler, D., Sripati, M.P. et al. Sample delivery methods for protein X-ray crystallography with a special focus on sample consumption. Nat Commun 16, 9856 (2025). https://doi.org/10.1038/s41467-025-65173-5
Nyckelord: seriekristallografi, protein‑röntgenkristallografi, provleverans, röntgen‑frielektronlaser, mikrofluidik