Clear Sky Science · sv
Minskning av RAD23A förlänger livslängd och mildrar patologi i en musmodell för TDP-43-proteinopati
Varför denna forskning är viktig för familjer och patienter
Många former av demens och motorneuronsjukdomar, inklusive amyotrofisk lateralskleros (ALS) och frontotemporal demens (FTD), kännetecknas av proteiner i hjärnceller som veckas fel, klumpar sig och gradvis förgiftar neuron. En av huvudsyndarna är ett protein kallat TDP-43, som normalt hjälper till att hantera RNA men blir giftigt när det aggregerar. Denna studie ställer en hoppfull fråga: kan vi göra hjärnceller mer motståndskraftiga genom att dämpa ett annat protein, RAD23A, som hjälper styra hur skadade proteiner hanteras? Författarna visar i möss att minskning av RAD23A kan förlänga livet, förbättra rörelseförmågan och minska hjärnskador i en modell för TDP-43–driven sjukdom, vilket pekar mot en ny typ av behandlingsstrategi.
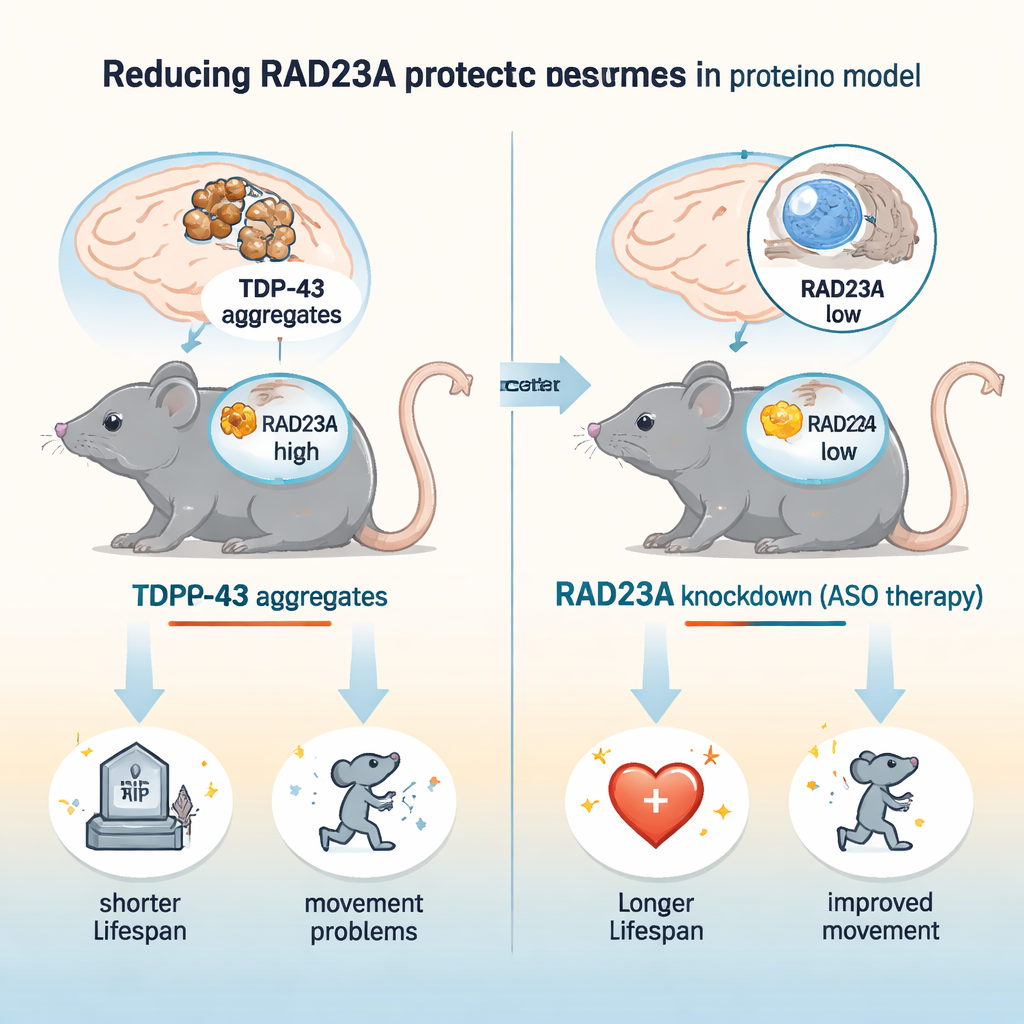
En proteintrafikstockning i sjuka neuroner
Neurodegenerativa sjukdomar präglas ofta av högar av felveckade proteiner som cellens avfallshantering inte lyckas rensa bort. Vid ALS och FTD flyttar TDP-43 ut ur kärnan, bildar klibbiga klumpar och blir kraftigt märkta med ubiquitin, en signal som normalt dirigerar proteiner till proteasomen, cellens huvudsakliga “förstörningsmaskin”. RAD23A är en av flera ”shuttle”-proteiner som kan föra ubiquitin-märkta laster till proteasomen. Tidigare arbete i maskar och odlade neuroner antydde dock att förlust av RAD23-lika proteiner faktiskt kunde skydda mot TDP-43–inducerad skada, ett paradoxalt fynd som denna studie undersökte i ett levande däggdjurs‑hjärna.
Att sänka RAD23A i en TDP-43-musmodell
Forskarna använde en väletablerad musmodell, kallad TAR4/4, som överproducerar mänskligt TDP-43 i neuroner och utvecklar rörelseproblem, ryggradskrökning, tremor och tidig död, vilket speglar centrala drag av ALS/FTD. De sänkte RAD23A på två sätt: genom att injicera nyfödda möss med antisense-oligonukleotider (ASO) som reducerar Rad23a‑RNA, och genom att avla möss som bär en genetisk knockout av Rad23a. En enda ASO‑behandling minskade RAD23A‑nivåerna i hjärna och ryggmärg med ungefär tre fjärdedelar. Hos dessa TDP-43‑möss förlängde RAD23A‑nedreglering livslängden med ungefär 50 % och fördröjde debut och svårighetsgrad av gångstörningar, tremor, ryggradskrökning och bakre lemmars clasping. Intressant nog gav fullständig genetisk förlust av RAD23A ingen ytterligare nytta, vilket tyder på att partiell minskning är optimal och att långvarig total frånvaro kan utlösa kompensatoriska förändringar.
Mindre inflammation, renare proteinhantering och ett lugnare genom
Mikroskopisk undersökning av motorcortex visade att TDP-43‑möss förlorade neuroner och utvecklade stark aktivering av astrocyter och mikroglia, hjärnans stöd- och immunceller. Att sänka RAD23A bevarade nervcellsantalet och minskade markörer för inflammation och celldöd. Biokemiska analyser visade att överproduktion av TDP-43 översvämmade cellerna med ubiquitin-märkta, detergent‑olösliga proteiner och drog in proteasom‑subenheter i dessa aggregat, vilket försvagade cellens förmåga att rensa skadade proteiner. Minskad RAD23A reducerade den totala mängden ubiquitinerade proteiner, höll fler proteasomer i den lösliga, fungerande poolen och återställde flera typer av proteasomaktivitet mot normala nivåer. Samtidigt minskade RAD23A‑nedreglering både totala och aggregerade former av TDP-43, inklusive en särskilt giftig 25‑kilodaltonfragment, och försköt TDP-43 från cytoplasman tillbaka mot kärnan. Genomisk RNA‑sekvensering visade att tusentals genuttrycksändringar som triggas av TDP-43 delvis återställdes när RAD23A minskades, särskilt gener involverade i neuronfunktion, mitokondriell energiproduktion och aggrefilterande vägar som aggrephagy.
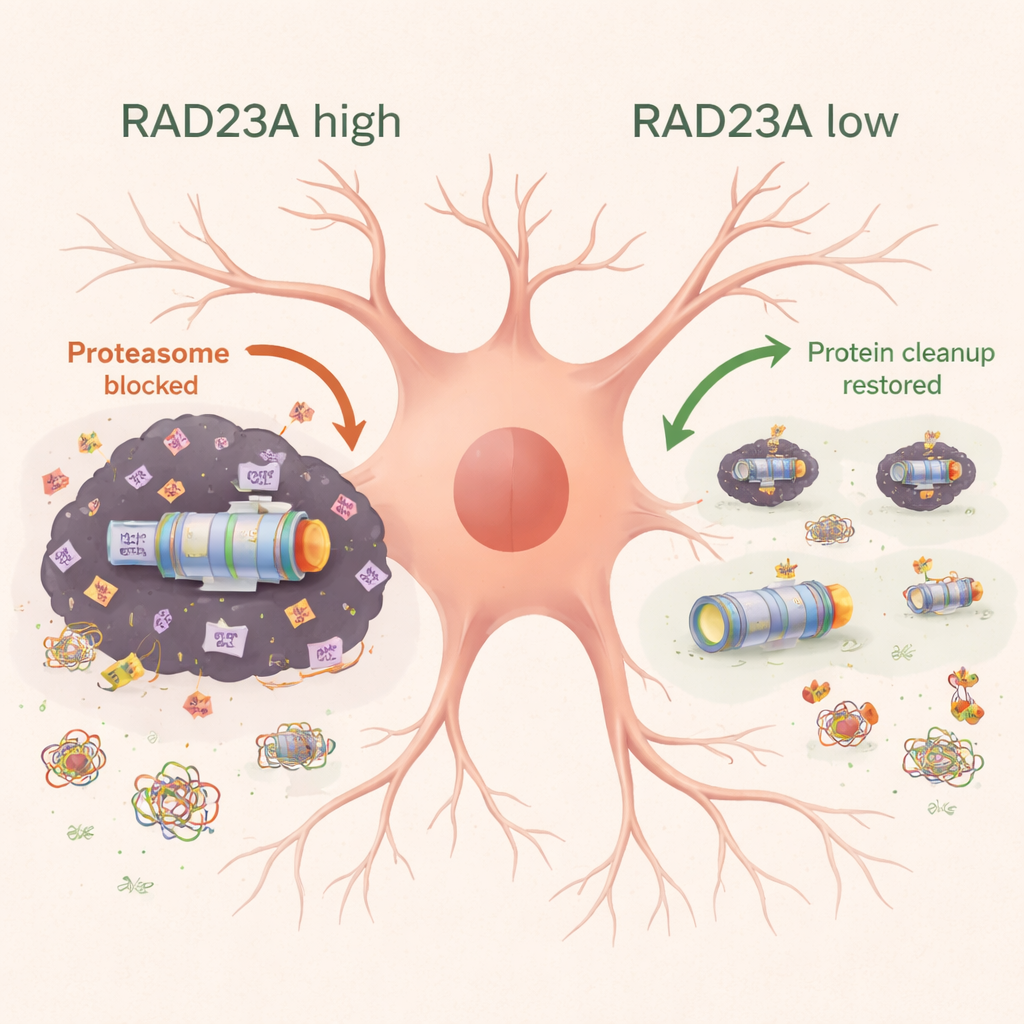
Omarbetning av den dolda ”olösliga” proteomen
För att granska mer noggrant de envisa aggregat som motstår vanliga detergenter använde teamet tung‑isotop‑masspektrometri för att katalogisera proteiner fast i den olösliga fraktionen av muscortex. Uttryck av mänskligt TDP-43 drog in proteasomkomponenter, cytoskelett- och transportproteiner och annan cellulär maskineri. När RAD23A slogs ner skiftade den övergripande sammansättningen av denna olösliga proteom: färre proteasom- och transportrelaterade proteiner fångades upp, medan vissa ribosomala och stressrelaterade proteiner ökade i aggregaten. Viktigt är att denna omstrukturering inte enkelt speglade förändringar i RNA‑nivåer, vilket tyder på att RAD23A främst påverkar hur befintliga proteiner fördelas mellan lösliga och aggregerade tillstånd, snarare än hur mycket av varje protein som tillverkas.
Vad detta kan innebära för framtida terapier
Tillsammans framställer dessa fynd RAD23A som en kraftfull finjusterare av proteinkvalitetskontroll i stressade neuroner. Genom att partiellt sänka RAD23A i en TDP-43–driven musmodell kunde författarna minska giftiga proteinklumpar, återställa aktiviteten i cellens avfallsmaskineri, dämpa skadliga genuttrycksförändringar, begränsa hjärnans inflammation och förlänga livslängd och motorisk funktion. Eftersom onormal TDP-43‑ansamling är utbredd i både ärftliga och sporadiska former av ALS, FTD och närliggande störningar, kan riktning mot RAD23A med människokompatibla antisense‑läkemedel erbjuda ett sätt att skydda neuroner utan att direkt blockera TDP-43 självt, ett essentiellt protein. Mycket återstår att testa i andra modeller och i människor, men arbetet identifierar RAD23A som ett lovande nytt grepp på en gemensam väg för neurodegeneration.
Citering: Guo, X., Prajapati, R.S., Chun, J. et al. Reduction of RAD23A extends lifespan and mitigates pathology in a mouse model of TDP-43 proteinopathy. Nat Commun 17, 1820 (2026). https://doi.org/10.1038/s41467-025-65104-4
Nyckelord: TDP-43, ALS, proteinaggregation, proteasom, antisense-terapi