Clear Sky Science · sv
Optisk superupplösningshistologi av formalinfixerade paraffininbäddade prov: utmaningar och möjligheter
Se mer i bevarade vävnadsprover
Sjukhus världen över bevarar tunna snitt av patienters organ i vaxblock så att sjukdomar som cancer eller njurskador kan studeras under många år. Den här översiktsartikeln förklarar hur nya typer av ljusmikroskop förvandlar dessa rutinprover till kraftfulla fönster mot sjukdom, och avslöjar detaljer som är alltför små för vanliga sjukhusmikroskop. Dessa framsteg skulle kunna hjälpa läkare att upptäcka sjukdomar tidigare, förstå hur de utvecklas och anpassa behandlingar mer precist.
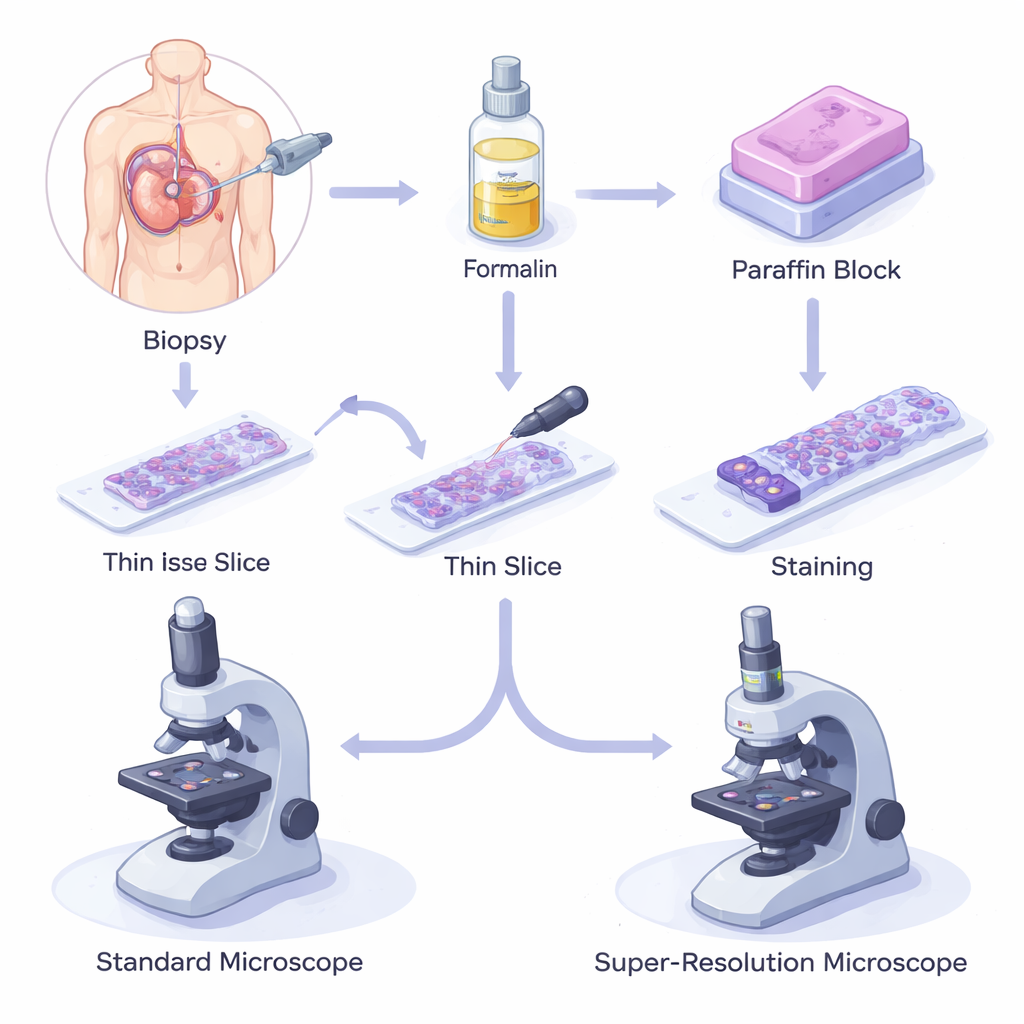
Hur vaxbevarade vävnader driver modern medicin
När en patient genomgår en biopsi tas en liten vävnadsbit bort, fixeras i en kemikalie kallad formalin för att stoppa nedbrytning, och inbäddas sedan i paraffinvax. Blocket skivas i hårtunna snitt, läggs på objektglas, färgas och undersöks i ett ljusmikroskop. Denna metod med formalinfixerade paraffininbäddade (FFPE) prover är billig, pålitlig och kan bevara prover i årtionden i rumstemperatur. Som ett resultat lagras miljontals FFPE-prover i biobanker världen över och stödjer allt från grundläggande biologi till avancerade genetiska och proteinstudier, och bildar ryggraden i modern diagnos och prognos.
Varför vanliga mikroskop inte längre räcker
Traditionella optiska mikroskop begränsas av ljusets fysik: detaljer mindre än ungefär 250 nanometer flyter ihop och blir suddiga. Många strukturer med betydelse för sjukdom—som de fina filtren i njurarna, förbindelserna mellan nervceller eller små förändringar i DNA-arkitekturen inne i kärnan—ligger under denna gräns. Dagens arbetsflöde kombinerar ofta standardljusmikroskopi för en översikt med elektronmikroskopi för nanometervis detaljer, men det tillvägagångssättet är långsamt, kostsamt och kräver helt annan provberedning. Kliniker och forskare söker därför efter ett enda, flexibelt system som snabbt kan skanna stora områden men också krypa in och se nanoskaliga egenskaper i samma FFPE-sektioner som de redan använder.
Nya sätt att skärpa bilden
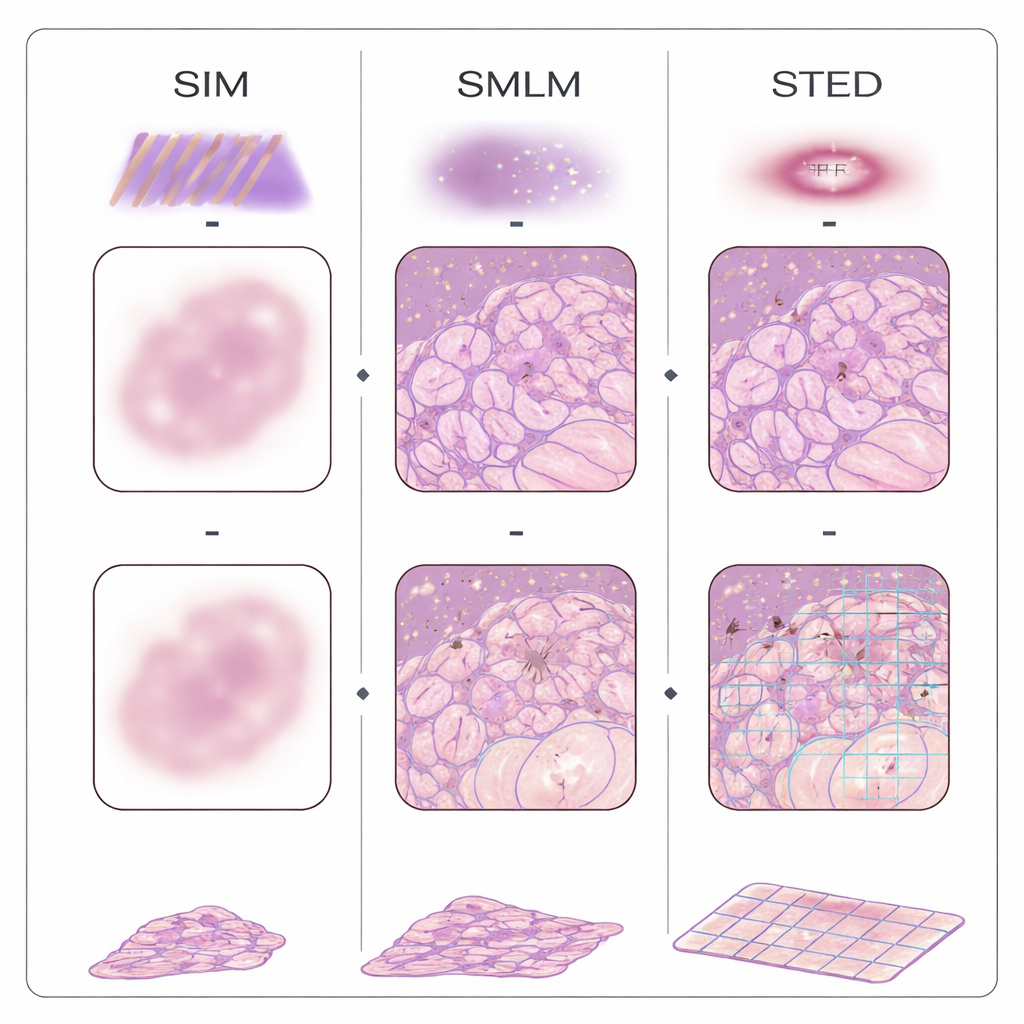
Under de senaste två decennierna har flera familjer av "superupplösnings"-mikroskop brutit den traditionella upplösningsgränsen med hjälp av fluorescerande markörer och smart optik. Metoder för lokalisering av enskilda molekyler växlar molekylerna av och på och bestämmer deras positioner en och en; strukturerad belysning projicerar randiga ljusmönster på vävnaden och använder beräkningar för att återställa finare detaljer; stimulerad utsläckningsmikroskopi (STED) karvar ut en liten lysande fläck med en ringformad stråle; och fluktuationsbaserade tillvägagångssätt analyserar subtilt flimmer i bilden för att härleda struktur. En annan strategi, kallad expansionsmikroskopi, undviker komplicerad optik genom att fysiskt svälla vävnaden i en gel så att vanliga mikroskop kan se tidigare osynliga detaljer. Dessa metoder har redan tillämpats på FFPE-prover från bröst, tjocktarm, bukspottkörtel, njure, hjärna, hud, placenta och andra organ och har avslöjat hur mitokondrier förändras i tumörer, hur njurens filter sviktar och hur proteinkluster bildas vid Alzheimers sjukdom.
Hinder på vägen mot vardagsanvändning
Trots sina löften är dessa tekniker ännu inte redo att bli rutinverktyg i de flesta patologilabb. Många superupplösningssystem är långsamma, täcker endast mycket små synfält eller kräver tiotusentals bilder för att bygga en enda bild med hög detaljrikedom, vilket är opraktiskt när en patolog måste bedöma stora vävnadsområden. Själva FFPE-vävnaderna är optiskt besvärliga: de sprider ljus, ger egen autofluorescens och kan dölja de molekyler som behöver märkas, vilket kan orsaka suddiga bilder eller falska strukturer. Vissa metoder kräver specialfärger, skräddarsydda buffertar eller flerstegs kemiska behandlingar som inte lätt passar in i standardiserade histologiarbetsflöden. Utöver detta är kommersiella instrument kostsamma och komplexa att använda, och de genererade data kräver tung beräkningsmässig bearbetning och lagring.
Förening av smart optik och smart mjukvara
För att övervinna dessa hinder kombinerar forskare förbättrad optik med etikettfri avbildning och artificiell intelligens. Höggenomströmmande, diffraktionsbegränsade metoder som Fourier-ptykografi och icke-linjära optiska mikroskop kan snabbt skanna stora, även ofärgade, FFPE-sektioner och ge kvantitativa kartor över vävnadsstrukturen. Digitala patologiplattformar fångar nu hela objektglas i hög upplösning och använder maskininlärning för att upptäcka tumörer och kvantifiera biomarkörer som HER2, Ki-67 och PD-L1. Djupinlärningsmodeller kan till och med omvandla lågupplösta bilder till superupplösta vyer, vilket potentiellt minskar behovet av viss specialiserad hårdvara samtidigt som man bättre utnyttjar befintliga biobankarkiv.
Vad detta betyder för framtida patienter
Författarna drar slutsatsen att verklig "superupplösningshistologi" av FFPE-prover—som kombinerar nanometernoggrannhet, hög hastighet, rimlig kostnad och kompatibilitet med nuvarande labbrutiner—ännu inte är helt förverkligad, men ligger inom räckhåll. När optiska metoder blir snabbare och mer robusta och AI-baserad analys mognar, kan dessa verktyg avslöja subtila tidiga förändringar i vävnader som idag förbises, förbättra diagnosernas noggrannhet och styra mer personliga behandlingsbeslut. I längden kan förvandlingen av varje arkiverat vaxblock till en högupplöst karta över sjukdom omforma både forskning och klinisk vård.
Citering: Villegas-Hernández, L.E., Dubey, V.K., Acharya, G. et al. Optical super-resolution histology of formalin-fixed paraffin-embedded tissue samples: challenges and opportunities. Nat Commun 16, 9760 (2025). https://doi.org/10.1038/s41467-025-64626-1
Nyckelord: mikroskopi med superupplösning, FFPE-vävnad, digital patologi, optisk avbildning, cancerdiagnostik