Clear Sky Science · sv
Nanozymers som vidgar gränserna för biokatalys
Små hjälpande agenter som snabbar upp kemin
Från öl‑tillverkning till matsmältning förlitar vi oss på osynliga hjälpare kallade katalysatorer som får kemiska reaktioner att gå snabbare. I mer än ett sekel trodde man att biologins katalysatorer bara var ömtåliga proteiner och senare katalytisk RNA. Denna översikt presenterar "nanozymers" – små konstruerade partiklar som beter sig som enzymer men är byggda av robusta material som metaller, oxider och kol. De klarar värme, kyla och hårda förhållanden och börjar omforma hur vi tänker kring kemi i levande system, sjukdomar, industrin och till och med livets ursprung.
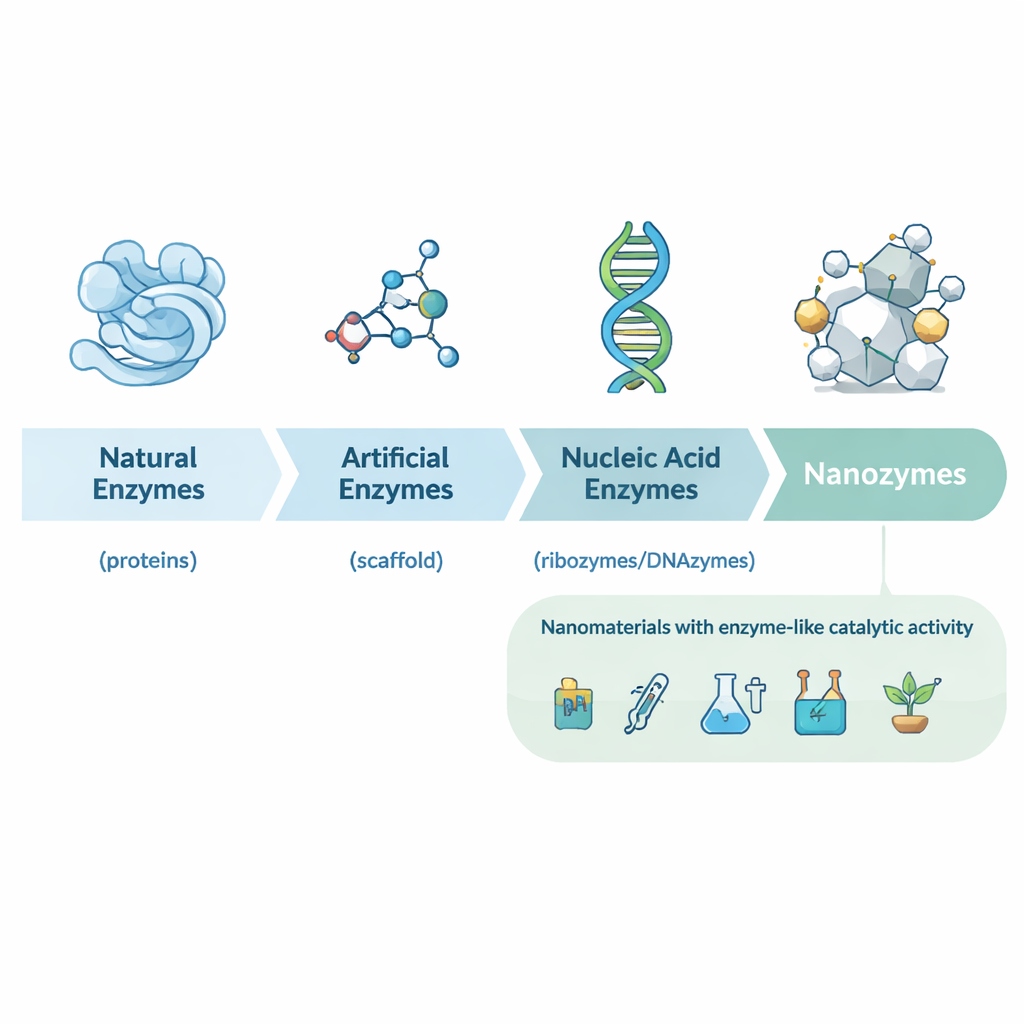
Från naturliga enzymer till designade nanokatalysatorer
Artikeln går först igenom biokatalysens historia, från tidiga upptäckter av proteinenzymer i jäst och magsafter till ribozymer (katalytisk RNA) och en mängd konstgjorda enzymer byggda av små molekyler och antikroppar. Dessa traditionella katalysatorer är kraftfulla men ofta dyra, instabila och svåra att massproducera. I början av 2000‑talet upptäckte forskare att vissa nanomaterial – till exempel järnoxidnanopartiklar – kunde efterlikna beteendet hos klassiska enzymer som pepparrotspersoxidas. Detta ledde till begreppet nanozymers: nanometerstora partiklar vars egen struktur ger dem enzymlik aktivitet, snarare än att aktiviteten kommer från fästa proteiner eller småmolekylära katalysatorer.
Vad som skiljer nanozymers åt
Till skillnad från enzymer, som har ett enda, noggrant format aktivt fack, exponerar nanozymers många aktiva punkter över sina ytor. Dessa punkter kan sitta vid kristallkanter, defekter eller gränsytor mellan två material, och tillsammans kan de omsätta många molekyler samtidigt. En enskild aktiv plats på en nanozymer är vanligtvis mindre effektiv än ett enzyms, men en enda nanopartikel kan hysa tusentals sådana platser, så dess totala katalytiska kraft kan matcha eller överträffa naturliga enzymer. Deras aktivitet kan också justeras genom att ändra storlek, form, kemisk dopning och ytskikt – ungefär som att fintrimma arkitekturen och ledningsdragningen i en liten maskin. Eftersom de är gjorda av robusta fasta material snarare än ömtåliga veckade proteiner fortsätter nanozymers att fungera vid höga temperaturer, låga temperaturer eller höga salthalter som snabbt skulle slå ut de flesta enzymer.
Hur nanozymers fungerar och hur de mäts
Författarna visar att nanozymers ofta följer samma grundläggande kinetiska regler som biokemister använder för enzymer, såsom Michaelis–Menten‑beteende, där reaktionshastigheten beror på hur lätt katalysatorn binder och omvandlar sitt substrat. Men det finns viktiga avvikelser. En partikel kan rymma flera typer av aktiva platser, så en enda nanozymer kan utföra olika reaktioner eller till och med motsägelsefulla sådana, som både att skapa och förstöra reaktiva syreföreningar. Detta kan ge upphov till komplexa "icke‑lärarboksmässiga" kinetiska kurvor som döljer flera processer under en jämn trend. Översikten förklarar hur forskare dissekerar dessa beteenden, uppskattar hur många aktiva platser som verkligen finns och jämför den totala aktiviteten hos olika nanozymers med standardiserade enheter — allt avgörande för att omvandla ett intressant material till ett pålitligt verktyg.
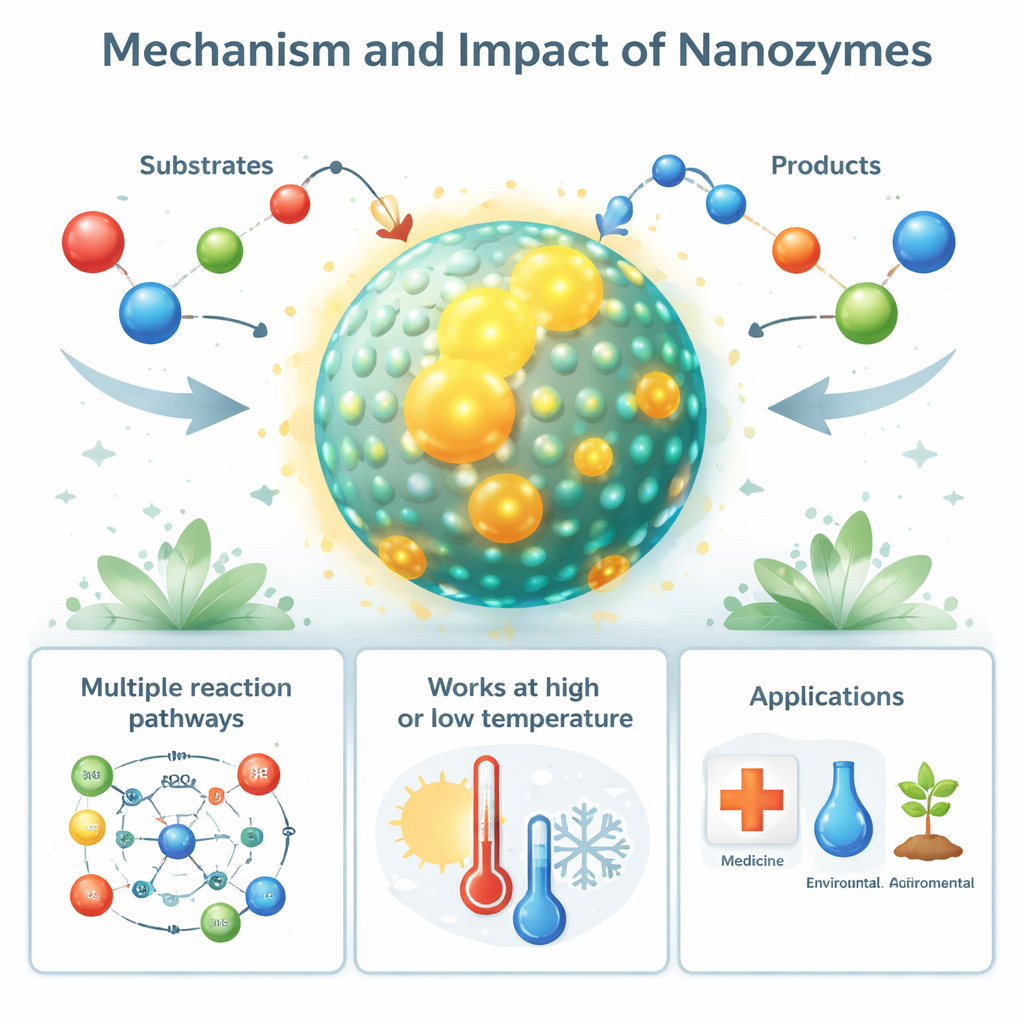
Från naturliga nanozymers till verkliga tillämpningar
Det är anmärkningsvärt att nanozymer‑liknande beteende inte är begränsat till laboratoriet. Vissa biologiska nanostrukturer, såsom järnfyllda proteinkapslar (ferritin) och magnetiska partiklar i bakterier (magnetosomer), fungerar som naturliga nanozymers som hjälper till att kontrollera skadliga reaktiva syreföreningar. Även sjukdomsrelaterade proteinfibrer, som amyloida avlagringar vid Alzheimers sjukdom, kan uppvisa peroxidasliknande nanozymer‑aktivitet som skadar närliggande celler. På den tillämpade sidan används syntetiska nanozymers som billigare, tåligare ersättare för enzymer i diagnostiska tester, biosensorer och industriella analyser. Deras förmåga att antingen generera eller avlägsna reaktiva syreföreningar utnyttjas för att döda tumörceller och bakterier, skydda vävnader från oxidativ stress och hjälpa grödor att motstå torka, salthalt och föroreningar.
Att utforma nästa generationens smarta katalysatorer
Framåt lyfter författarna fram viktiga utmaningar: att lokalisera de exakta atomära strukturer som fungerar som aktiva platser, förbättra reaktionsselektiviteten så att nanozymers agerar endast där och när de önskas, samt säkerställa säkerhet och stabilitet i kroppen. De pekar på avancerad avbildning, kvantnivå‑simulationer och maskininlärning som kraftfulla verktyg för att förutsäga och optimera nanozymers prestanda. Eftersom nanozymers kan fungera i extrema förhållanden, reagera på ljus, värme, ljud eller magnetfält och ibland utföra flera reaktioner i följd, kan de bli grunden för nya terapier, miljötekniker och industriella processer. Översikten avslutas med att nanozymers vidgar själva definitionen av biokatalys och kanske till och med ger ledtrådar om hur primitiva katalysatorer en gång drev kemin i tidigt liv.
Citering: Zhang, R., Yan, X., Gao, L. et al. Nanozymes expanding the boundaries of biocatalysis. Nat Commun 16, 6817 (2025). https://doi.org/10.1038/s41467-025-62063-8
Nyckelord: nanozymers, biokatalys, nanopartiklar, enzymimitat, reaktiva syreföreningar