Clear Sky Science · sv
Nanoporreavkänning av protein- och peptidkonformation för punktvårdsapplikationer
Varför små proteinformer kan förändra din nästa hälsokontroll
När befolkningar åldras blir sjukdomar som Alzheimers, Parkinsons, hjärtsjukdom och cancer allt vanligare. Många av dessa tillstånd börjar när viktiga proteiner och små proteinfragment (peptider) subtilt ändrar sin form långt innan symtomen visar sig. Dagens kliniska tester mäter vanligtvis hur mycket av en biomarkör som finns, inte om dess form är normal eller förvriden. Den här artikeln undersöker en teknik kallad nanoporreavkänning, som elektriskt kan ”känna” formen och kemin hos enskilda proteinmolekyler, och förklarar varför den skulle kunna bli grund för framtida punktvårdstester som körs på minuter i en liten apparat.
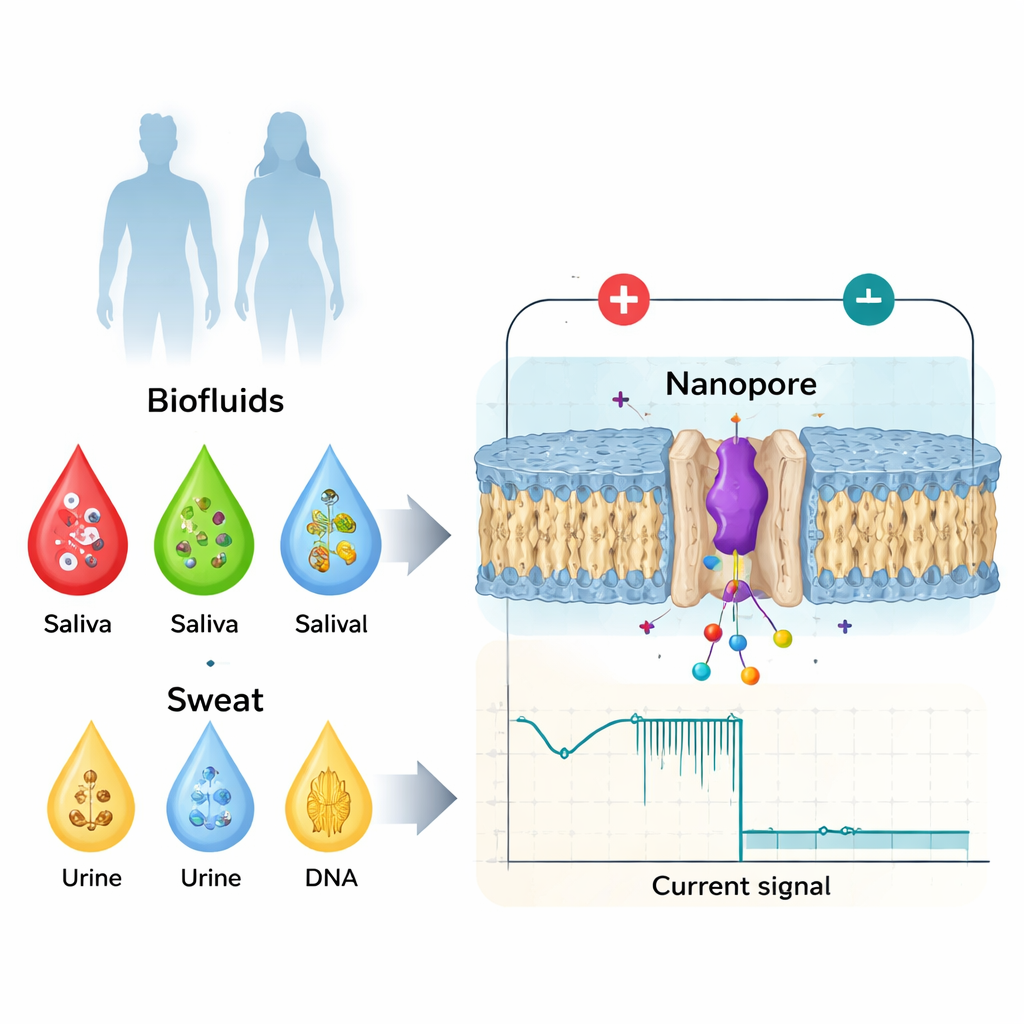
Från enkla blodprover till formmedvetna biomarkörer
Läkare använder redan många biomarkörer från blod, saliv, urin eller svett—såsom proteiner, hormoner eller små molekyler—för att följa hälsa och sjukdom. Traditionellt har fokus legat på grova förändringar: fler kopior av ett protein, skadat DNA eller närvaro av en viralkomponent. Men biologin visar sig vara mer subtil. Samma protein kan slås på eller av av små förändringar i dess struktur, genom kemiska märkningar som läggs till efter syntes, eller genom spegelbildsversioner av dess byggstenar. Dessa små förändringar kan påverka hur ett protein binder partner, bildar klumpar eller för vidare signaler, och är kopplade till blodkoagulationsproblem, neurodegenerativa sjukdomar och cancer. Standardverktyg på sjukhus som massespektrometri, antikroppsbaserade tester och högupplöst avbildning är kraftfulla, men de är dyra, långsamma, kräver högutbildad personal och kan i allmänhet inte användas som snabba, enkla punktvårdsapparater.
Vad en nanoporre gör annorlunda
Nanoporreavkänning vänder problemet upp och ner. Istället för att ta ett medelvärde över biljoner molekyler undersöker den en i sänder när den passerar genom ett litet hål i ett membran som bara är några miljarder delar av en meter brett. En spänning appliceras så att joner flödar genom poren och skapar en stadig elektrisk ström. När ett protein eller en peptid går in i poren blockerar den delvis den strömmen. Djupet av strömfallet, hur länge det varar och de finare detaljerna i dess form beror på molekylens storlek, laddning och konformation (dess tredimensionella veckning). Genom att noggrant utforma poren—antingen med konstruerade proteiner eller med solida material—kan forskare hålla enskilda biomolekyler inkapslade tillräckligt länge för att skapa rika elektriska ”fingeravtryck” som särskiljer inte bara olika proteiner, utan även subtila varianter av samma biomarkör.
Läsa sjukdomsrelevanta förändringar, en molekyl i taget
Översikten framhäver hur nanoporer redan har använts för att lösa medicinskt viktiga skillnader som andra metoder har svårt att se. De kan skilja åt peptider som skiljer sig med endast en aminosyra, upptäcka sjukdomsassocierade varianter av hemoglobin direkt från blod och särskilja korta hormonlika peptider som varierar med bara en byggsten eller till och med med en spegelbildsform av den byggstenen. Nanoporer kan också känna av posttranslationella modifieringar—små kemiska märken som fosfat-, socker- eller sulfatgrupper—som hjälper till att styra om proteiner som är involverade i Alzheimers, Parkinsons, blodkoagulation eller cancer beter sig normalt eller patologiskt. I vissa experiment hålls ett enda enzym eller bindande protein inne i poren, och förändringar i dess elektriska signal avslöjar, i realtid, hur det binder partner eller utför reaktioner, vilket potentiellt kan exponera felaktiga vägar vid sjukdom.
Mot snabba tester vid sängen
Eftersom varje blockeringstillfälle motsvarar en molekyl kan nanopureenheter vara extremt känsliga och detektera så få som tusentals kopior av en biomarkör i en komplex vätska. Författarna diskuterar strategier för att övervinna centrala hinder för klinisk användning: öka hastigheten för infångst av sällsynta molekyler, stabilisera membran eller använda hybridlösningar med både solida och biologiska porer, samt använda maskininlärning för att automatiskt klassificera komplexa elektriska mönster till tydliga diagnostiska kategorier. De visar också hur indirekta metoder—som att fästa DNA-taggar eller bindande partner—kan förstärka svaga signaler eller möjliggöra samtidig mätning av flera biomarkörer, samtidigt som mycket av den konformationella detaljen som gör nanoporer unika bevaras.
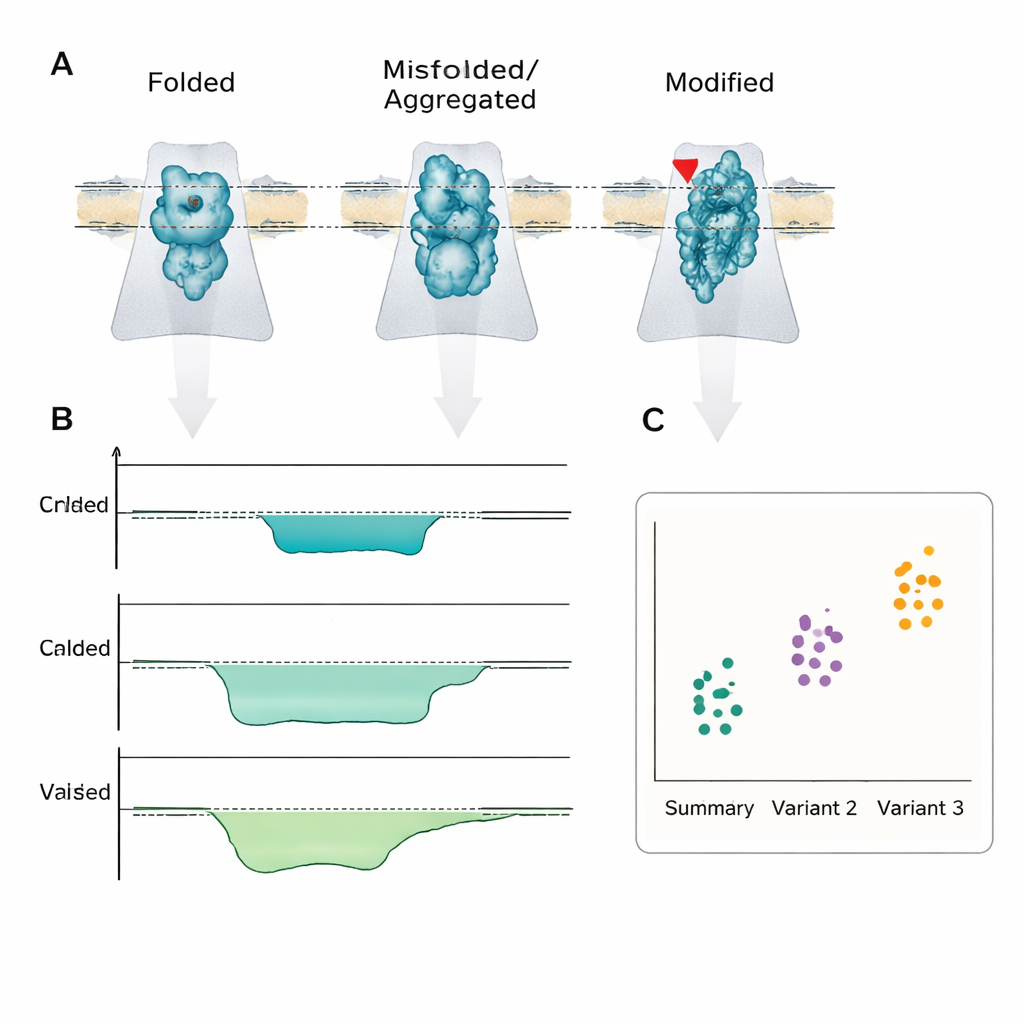
Vad detta kan betyda för patienter
Huvudbudskapet är att sjukdom ofta drivs mindre av hur mycket protein som finns och mer av vilken form eller kemisk version som är närvarande. Nanoporreavkänning är en av få tekniker som direkt kan läsa av dessa skillnader på enskild molekylnivå, tillräckligt snabbt och enkelt för att integreras i bärbara enheter. Även om betydande ingenjörs- och standardiseringsutmaningar kvarstår, menar författarna att, på samma sätt som nanoporre-DNA-sekvenserare har tagit steg in i kliniken, kan nanoporrebaserade sensorer för proteiner och peptider så småningom leverera snabba tester vid sängen som inte bara säger ”något är fel” utan också avslöjar den exakta molekylära felveckningen eller modifieringen bakom en patients tillstånd.
Citering: Ratinho, L., Meyer, N., Greive, S. et al. Nanopore sensing of protein and peptide conformation for point-of-care applications. Nat Commun 16, 3211 (2025). https://doi.org/10.1038/s41467-025-58509-8
Nyckelord: nanoporreavkänning, proteinsignalämnen, punktvårdsdiagnostik, posttranslationella modifieringar, konformationssjukdomar