Clear Sky Science · sv
Att belysa effekten av N-terminal acetylering: från protein till fysiologi
Hur små kemiska märken kan förändra proteiners beteende
Varje cell i din kropp är fylld av proteiner som måste vikas rätt, ta sig till rätt plats, sätta ihop sig till molekylära maskiner och avlägsnas när de är skadade. Denna översiktsartikel undersöker en subtil men mycket vanlig kemisk förändring i ena änden av många proteiner — kallad N-terminal acetylering — och visar hur denna lilla ”mössa” hjälper till att kontrollera allt från celltillväxt och stressresponser till hjärtutveckling och hjärnfunktion.
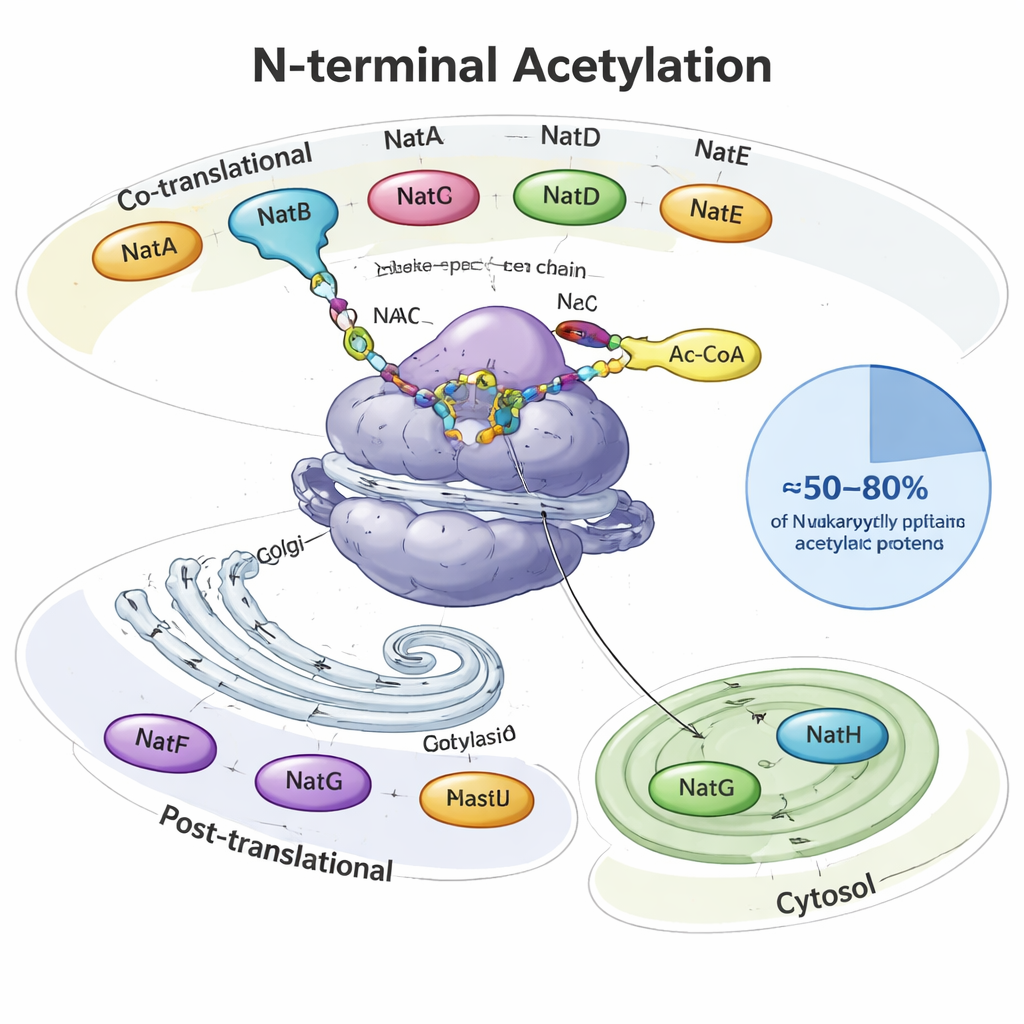
Proteinmössan som de flesta av oss aldrig hört talas om
När ett protein bildas kommer det ut från cellens proteinfabrik, ribosomen, som en växande tråd. I dess allra början — N-terminalen — får många eukaryota proteiner en acetylgrupp, en liten tvåkolig mössa. Specialiserade enzymer kallade N-terminala acetytransferaser (NATs) utför detta arbete och använder en vanlig metabolisk molekyl (acetyl‑CoA) som givare. I jäst, växter och djur delar åtta huvudtyper av NATs (NatA–NatH) upp arbetsuppgifterna. Vissa verkar medan proteinet fortfarande syntetiseras, andra arbetar efteråt och är stationerade på specifika platser som Golgiapparaten eller växtplaster. Tillsammans modifierar de ungefär hälften till fyra‑femtedelar av alla cellulära proteiner, där varje NAT känner igen föredragna startsekvenser av två till fyra aminosyror.
Många enzymer, var och en med sin specialitet
NatA, NatB och NatC är de stora arbetsmyrorna, de verkar direkt vid ribosomen och täcker stora delar av det så kallade ”N-terminala acetyleromet”. Endast NatA kan modifiera omkring 40 % av mänskliga proteiner, vanligtvis de vars första metionin har klippts bort. NatB och NatC verkar på proteiner som behåller sin initiala metionin, men skiljer sig åt i vilka närliggande aminosyror de föredrar. Andra NATs är mer selektiva: NatD fokuserar på bara några histonproteiner som packar DNA, NatF riktar sig mot transmembranproteiner vid Golgi, NatG verkar inne i växtplaster, och NatH (NAA80) slutför en särskild tvåstegs‑mognadsprocess på aktin, en huvudkomponent i cellens skelett. Artikeln sammanför strukturella och biokemiska studier som visar hur hjälpsubenheter förankrar dessa enzymer vid ribosomer eller membran och finjusterar vilka proteiner de verkar på.
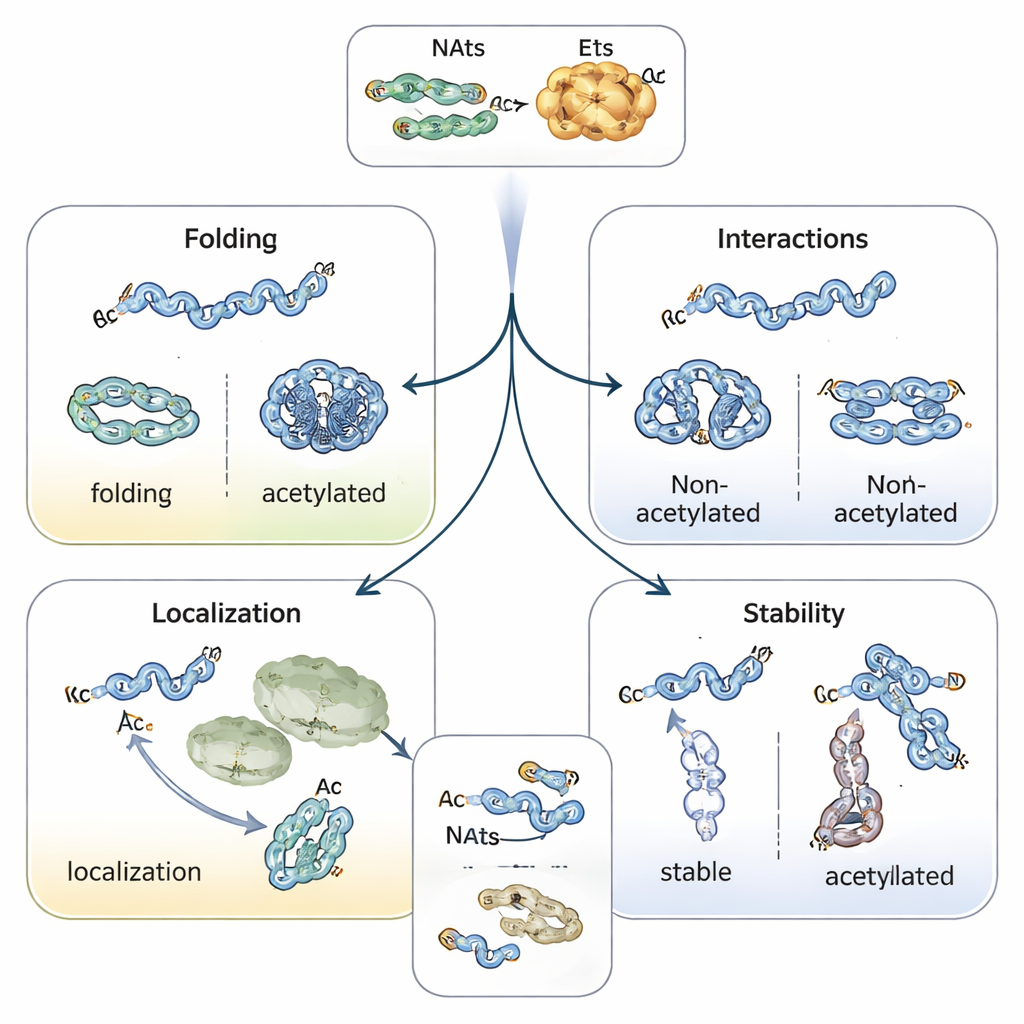
Styr proteinveckning, plats och livslängd
Tillägg av en acetylmössa förändrar den kemiska naturen hos proteinets början och stabiliserar ofta helixstrukturer och påverkar hur proteiner veckas. Till exempel tenderar det Parkinson‑kopplade proteinet alfa‑synuklein att klumpa sig mindre och anta en säkrare form när dess N‑terminus är acetylerad. Tropomyosin, en partner till aktin, binder och reglerar aktinfilament mycket bättre när det är korrekt acetylerat. Hos växter och djur kan N‑terminal acetylering fungera som en slags adressetikett som hjälper proteiner att hitta till kloroplaster, lysosomer eller Golgi. Kanske mest anmärkningsvärt är dess roll i att bestämma hur länge proteiner överlever: en oprotektad N‑terminus kan läsas som en ”nedbrytningssignal” av ubiquitin‑märkande enzymer, medan acetylering kan dölja den signalen och stabilisera proteinet — eller, i vissa fall, skapa en villkorlig etikett som endast känns igen när proteinet är felveckat eller inte i rätt komplex.
Från cellfysiologi till utveckling och sjukdom
Där N‑terminal acetylering påverkar så många proteiner får störningar i NATs vidsträckta konsekvenser för hela organismer. Att ta bort NatA, NatB eller NatC i modellorganismer orsakar ofta allvarliga utvecklingsfel, förändrade stressresponser eller till och med död, medan mer specialiserade enzymer som NatF och NatH ger snävare problem som hjärnförkalkningar eller hörselnedsättning. Hos människor ligger ärftliga mutationer i flera NAT‑gener bakom sällsynta neuroutvecklingssyndrom med intellektuell funktionsnedsättning, hjärtdefekter eller muskelsvaghet. Samma maskineri är ofta överaktivt i cancer, där förhöjda NAT‑nivåer korrelerar med dålig prognos och kan driva tumörtillväxt, metastasering och terapimotstånd. Förändringar i N‑terminal acetylering påverkar också proteiner som lätt bildar aggregat, såsom alfa‑synuklein och huntingtin, vilket kopplar denna modifiering till mekanismer för neurodegenerativa sjukdomar.
Framtida riktningar och medicinska möjligheter
Författarna drar slutsatsen att även om vi nu känner till de flesta kärnenzym som lägger till dessa N‑terminala mössor, förstår vi fortfarande endast en bråkdel av de specifika proteinmålen och regleringsprinciperna. Ett huvudtema är att acetylering vid proteinets början ofta skyddar det från för tidig nedbrytning, samtidigt som den skapar kontextberoende signaler för kvalitetskontroll. Att kartlägga vilka ubiquitin‑ligaser som läser vilka N‑terminala mönster, och att ta reda på om något enzym kan ta bort dessa mössor, är viktiga öppna frågor. Eftersom NATs sitter i korsningen mellan proteinstabilitet, genreglering och cellens stressresponser, framstår selektiva NAT‑hämmare — och kanske framtida verktyg som finjusterar N‑terminal acetylering av specifika sjukdomsrelaterade proteiner — som lovande vägar för nya behandlingar vid cancer, hjärtsjukdom och neurodegeneration.
Citering: McTiernan, N., Kjosås, I. & Arnesen, T. Illuminating the impact of N-terminal acetylation: from protein to physiology. Nat Commun 16, 703 (2025). https://doi.org/10.1038/s41467-025-55960-5
Nyckelord: proteinmodifiering, N-terminal acetylering, proteinernas kvalitetskontroll, neurodegenerativ sjukdom, cancerbiologi