Clear Sky Science · sv
m6A-RNA-metylering påverkar antiviral respons vid celiaki
När ett virus och gluten går ihop
Celiaki ses ofta som ett enkelt matproblem: ät gluten och tarmen skadas. Denna studie visar en djupare berättelse där en vanlig tarmvirus och en liten kemisk markering på våra RNA-molekyler samarbetar för att driva immunsystemet mot långvarig skada. Att förstå detta dolda kontrollskikt kan hjälpa till att förklara varför bara vissa personer utvecklar celiaki och peka på nya behandlingar som går bortom glutenfri kost. 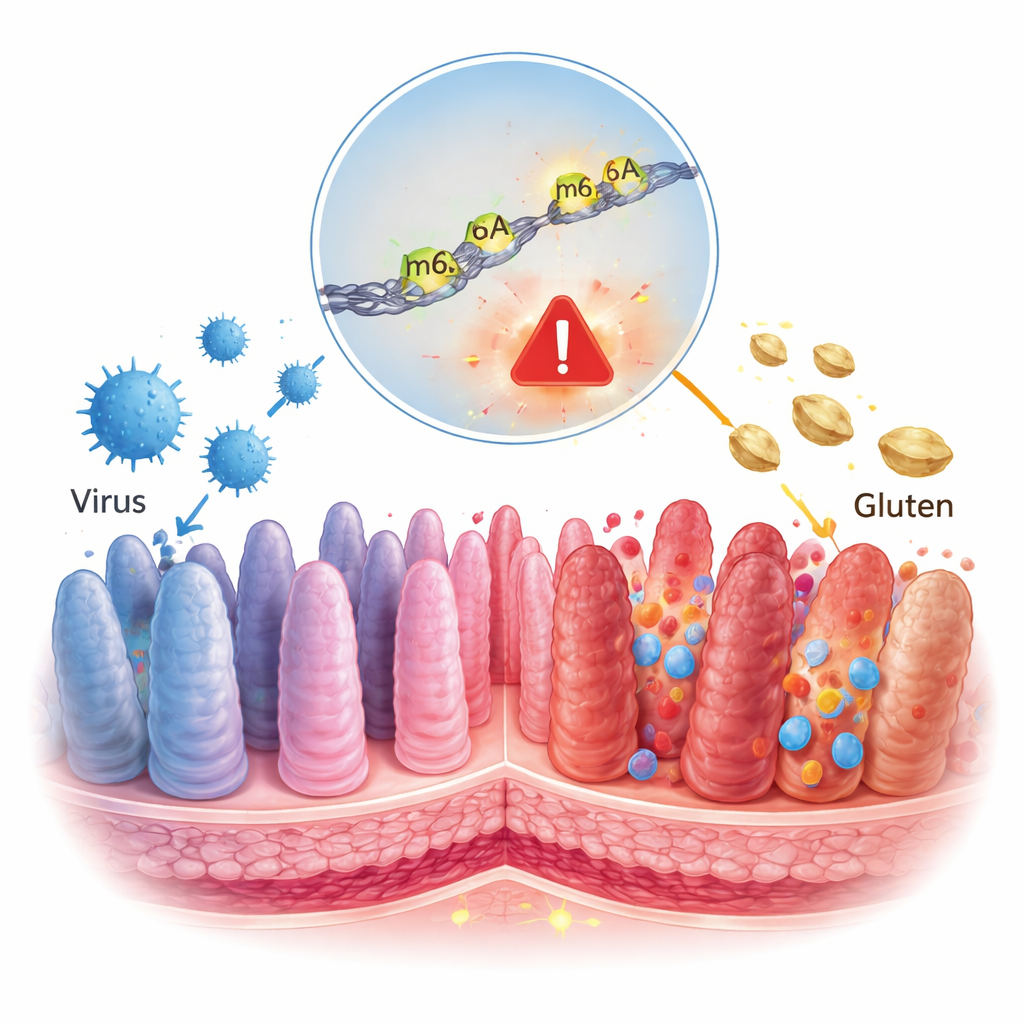
En dold markering på våra genetiska budskap
Våra celler läser ständigt av gener och kopierar dem till RNA, korta ”meddelanden” som säger åt cellen vilka proteiner som ska tillverkas. Dessa meddelanden är inte fasta; de kan dekoreras med kemiska märken som fungerar som markörer och ändrar hur starkt ett budskap läses. En av de vanligaste markeringarna kallas m6A, en liten förändring i RNA-bokstäverna. Virus är kända för att förändra dessa RNA-markeringar i infekterade celler, och tidigare arbete har redan kopplat m6A till hur gluten utlöser inflammation i celiaktarmen. Författarna frågade om en virusdriven förändring i m6A skulle kunna hjälpa till att växla immunsystemet från tolerans mot föda till attack.
Bevis från patienter med celiaki
Forskarna tittade först på blod och tarmbiopsier från personer med aktiv celiaki och från icke-celiaktiska kontroller. De fann att celiakipatienter hade högre nivåer av antikroppar mot reovirus, ett dubbelsträngat RNA-virus som infekterar tarmen, vilket tyder på frekventare eller starkare exponering. I tarmvävnaden hos dessa patienter var viktiga antivirala varningsgener, särskilt en som kallas IRF7, påslagna i högre grad, tillsammans med inflammatoriska molekyler som STAT1 och immuncellsatraktanten CXCL10. Samtidigt var maskineriet som lägger till och läser m6A-markeringar mer aktivt och de totala m6A-nivåerna på RNA var högre. Uttrycket av antivirala gener steg och föll i takt med gener relaterade till m6A, vilket antyder att samma kontrollsystem kan driva både virusförsvar och autoimmun skada.
Hur gluten förstärker viruslarmet
För att undersöka orsak och verkan byggde teamet en celiakiliknande modell i tarmceller odlade i laboratoriet. De efterliknade en virusinfektion med syntetiskt dubbelsträngat RNA och tillsatte sedan nedbrutna glutenfragment liknande dem som uppstår i tarmen efter en måltid. Virusmimiken ensam ökade både IRF3 och IRF7, två huvudströmbrytare för antivirala responser. Men när gluten lades till ökade IRF7 kraftigt extra, medan IRF3 inte gjorde det. Forskarna upptäckte att under dessa förhållanden ökade m6A-markeringar på ett specifikt område inom IRF7-RNA, och att detta RNA fysiskt interagerade med ett m6A-skrivande enzym (METTL3) och ett raderande enzym (ALKBH5). Att höja m6A, antingen genom att tillsätta mer METTL3 eller genom att minska ALKBH5, drev IRF7-nivåerna ännu högre, vilket knöt gluten-och-virus-synergien direkt till denna RNA-modifiering. 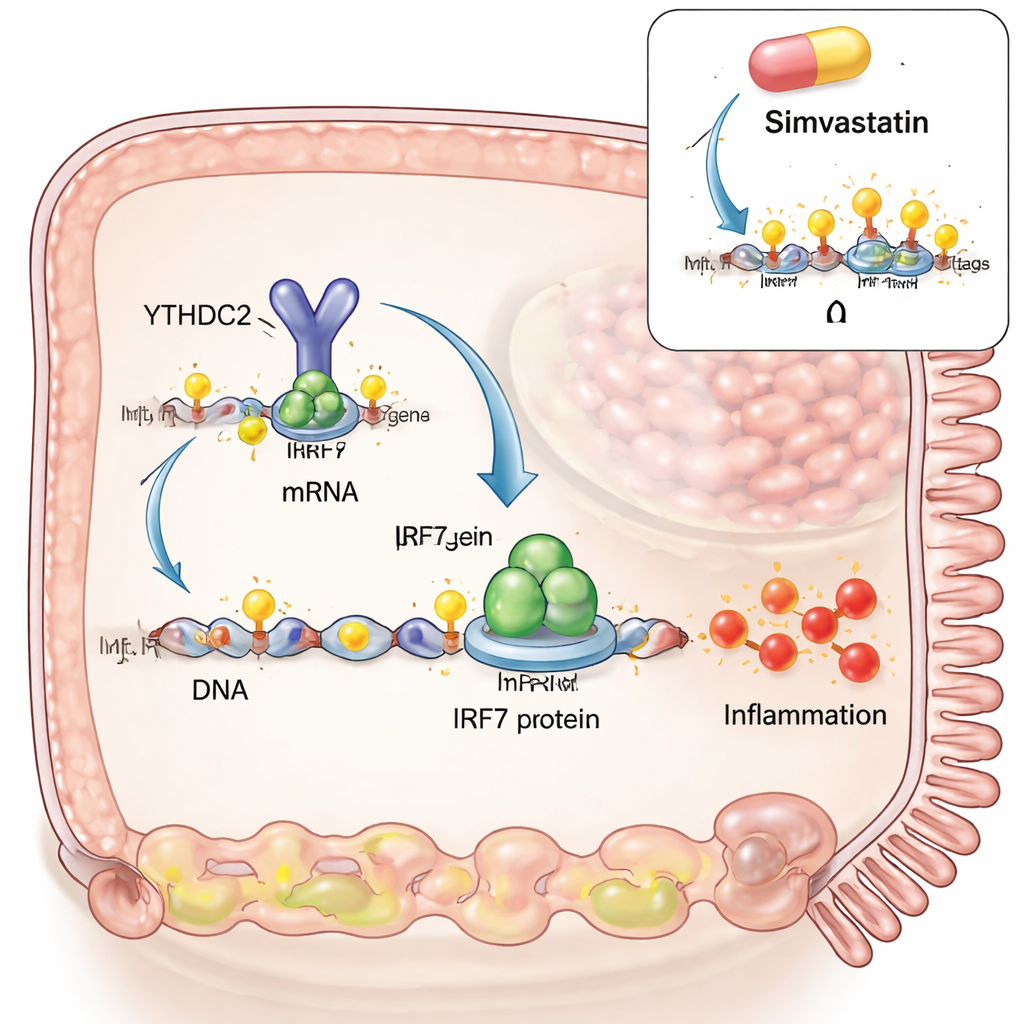
Den molekylära mellanhanden och ett överraskande läkemedel
Nästa steg var att ta reda på hur m6A-markeringar på IRF7-RNA faktiskt ändrar cellens beteende. De konstruerade en version av IRF7-RNA med samma proteinkod men utan m6A-ställen. Detta RNA gav liknande mängder transkript men betydligt mindre IRF7-protein, och det misslyckades med att utlösa nedströms inflammatoriska gener som STAT1 och CXCL10. Den saknade länken var en läsarprotein kallad YTHDC2, som normalt binder m6A inom den proteinkodande regionen och hjälper till att driva effektiv translation till protein. Utan m6A-ställena kunde YTHDC2 inte fästa vid IRF7-RNA. Att blockera m6A-skrivaren METTL3 i cellmodellen minskade IRF7-protein och CXCL10 och dämpade den inflammatoriska utsignalen. Ett kolesterolsänkande läkemedel, simvastatin, som nyligen visats minska m6A i andra vävnader, minskade också m6A på IRF7-RNA, reducerade IRF7-protein i celler och dämpade IRF7-relaterade gener i färska celiakibiopsier odlade ex vivo. Storskaliga jämförelser av genuttryck antydde att simvastatin skjuter celiakivävnad mot ett profil mer likt patienter på glutenfri kost.
Vad detta innebär för personer med celiaki
Arbetet skisserar en bild där ett tarmvirus och gluten samverkar på ett finjusterat lager av RNA-kontroll. Hos känsliga personer verkar virusinfektion öka m6A-taggingen av IRF7-RNA i intestinala celler. Glutenexponering förstärker sedan ytterligare den taggade signalen, vilket leder till mer IRF7-protein, starkare antivirala larm och högre nivåer av inflammatoriska budbärare som bidrar till den autoimmuna attacken på tarmens yta. Genom att dämpa m6A-markeringarna—antingen genetiskt eller med ett läkemedel som simvastatin—kan kedjereaktionen mildras, åtminstone i laboratorie- och ex vivo-modeller. För lekmän är huvudbudskapet att celiaki inte bara handlar om vad du äter, utan också om hur infektioner och subtila kemiska markeringar på RNA formar immunsystemets beslut att tolerera eller angripa. Att rikta in sig på dessa RNA-markeringar skulle en dag kunna komplettera glutenfri kost och inspirera till nya behandlingar för ett bredare spektrum av autoimmuna sjukdomar.
Citering: Sebastian-delaCruz, M., Olazagoitia-Garmendia, A., Pascual-Gonzalez, I. et al. m6A RNA methylation modulates antiviral response in celiac disease. Genes Immun 27, 130–139 (2026). https://doi.org/10.1038/s41435-025-00373-z
Nyckelord: celiaki, RNA-metylering, antiviral immunitet, IRF7, simvastatin