Clear Sky Science · sv
CRISPR-AuNP: fysikokemisk optimering av en guldfokuserad nanopartikelsplattform för kostnadseffektiv och modulär icke-viral genredigering i HSPC
Göra genredigering tillgängligt för fler patienter
Genredigeringsverktyg som CRISPR har redan förändrat livet för personer med ärftliga blodsjukdomar, men behandlingarna är fortfarande dyra, tekniskt krävande och i stor utsträckning begränsade till några få specialiserade center. Den här artikeln beskriver ett nytt sätt att leverera CRISPR till blodbildande stamceller med hjälp av små guldbaserade partiklar som kan blandas på laboratoriebänken på bara ett par timmar. Målet är att göra kraftfulla genredigeringsmetoder enklare, billigare och lättare att använda på fler platser i världen.
Varför blodstamceller är viktiga
Blodbildande stam- och progenitorceller finns i benmärgen och fyller kontinuerligt på alla kroppens olika blodcellstyper. Om läkare kan säkert åtgärda sjukdomsframkallande mutationer i dessa celler kan en engångsbehandling ge ett livslångt botemedel för tillstånd som sickelcellanemi och vissa immundefekter. Idag förlitar sig den vanligaste metoden för att få CRISPR in i dessa celler på elektroporering, en process som använder elektriska pulser för att skapa öppningar i cellmembran. Trots att den är effektiv är elektroporering hård mot cellerna, kräver dyr utrustning och specialreagenser och är inte lätt att skala upp eller exportera till resurssvaga miljöer. Säkerare virala vektorer är utmärkta för många genbehandlingar, men de är mindre lämpade för CRISPR-leverans eftersom de fortsätter producera redigeringsverktyg för länge, vilket ökar risken för off-target-förändringar.
Bygga ett mikroskopiskt guldtransportmedel
Forskarna satte som mål att förbättra ett tidigare rapporterat system med guldnanopartiklar som bar CRISPR-komponenter på ytan. I tidigare konstruktioner förankrades den RNA som styr CRISPR-klippproteinet direkt på guldkärnan och parade sedan detta med Cas9-proteinet. Detta fungerade relativt bra för en typ av CRISPR-enzym men presterade dåligt med Cas9, som är centralt i många terapeutiska strategier. Genom att noga studera hur Cas9 och dess styrande RNA beter sig under de syralika förhållanden som används vid partikelsammanfogning upptäckte teamet att guida-RNA-duplexet blev instabilt på guldytan, vilket ledde till att lite eller inget aktivt Cas9 fäste vid partikeln. Konfokal mikroskopi antydde också att den polymerbeläggning som skulle hjälpa partiklarna att ta sig ut ur cellulära fack skalades av innan den hann göra sitt jobb.
Stegvis omdesign av plattformen
För att övervinna dessa problem byggde forskarna om systemet från grunden i tre etapper. Först, i stället för att förankra bar RNA på guldet och sedan tillsätta protein, bildade de kompletta CRISPR-ribonukleoproteinkomplex (protein plus styr-RNA) innan de förde dem i kontakt med guldytan. De identifierade ett svagt surt tillstånd som tillät dessa komplex att binda partiklarna samtidigt som klippenzymet förblev aktivt. Därefter täckte de de lastade partiklarna med specialdesignade polymerer som kombinerade positivt laddade kedjor—nödvändiga för att undkomma cellulära fack—med flexibla, vattenälskande polyetylenglykolsegment som förhindrar aggregering. Genom att mäta storlek, ytladdning och proteininnehåll visade de att de reproducerbart kunde lasta dussintals CRISPR-komplex per partikel samtidigt som stabiliteten i lösning bibehölls.
Knäcka cellens försvar
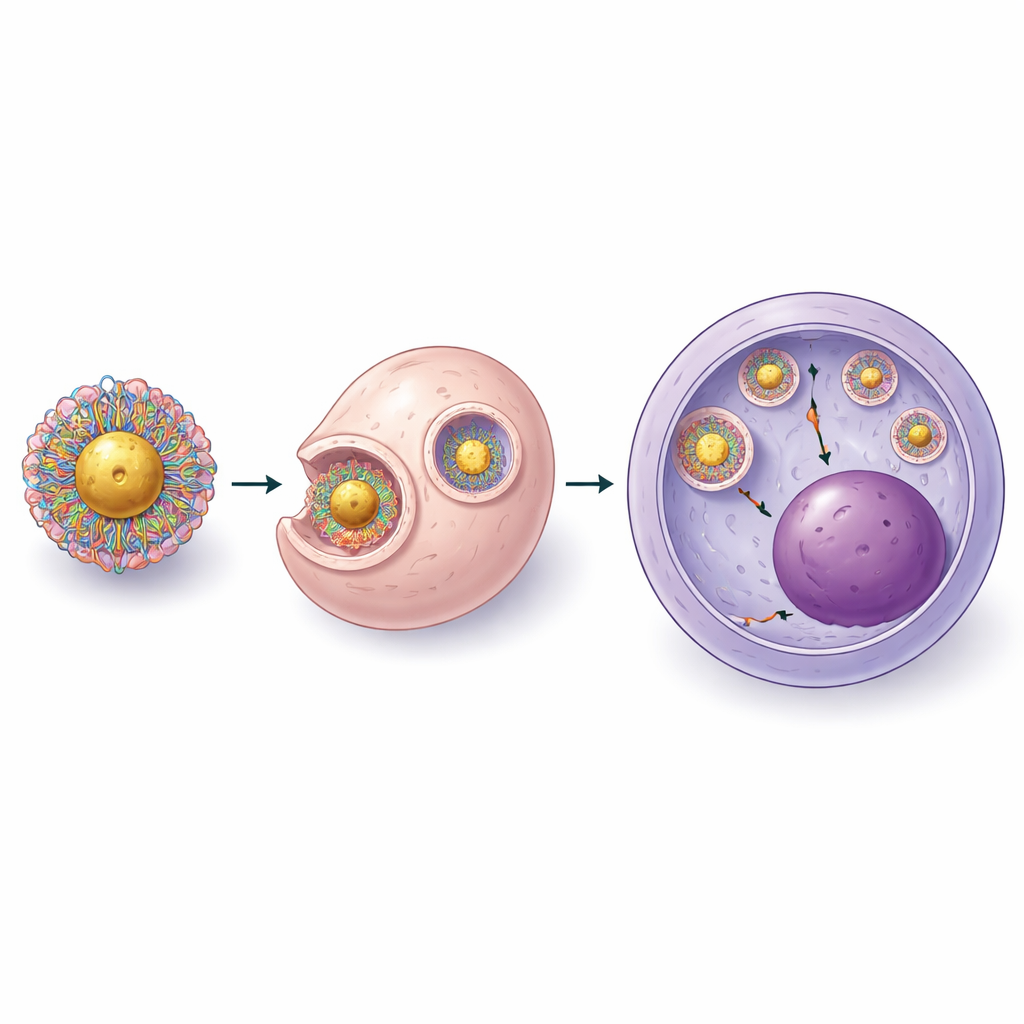
Även med bättre lastning stod den andra generations partiklar fortfarande inför ett centralt hinder: att få CRISPR ut ur cellens interna vesiklar och in i den del av cellen där DNA finns. Teamet finjusterade därför systematiskt kemin i polymerlagret och förhållandet mellan positiva grupper på polymeren och negativa grupper på CRISPR-komplexet. De upptäckte att tillskott av fler korta polyetylenglykolkedjor och ett kontrollerat antal svavelinnehållande ankare förbättrade både partikelstabilitet och förmågan att störa endosomala membran utan att skada cellerna. I den slutliga, tredje generationens design skapade de först kompakta komplex av CRISPR och polymer och fäste sedan dessa på koncentrerade guldkärnor. Elektronmikroskopi visade ett tunt skal av CRISPR och polymer runt varje guldsfär, och avbildning i levande stamceller bekräftade att lasten kunde ta sig ut i cellens inre och nå cellkärnan.
Redigeringsresultat med flera CRISPR-verktyg
För att pröva hur väl de optimerade partiklarna fungerade riktade forskarna in sig på en gen som kallas beta-2-mikroglobulin, som producerar ett protein som finns på ytan av nästan alla blodceller och som lätt kan mätas med flödescytometri. Med hjälp av deras tredjegenerationens guldbaserade plattform uppnådde de mer än 10 % precisa störningar i denna gen i primära mänskliga blodstam- och progenitorceller—nivåer som anses meningsfulla för många terapeutiska tillämpningar—samtidigt som hög cellöverlevnad bibehölls. Även om denna effektivitet är lägre än vad som kan uppnås med elektroporering krävde guldsystemet ingen specialutrustning och orsakade minimal stress för cellerna. Viktigt är att samma plattform kunde användas med olika CRISPR-proteiner, inklusive Cas9, Cas12a och ett nyare enzym kallat Cas12a-M29-1, med liknande redigeringsnivåer och ingen upptäckbar toxicitet, vilket understryker designens modulära natur.
Vad detta kan innebära för framtida terapier
Enkelt uttryckt visar detta arbete att det är möjligt att bygga en liten, omsorgsfullt konstruerad guldbaserad bärare som kan föra CRISPR-verktyg in i känsliga blodstamceller utan elektricitet eller virus, med färdigmaterial för under sjuttio dollar per miljon celler. Medan ytterligare förbättringar krävs för att matcha effektiviteten hos dagens bästa kliniska metoder, särskilt för sjukdomar som kräver mycket höga nivåer av korrigerade celler, sänker denna bänkmonterade plattform praktiska hinder för att utföra sofistikerad genredigering. Med fortsatt förfining och säkerhetstestning kan sådana nanopartiklar bidra till att sprida fördelarna med CRISPR-baserade terapier bortom specialcentra och göra botande behandlingar mer tillgängliga för patienter världen över.
Citering: Gottimukkala, K.S.V., Lane, D.D., Cunningham, R. et al. CRISPR-AuNP: physicochemical optimization of a gold nanoparticle platform for cost-effective and modular non-viral gene editing in HSPCs. Gene Ther 33, 188–202 (2026). https://doi.org/10.1038/s41434-025-00591-0
Nyckelord: CRISPR genredigering, guldnanopartiklar, hematopoetiska stamceller, icke-viral leverans, nanomedicin