Clear Sky Science · sv
Omprövad genomik för facioscapulohumeral muskeldystrofi i telomer-till-telomer-eran: fallgropar i det dolda landskapet av D4Z4-repeats
Varför den här muskelsjukdomsberättelsen spelar roll
Facioscapulohumeral muskeldystrofi (FSHD) är en av de vanligaste ärftliga muskelförtviningssjukdomarna och försvagar ofta ansikts- och skuldermusklerna hos i övrigt unga, friska vuxna. I åratal har forskare fokuserat på en enda DNA-sträcka nära spetsen av kromosom 4 som boven. Denna nya studie visar att bilden är mycket mer komplicerad: liknande DNA-repeats är utspridda över genomet, och många standardlaboratorietester kan inte skilja dem åt. Att förstå detta dolda landskap är avgörande för korrekt diagnostik, bättre forskning och i slutändan säkrare behandlingar.
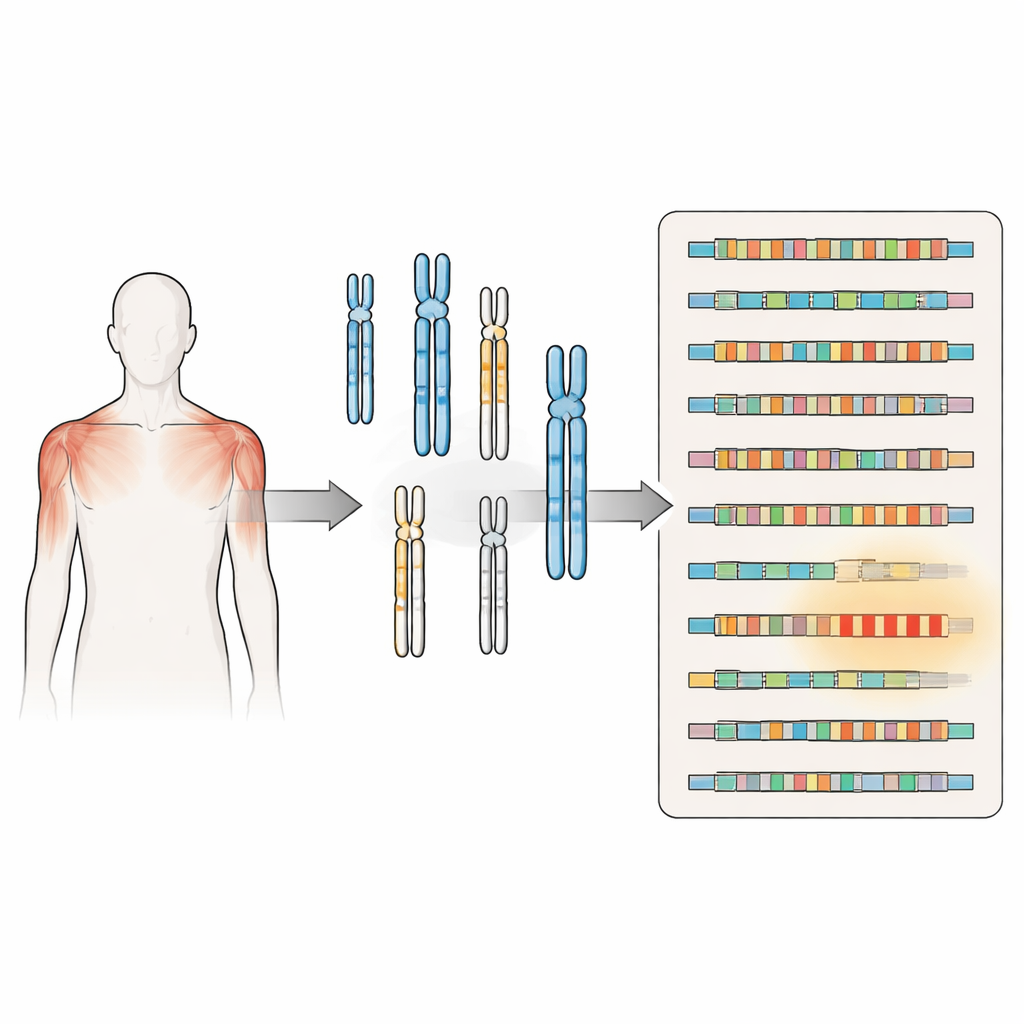
Närmare granskning av en förbryllande muskelsjukdom
FSHD har länge kopplats till förkortning av en upprepad DNA-sekvens kallad D4Z4 nära änden av kromosom 4. När detta repeatområde krymper under en viss storlek och befinner sig på en särskild genetisk bakgrund, tillåts produktionen av ett protein kallat DUX4, vilket kan skada muskelceller. En andra form av sjukdomen uppstår när gener som normalt håller detta område tätt packat och tyst är muterade, vilket återigen tillåter DUX4 att förekomma. Båda vägarna konvergerar på samma problem: en gen som i huvudsak borde vara avstängd i vuxen muskel blir sporadiskt aktiv och bidrar till muskelsvaghet och förtvinning.
Dolda repeats över hela genomet
Tidigare människogenomkartor var ofullständiga, särskilt i regioner rika på repetitivt DNA vid kromosomändar och nära centromerer. Med den nya telomer-till-telomer-människogenomsekvensen, som fyller igen dessa luckor, genomsökte författarna hela genomet med D4Z4-sekvensen från kromosom 4 som sökmall. De upptäckte kluster och isolerade kopior av D4Z4-liknande repeats på minst tio ytterligare kromosomer. Vissa av dessa repeats är strukturellt kompletta och sitter intill signaler som skulle kunna stabilisera DUX4-liknande RNA, vilket tyder på att de under rätt förhållanden kan producera besläktade proteiner eller RNA-molekyler.
När labbtester ser mer än ett ställe samtidigt
FSHD-forskning och diagnostik bygger ofta på tester som amplifierar specifika DNA- eller RNA-fragment med korta primersekvenser, en strategi känd som PCR. Dessa primers designades ursprungligen utifrån antagandet att D4Z4-repeats endast fanns på kromosomerna 4 och 10. Genom att kombinera datorbaserade prediktioner med experiment på celler som bär enskilda mänskliga kromosomer visar författarna att många allmänt använda primers inte bara binder till den sjukdomsassocierade regionen på kromosom 4, utan även till liknande repeats utspridda i genomet. Primers riktade mot huvud-DUX4-exonen eller intilliggande långa icke-kodande RNA amplifierar ofta produkter från flera kromosomer samtidigt, vilket gör det omöjligt att veta var en given signal faktiskt härstammar från.
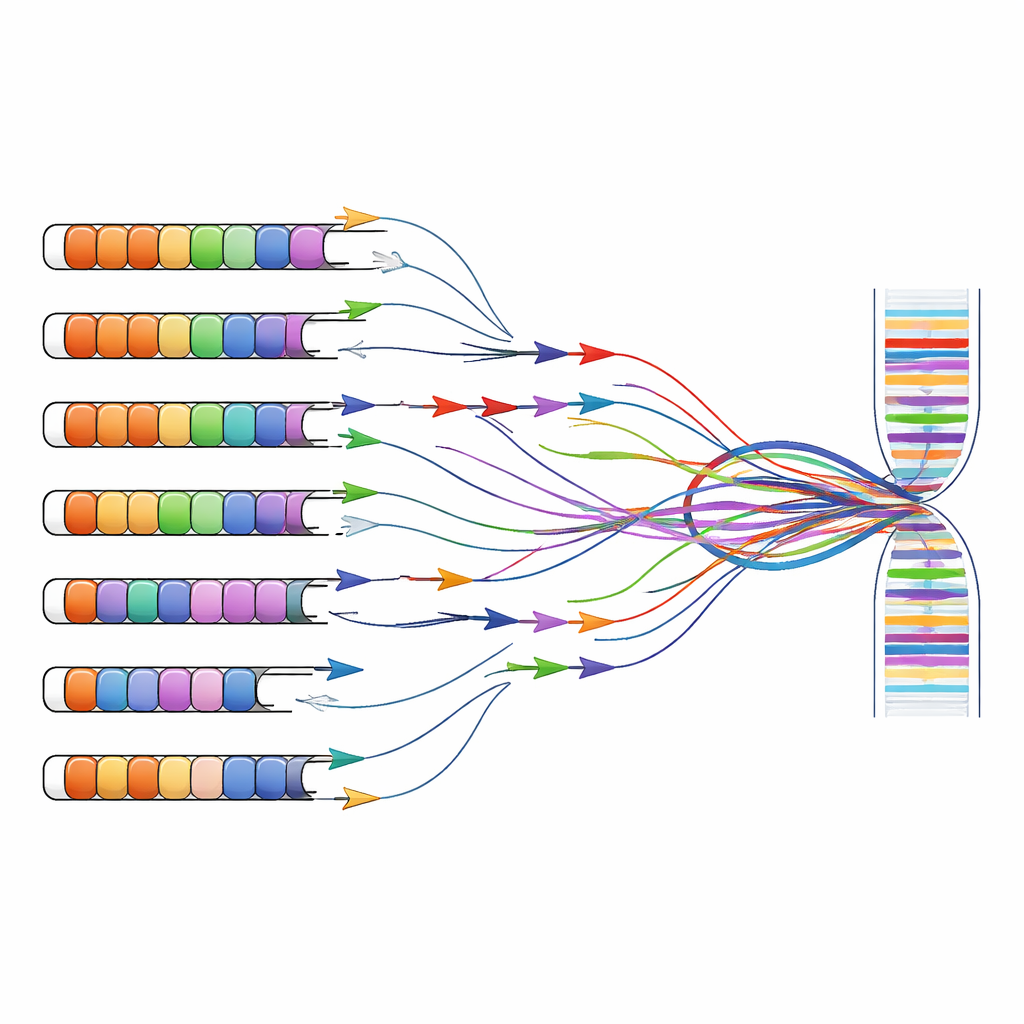
Omprövning av diagnostiska och forskningsverktyg
Detta multiplatsproblem sträcker sig bortom grundforskningen och in i kliniken. Nyare tester som mäter DNA-metylering (en kemisk markör kopplad till geninaktivering) eller använder kortläsningssekvensering tenderar ofta att slå ihop signaler från många nästan identiska repeats. Som en följd kan mätningar av “D4Z4-metylering” eller “DUX4-transkript” i publika dataset faktiskt avspegla en blandning av bidrag från kromosom 4, kromosom 10 och andra platser. Författarna hävdar att för att korrekt koppla genetiska förändringar till symptom måste forskare nu anta repeat-medvetna metoder som särskiljer individuella locus — till exempel långläsningssekvensering som kan spänna över hela repeatblock och fånga deras metyleringsmönster och RNA-produkter i sin helhet.
Vad detta innebär för patienter och framtida terapier
Studien kullkastar inte den centrala rollen för den förkortade D4Z4-regionen på kromosom 4 i FSHD, men visar att denna region lever i ett trångt grannskap av liknande sekvenser. Signaler som tidigare antogs bevisa aktivitet vid sjukdomslocus kan i själva verket delvis komma från dess genomiska kusiner. För patienter innebär detta att de mest pålitliga diagnostiska verktygen blir de som fysiskt kan urskilja exakt vilken kromosom och vilket repeat-array som är involverat, snarare än att förlita sig enbart på indirekta avläsningar. För forskare och läkemedelsutvecklare framhäver det behovet av mycket specifika designval som undviker att oavsiktligt rikta in sig mot ofarliga repeats någon annanstans i genomet. I telomer-till-telomer-eran kommer förståelse och behandling av FSHD att bero på att se hela repeatlandskapet, inte bara ett enda landmärke.
Citering: Salsi, V., Losi, F., Pini, S. et al. Rethinking genomics of facioscapulohumeral muscular dystrophy in the telomere-to-telomere era: pitfalls in the hidden landscape of D4Z4 repeats. Eur J Hum Genet 34, 357–367 (2026). https://doi.org/10.1038/s41431-025-02000-x
Nyckelord: facioscapulohumeral muskeldystrofi, D4Z4-repeats, DUX4, telomer-till-telomer-genom, genetisk diagnostik