Clear Sky Science · sv
Artificiella chaperoner: från konventionella konstruktioner till smarta system
Hjälpmolekyler som får proteiner att vika sig rätt
Inne i varje levande cell måste långa kedjor av proteiner och genetiskt material böja sig och vrida sig till precis rätt former för att fungera korrekt. När de felviks kan de klumpa ihop sig, förlora sina funktioner och till och med utlösa sjukdomar som neurodegenerativa tillstånd. Naturen förlitar sig på ”chaperon”-molekyler för att hålla ordning i detta mikroskopiska kaos, men dessa naturliga hjälpare är dyra, känsliga och svåra att använda utanför celler. Denna artikel undersöker hur forskare nu bygger artificiella chaperoner—konstruerade hjälpmedel som kan övertala vilsna molekyler att återgå till rätt form och som till och med kan slås av och på som smarta verktyg.
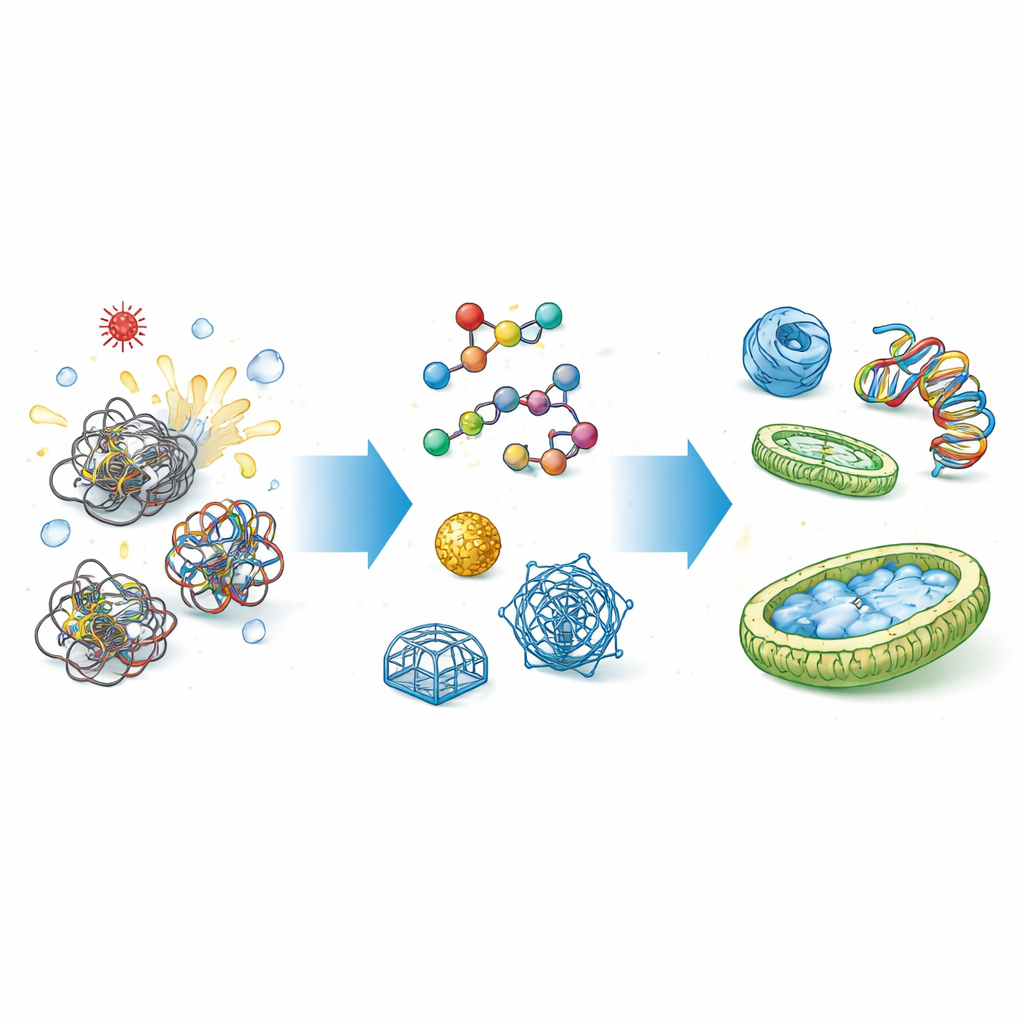
Varför celler behöver vikningshjälpare
Proteiner och nukleinsyror (som DNA och RNA) föds inte färdiga; de måste vikas till intrikata tredimensionella former. Vägen till dessa former är fylld av fallgropar där kedjor kan fastna eller fastna i varandra. Naturliga chaperoner, såsom värmechockproteiner, griper tag i dessa sladdriga kedjor, skärmar deras klibbiga partier och ger dem ett skyddat utrymme för att vikas korrekt. Liknande vägledande roller finns för nukleinsyror, där chaperoner hjälper till att reda ut knutar och omorganisera baspar. När denna kontroll brister kan resultatet bli förlorad funktion, toxiska klumpar, sjukdom och kostsamma misslyckanden i industriell proteinproduktion.
Från enkla kemikalier till designade polymerer
De första artificiella chaperonerna var relativt enkla kemikalier som ändrar hur molekyler upplever sin omgivning. Vissa lösningsmedel och tensider kan dölja klibbiga regioner på proteiner, förhindra aggregering och ge dem en ny chans att veckas om. Vissa små fettsyror hjälper till exempel muterat kollagen att veckas mer korrekt och lindrar stress i celler som påverkas av ärftliga sjukdomar. Men dessa kemiska hjälpmedel måste vanligtvis tillsättas i höga doser, är svåra att skräddarsy för specifika mål och kan störa andra komponenter i komplexa blandningar. För att få större kontroll vände sig forskare till större, specialtillverkade polymerer—flexibla kedjor som kan dekoreras med laddade eller vattenälskande grenar för att mer selektivt vagga DNA, RNA och proteiner.
Polymer‑ och nanogelverktyg
Designerpolymerer kan fästa vid laddade ryggrader på DNA eller exponerade fläckar på proteiner och jämna ut energilandskapet så att dessa molekyler hittar sina föredragna former snabbare och mer pålitligt. För nukleinsyror kan katjoniska (positivt laddade) polymerer neutralisera repulsion mellan strängar, påskynda basparning, strandutbyte och bildandet av exotiska strukturer som används i DNA‑beräkning och biosensorer. För proteiner kan polymerer såsom specialformade polyetylenglykol‑loopar eller syntetiska polyanjoner överträffa vissa naturliga chaperoner vid förebyggande av värmeinducerad aggregering. Andra system parar flexibla chaperonpolymerer med korta peptider för att remodelera cell‑lika membraner till platta nanoblad eller vesiklar, och skapar reversibla tvådimensionella plattformar för lastleverans och vävnadsteknik.

Att bygga smarta, strömbara chaperoner
Utöver att bara hålla kvar och släppa sina klienter kan moderna artificiella chaperoner nu reagera på sin omgivning. Forskare har byggt nanogeler, nanopartiklar och polymernätverk vars grepp om proteiner hårdnar eller löses upp vid förändringar i surhet, temperatur, ljus eller specifika kemikalier som glukos. Till exempel blir vissa miceller mer hydrofoba vid lätt sur pH och efterliknar naturliga chaperoner genom att fånga hotade proteiner för att sedan släppa dem när pH förändras igen. Temperaturkänsliga polymerer kollapsar eller expanderar när de korsar en tröskel, vilket gör att de kan isolera skadade proteiner vid en temperatur och frigöra omstrukturerade vid en annan. Ljuskänsliga grupper kan användas som molekylära strömbrytare som slår på eller av DNA‑samlingsvägar med en blixt, medan sockerresponsiva partiklar kan skydda ett terapeutiskt hormon för att sedan frisätta det i första hand när blodsockret är högt.
Vad detta betyder för medicin och teknik
Artikeln drar slutsatsen att artificiella chaperoner utvecklas från enkla kemiska stabilisatorer till högt programmerbara ”molekylära verktyg” som kan känna igen, skydda och omforma många slags biologiska strukturer på begäran. Genom att noggrant balansera attraktiva och repulsiva krafter och genom att koppla in känslighet för signaler som pH, värme, ljus eller mekanisk stress kan dessa system vika målmolekyler på rätt plats och i rätt tid. På sikt skulle sådana smarta hjälpmedel kunna göra industriell proteinproduktion mer effektiv, skärpa biosensorer, driva molekylära datorer och erbjuda nya sätt att angripa sjukdomar kopplade till felvikta proteiner—potentiellt inklusive tillstånd som Alzheimers sjukdom—samtidigt som de efterliknar den subtila kontroll som levande celler redan uppnår.
Citering: Zhang, W., Maruyama, A. Artificial chaperones: from conventional designs to smart systems. NPG Asia Mater 18, 12 (2026). https://doi.org/10.1038/s41427-026-00640-z
Nyckelord: artificiella chaperoner, proteinfoldning, smarta polymerer, nanomedicin, stimuli‑responsiva material