Clear Sky Science · sv
Att bemästra cuproptos: från metabol omkoppling till terapeutisk utnyttjande vid cancer
När en hjälpsam metall vänder sig mot cancer
Koppar är mest känt som en komponent i elkablar och rördragning, men det löper också tyst genom våra celler och hjälper enzymer att producera energi och skydda oss från skador. Denna översiktsartikel undersöker en överraskande vändning: under rätt villkor kan för mycket koppar driva cancerceller in i en speciell form av död. Att förstå denna process — kallad ”cuproptos” — kan öppna nya möjligheter att behandla tumörer som har överlistat standardterapier.
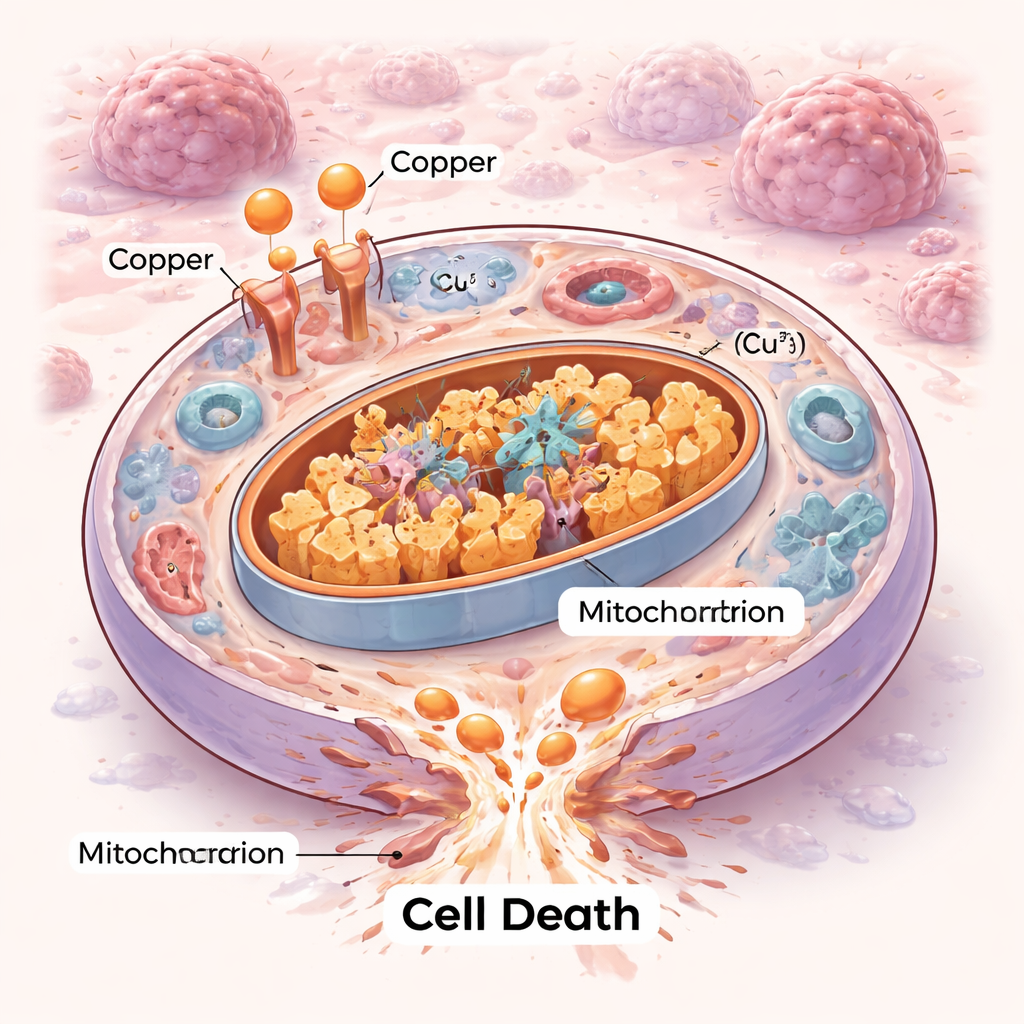
Ett nytt sätt celler kan dö på
Celler dör inte på samma sätt. I årtionden har forskare kartlagt ordnade självdödprogram som apoptos och nyare former som ferroptos. Cuproptos tillför ett nytt kapitel. Här dränks cellens kraftverk — mitokondrierna — i överskott av koppar som binder till specifika metaboliska enzymer som normalt hjälper till att förbränna bränsle. Denna bindning får dessa enzymer att klumpa ihop sig och destabiliserar små järn–svavel‑komponenter som mitokondrierna behöver för att fungera. Resultatet blir ett slags inre trafikstockning och mekaniskt haveri som cellen inte kan reparera, vilket leder till död genom proteotoxisk stress snarare än genom klassiska självmordsvägar.
Hur cancerceller kontrollerar koppar och energi
Eftersom koppar är både nödvändigt och farligt upprätthåller celler ett invecklat logistiskt nätverk för att hantera det säkert. Dedikerade transportörer för in koppar i cellen, chaperonproteiner eskorterar det till mitokondrier och andra destinationer, och lagringsmolekyler som metallotioner och glutation tar hand om överskott. Tumörer omkopplar ofta detta system. Vissa ökar importörer eller chaperoner för att tillgodose sina höga energibehov; andra ökar exportörer eller lagringsproteiner för att undvika kopparöverbelastning. Samtidigt skiftar många cancerformer sin metabolism — växlar mellan yttre sockerförbränning och djupare mitokondriell respiration. Översikten förklarar att cuproptos slår hårdast mot celler som fortfarande är starkt beroende av mitokondrier, vilket gör tumörer med denna metaboliska profil särskilt sårbara.
Huvudströmbrytare som ställer in kopparkänslighet
Stora cellulära ”beslutsfattare” påverkar om cuproptos kan inträffa. Tumörsuppressorn p53 tenderar till exempel att styra celler bort från snabb sockerjäsning mot mer ordnad mitokondriell bränsleanvändning. Genom detta och genom att förändra hanteringen av kopparbindande enzymer kan p53 göra cancer mer mottaglig för kopparinducerad död — medan mutanta former av p53 ofta gör tvärtom. I kontrast hjälper hypoxifaktorn HIF‑1α, som aktiveras i dåligt syresatta tumörcentra, celler att undkomma cuproptos genom att dämpa nyckelmitokondriella enzymer och öka kopparbindande skydd. Andra vägar, såsom Wnt/β‑catenin och AKT, främjar resistens genom att driva kopparexport eller kemiskt modifiera viktiga proteiner så att de inte längre reagerar på kopparöverbelastning. Tillsammans fungerar dessa nätverk som termostater som höjer eller sänker en tumörs känslighet för kopparbaserade behandlingar.
Koppar, immunsystemet och smartare läkemedelsleverans
Kopparns roll begränsar sig inte till att döda cancerceller direkt; den formar också immunlandskapet runt tumörer. Kontrollerad kopparstress kan göra döende cancerceller mer ”synliga” genom att frigöra dangersignaler som rekryterar och aktiverar T‑celler, dendritiska celler och makrofager. Koppar kan också påverka nivåerna av immunkontroller som PD‑L1, vilka tumörer använder för att stänga av antitumör‑T‑celler, vilket pekar på möjligheter att kombinera kopparinriktade läkemedel med moderna immunoterapier. Eftersom fritt koppar kan skada friska vävnader bygger forskare precisionverktyg — små molekylära ionofores som selektivt för handledar koppar in i cancerceller, och nanomedicinska plattformar som packar koppar eller kopparstyrda läkemedel i riktade partiklar eller hydrogel. Dessa teknologier syftar till att höja kopparnivåerna till dödliga nivåer inne i tumörer samtidigt som resten av kroppen hålls inom ett säkert intervall.
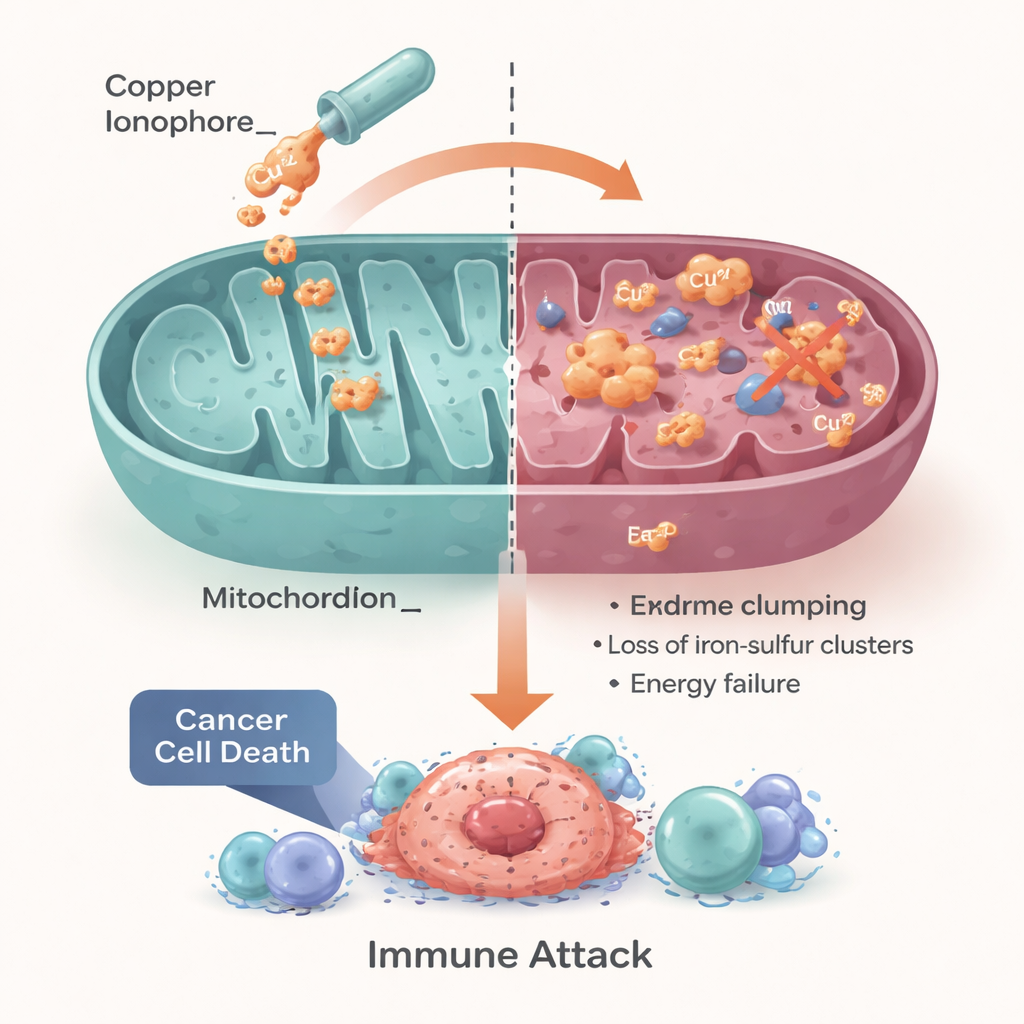
Att vända en cellulär svaghet till en behandling
Författarna slår fast att cuproptos gör ett grundläggande cellulärt behov — noggrann koppar- och energihantering — till ett potentiellt akilleshäl för cancer. Cancerformer med störd kopparhantering eller ett överberoende av mitokondriell metabolism kan vara särskilt känsliga för kopparbaserade strategier, inklusive återanvända läkemedel som disulfiram och elesclomol samt nästa generations nanopartiklar. De betonar dock att framgång kommer att bero på att matcha rätt patienter med rätt angreppssätt, med hjälp av biomarkörer som rapporterar om koppartransportörer, mitokondriell aktivitet samt tumörens immunsvar och syretillstånd. Om dessa hinder kan övervinnas kan utnyttjandet av cuproptos ge onkologer en ny, metalldriven spak för att behandla tumörer som för närvarande har få bra alternativ.
Citering: Hao, Q., Gan, Y. & Zhou, X. Tackling cuproptosis: from metabolic rewiring to therapeutic exploitation in cancer. Cell Mol Immunol 23, 239–260 (2026). https://doi.org/10.1038/s41423-026-01387-x
Nyckelord: cuproptos, kopparmetabolism, cancerbehandling, tumörmetabolism, cancerimmunoterapi