Clear Sky Science · sv
Integrativ spatial profilpipeline för att bestämma TME‑arkitekturer i arkiverade kliniska prov med CmTSA superplex‑teknologi
Varför landskapet runt tumörer som döljs är viktigt
Cancer växer inte i isolation. Den omges av ett livligt grannskap av immunceller, stödjeceller, blodkärl och ärrliknande vävnad som tillsammans bildar tumörens ”mikromiljö”. Denna artikel presenterar ett praktiskt sätt att kartlägga det dolda landskapet i detalj med hjälp av vanliga sjukhusprover. Genom att avslöja vilka typer av celler som sitter intill varandra och hur de organiserar sig i hjälpsamma eller skadliga grannskap kan metoden hjälpa läkare att bättre förutsäga hur en patients cancer kommer att bete sig och vilka behandlingar som sannolikt fungerar.
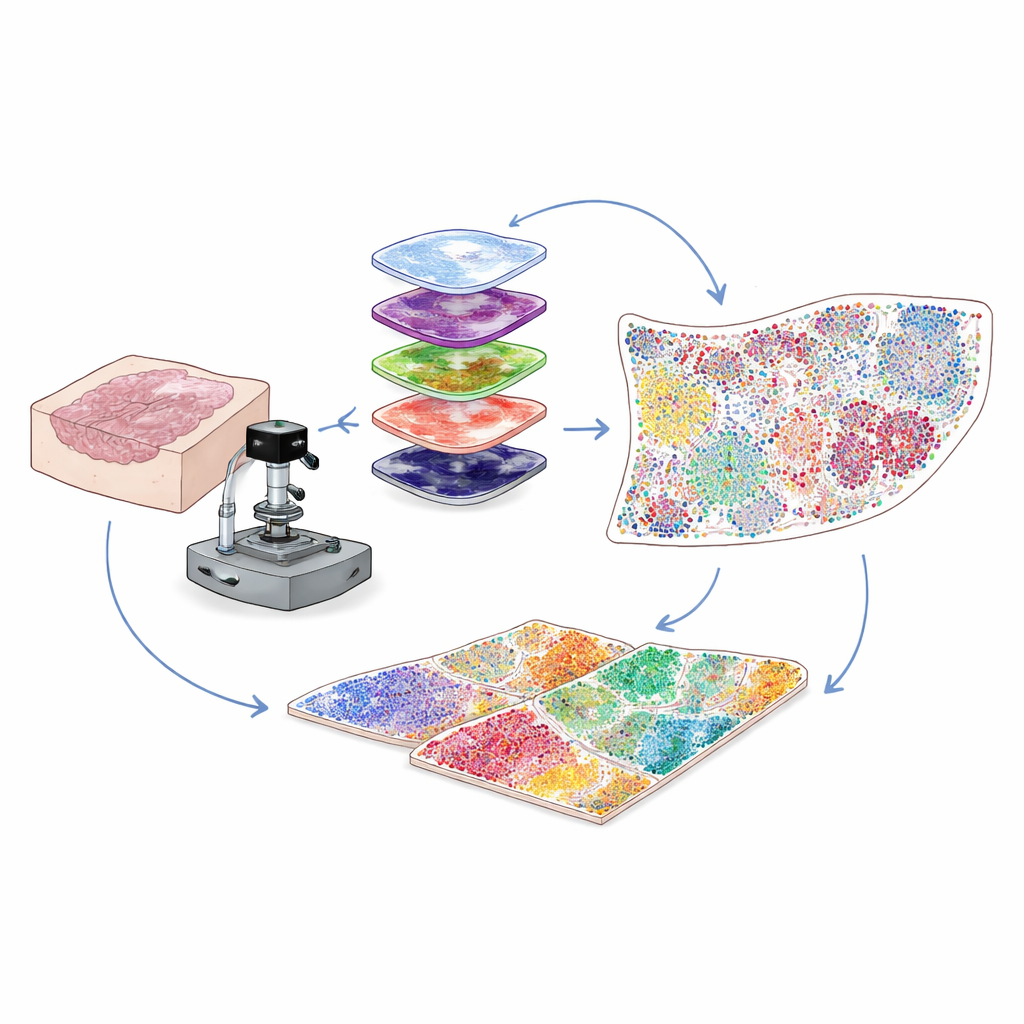
Se mer i vardagliga sjukhusprover
De flesta kliniska cancerprover bevaras som tunna skivor av vaxinbäddad vävnad, kända som FFPE‑block, som kan lagras i åratal. Dessa är en guldgruva för forskning, men ett tekniskt problem har hindrat forskare: sådana prover avger ett naturligt bakgrundsfluorescens som överröstar de svaga signalerna från många viktiga proteiner. Författarna löste detta genom att kombinera intensiv, noggrant avstämd ljusbehandling med en mild kemisk procedur för att selektivt radera den bakgrundslysningen utan att skada vävnaden eller proteintargets. Detta hybrida optiska och kemiska ”bleknings”steg förbättrar bildklarheten markant och gör det möjligt att upptäcka svaga proteinsignaler som annars skulle gå förlorade.
Måla flera dussin proteinetiketter på samma skiva
För att förstå vilka celler som finns och vad de gör färgar forskare vävnader med antikroppar som fäster vid specifika proteiner. Traditionella multiplexmetoder kämpar antingen med svag signal för sällsynta proteiner eller kan bara följa ett begränsat antal markörer åt gången. Här använder teamet en metod kallad cyklisk tyramid‑signalamplifiering. I varje rond färgas en liten uppsättning markörer och enzymatiskt ”utvecklas” till starka, permanent bundna fluorescerande fläckar. Antikropparna avlägsnas sedan försiktigt medan signalen kvarstår, bakgrunden bleks på nytt och nästa uppsättning markörer tillsätts. Genom att upprepa denna cykel många gånger och alignera bilderna med hjälp av den konstanta signalen från cellkärnorna kan man tillförlitligt visualisera 30 till 60 olika proteiner på en enda vävnadsskiva, över ett helt objektglas, med upplösning på enskild cellnivå.
Förvandla färgrika bilder till en cell‑för‑cell‑atlas
High‑plex‑bilder innehåller miljontals pixlar, långt mer än vad ett mänskligt öga kan analysera. Författarna bygger därför en datorvisionspipeline som först hittar och konturerar varje cellkärna med hjälp av djupinlärningsverktyg ursprungligen utvecklade för generell cellsegmentering. Sedan, beroende på var varje proteins fluorescens uppträder — på membranet, i cytoplasman eller i kärnan — och utifrån uppsättningar logiska regler, tilldelas varje cell en typ eller subtype, såsom tumörcell, hjälpar‑T‑cell, cytotoxisk T‑cell, B‑cell, fibroblast eller andra. Utdata är en digital tabell som för varje cell på objektglaset listar dess identitet och dess exakta koordinater. Detta förvandlar en komplex bild till en kvantitativ karta över vem som finns var inom tumörmikromiljön.
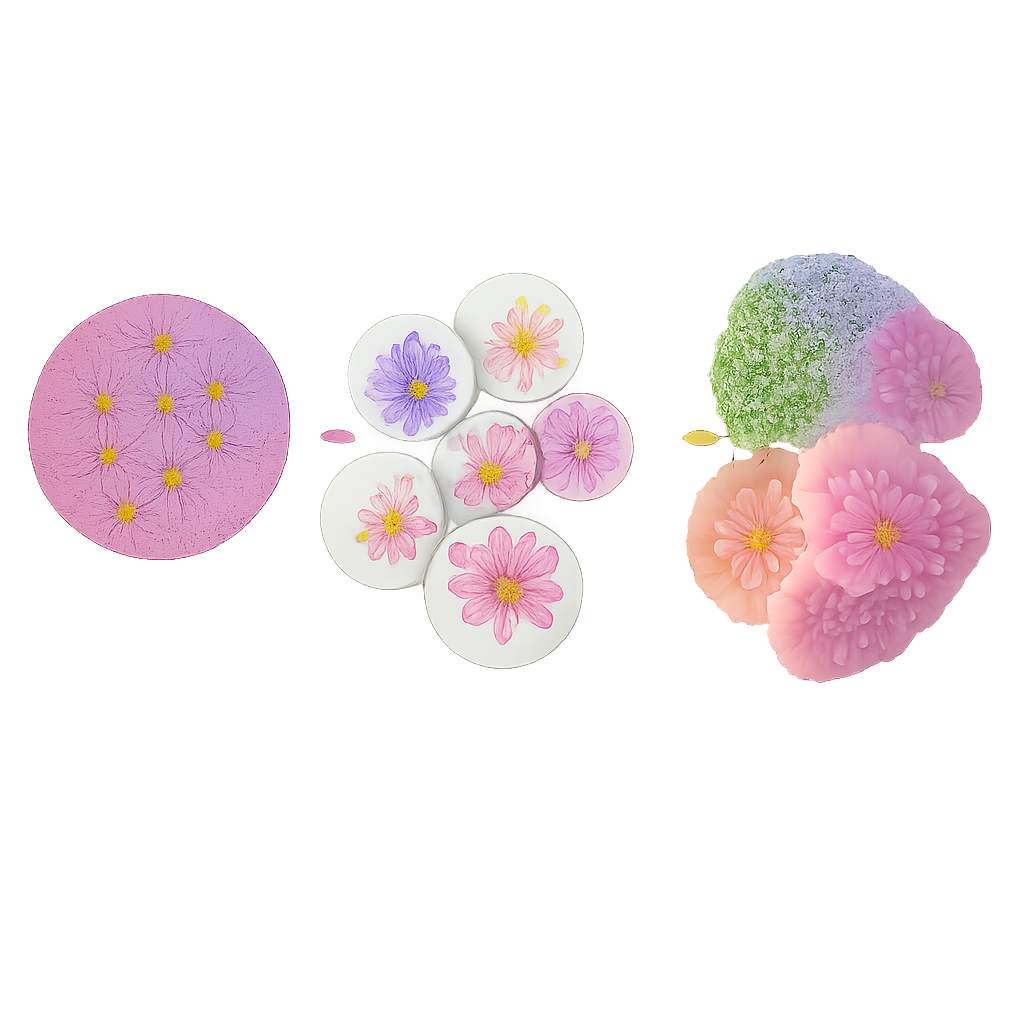
Avslöja cellulära grannskap som formar utfall
Celler agerar sällan ensamma; det som spelar roll är vilka grannar de har. För att fånga detta testar forskarna olika sätt att definiera lokala grannskap runt varje cell och landar i en radie‑baserad nätverksmetod. Föreställ dig att du ritar en liten cirkel — ungefär tjockleken av ett människohår — runt varje cell och listar vilka som finns inuti den. Genom att gruppera celler vars omgivande cirklar har liknande blandningar av grannar identifierar metoden återkommande ”funktionella nischer”, såsom immunrika zoner, fibroblasttäta barriärer eller tumördominerade regioner. Att tillämpa denna strategi på kolonvävnad visar att radie‑baserade grannskap stämmer bättre överens med kända anatomiska strukturer än alternativa metoder. I livmoderhalscancerprover från patienter med god respektive dålig prognos finner teamet att immuncellsrika nischer klustrar vid tumörkanten hos patienter som klarar sig väl, medan patienter med sämre utfall visar tjocka fibroblasttäta zoner som omsluter tumörceller och verkar avskärma angripande immunceller.
Från spatiala kartor till skräddarsydd behandling
Genom att kombinera högkvalitativ, prisvärd färgning av många proteiner med robust bildanalys levererar detta arbete en änd‑till‑änd‑pipeline som kan tillämpas på stora mängder vanliga sjukhusprover. Metoden förvandlar bevarad vävnad till detaljerade kartor över hur tumör-, immun‑ och stromaceller arrangerar sig och interagerar. För allmänheten är slutsatsen att det inte bara är celltyperna utan även deras precisa grannskapsmönster som påverkar hur en cancer beter sig. Denna plattform kan hjälpa forskare att lokalisera skyddande immunhotspots, identifiera suppressiva cellulära barriärer och i slutändan stödja mer exakt prognos och finjusterade immunoterapistrategier.
Citering: Xiao, C., Zhou, R., Chen, Q. et al. Integrative spatial profiling pipeline for determining TME architectures in archival clinical specimens using CmTSA superplex technology. Cell Discov 12, 16 (2026). https://doi.org/10.1038/s41421-026-00874-9
Nyckelord: tumörmikromiljö, spatial proteomik, multiplexavbildning, cancerimmunologi, analys på enkla cellnivå