Clear Sky Science · sv
Kronobiologi hos neurotopiska virus: rytmisk viral inträde och arytmiska värdur
Varför tidpunkt spelar roll för hjärninfektioner
Många farliga virus, inklusive rabies och herpes, har en förmåga att invadera hjärnan och nerverna. Denna studie ställer en överraskande enkel fråga med stora implikationer: ändrar tid på dygnet hur lätt dessa ”neurotopiska” virus kan ta sig in i vårt nervsystem, och kan virusen i sin tur rubba våra inre klockor? Att förstå denna tvåvägskommunikation mellan biologiska klockor och virus kan öppna nya möjligheter att tajma vaccin, antivirala läkemedel och till och med skiftarbete för att minska risk.
Dygnet-runt‑klockor och virala dörrhandtag
Nästan varje cell i kroppen bär på ett inbyggt 24‑timars tidssystem, ofta kallat den cirkadiska klockan. Det drivs av ett antal kärnproteiner i klockan, inklusive BMAL1 och REV‑ERBα, som slår på och av tusentals gener i rytmiska vågor. Författarna fokuserade på de ”dörrhandtag” virus använder för att ta sig in i celler – receptorproteiner på cellens yta – för flera dussin hjärn‑inriktade eller hjärninvaderande virus. Genom att undersöka hjärnliknande organoider odlade från stamceller, nerv‑härledda cellinjer och musvävnader fann de att de flesta av dessa virala receptorer stiger och sjunker över dygnet. Dessa rytmer följde nära klockkomponenternas aktivitet, vilket antyder att vårt dagliga tidssystem tyst styr hur många virala inträdespunkter som finns tillgängliga vid en viss tidpunkt.
En cellcykelfaktor blir en klockbudbärare
För att gå djupare frågade forskarna hur ett protein som vanligen är känt för att reglera celldelning, kallat E2F8, passar in i detta tidsnätverk. De upptäckte att E2F8 själv är under cirkadisk kontroll och fungerar som en reläpunkt mellan klockan och åtminstone en viktig rabiesreceptor, p75NTR. När klockproteinet REV‑ERBα är aktivt undertrycker det E2F8. I sin tur släpper låg nivå av E2F8 på bromsen för p75NTR‑genen, vilket tillåter mer av denna receptor att produceras och gör cellerna mer välkomnande för rabiesvirus. Slående nog återkopplar E2F8 också på klockan: det kan binda direkt till kontrollregioner hos kärnklockgener som REV‑ERBα och PER2 och dämpa deras aktivitet. Detta skapar en återkopplingsslinga där en cellcykelregulator hjälper till att forma dygnsrytmer och därigenom påverkar nervcellers sårbarhet för infektion.
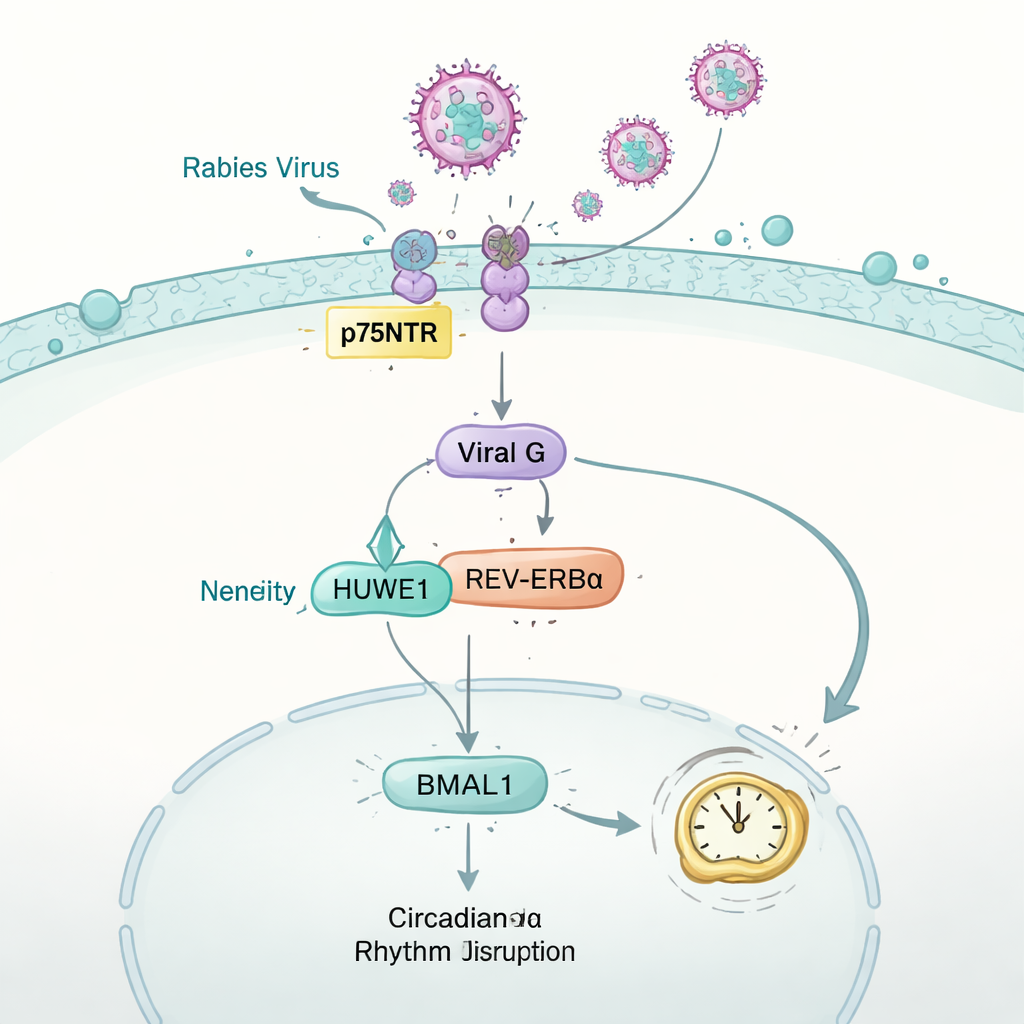
Hur rabiesvirus skjuter klockan ur kurs
Studien vände sedan på frågan: kan ett virus slå tillbaka mot klockan? Med hjälp av möss infekterade med rabiesvirus övervakade teamet löpaktivitet, ämnesomsättning och andningskemi. Trots normalt matintag tidigt i infektionen förlorade djuren gradvis de regelbundna dag‑natt‑mönster som friska möss visar. I hjärnan och flera andra organ sjönk nivåerna av det avgörande klockproteinet BMAL1 kraftigt. I nervliknande celler kunde denna effekt spåras till rabiesglycoproteinet ”G”, ett ytprotein som normalt hjälper viruset att fusera med celler. G kapade ett värdenzym kallat HUWE1, som vanligtvis hjälper till att märka ett annat klockprotein, REV‑ERBα, för nedbrytning. Genom att konkurrera om HUWE1 stabiliserade det virala G‑proteinet REV‑ERBα, vilket ledde till ökad undertryckning av BMAL1 och slutligen störning av klockverk som håller fysiologin på ett 24‑timmarschema.
Tajming, jetlag och infektionssvårighetsgrad
För att testa om dessa molekylära förändringar spelar roll för hela organismen infekterade teamet möss med rabies vid olika tidpunkter på dygnet, under normala ljus‑mörker‑cykler, under kroniska ”jetlag”‑förhållanden och i djur som genetiskt saknade REV‑ERBα. Möss infekterade i början av deras aktiva (nattliga) fas, när rabiesreceptorn p75NTR når sin topp, tappade snabbare i vikt, hade högre virusmängder i flera hjärnregioner, mer hjärn inflammation och dog tidigare än möss infekterade i början av deras vilofas. Möss utsatta för upprepade fasförskjutningar som efterliknar roterande skiftarbete förlorade normala klockrytmer i hjärnan, uppvisade ihållande högre nivåer av p75NTR, hade svagare grundläggande antivirala signaler och drabbades av svårare sjukdom. I kontrast uttryckte möss utan REV‑ERBα mindre p75NTR, bar lägre virusbördor och överlevde längre efter infektion, vilket indikerar att denna klockkomponent är en kritisk grindvakt för rabiesens svårighetsgrad.
Vad detta betyder för människor
Enkelt uttryckt visar studien att våra inre klockor inte bara styr sömntider; de öppnar och stänger också molekylära dörrar som hjärninvasiva virus använder, och dessa samma virus kan slå tillbaka genom att ställa klockan ur balans. En enda faktor, REV‑ERBα, sitter i en nyckelknutpunkt: tillsammans med E2F8 formar den både receptornivåer och dygnstiming, medan rabiesvirus manipulerar den till sin fördel. Dessa insikter pekar mot praktiska vägar framåt. Vacciner eller antivirala läkemedel kan fungera bättre vid vissa tider på dygnet, när receptorer är låga eller immunsvar är starka. Personer med kroniskt störda rytmer – såsom skiftarbetare eller frekventa resenärer – kan ha högre risk för vissa neurotopiska infektioner. Att rikta in sig på REV‑ERBα eller närliggande vägar skulle kunna hjälpa till att vända balansen till värdens fördel, göra infektioner mindre allvarliga och förbättra utfall.
Citering: Zeng, S., Zhang, Q., Yang, X. et al. Chronobiology of neurotropic viruses: rhythmic viral entry and arrhythmic host clocks. Cell Discov 12, 11 (2026). https://doi.org/10.1038/s41421-026-00867-8
Nyckelord: circadian klocka, neurotopiska virus, rabies, virala receptorer, kronoterapi