Clear Sky Science · sv
Dynamiska förändringar i immunsystemets mikro‑miljö vid ovarialcancer efter neoadjuvant kemoterapi
Varför denna forskning är viktig för kvinnor med ovarialcancer
Avancerad ovarialcancer behandlas ofta med kraftfull kemoterapi före eller efter operation, men många kvinnor får ändå återfall och slutar svara på läkemedel. Denna studie tar upp en angelägen fråga: hur omformar kemoterapin tyst kroppens egna försvar runt tumören, och kan vi justera det svaret för att få behandlingen att fungera längre? Genom att studera enskilda celler och testa nya läkemedelskombinationer i möss avslöjar forskarna en dold roll för fettlika hormonliknande molekyler kallade prostaglandiner i att hjälpa tumörer undkomma immunsystemet efter kemoterapi.
En föränderlig stridszon runt tumören
Ovariala tumörer växer inte isolerat: de ligger i ett trångt ”kvarter” av immunceller, bindväv och vätska i buken. Redan före behandling är detta kvarter ofta gynnsamt för cancern, med få aggressiva mördande T‑celler och många celler som dämpar immunsvaret. Teamet analyserade tidigare publicerade single‑cell RNA‑sekvenseringsdata från kvinnor med höggradig serös ovarialcancer och jämförde prover tagna före och efter neoadjuvant kemoterapi (kemoterapi som ges före operation). De fann att kemoterapin inte bara dödade tumörceller; den väckte också temporärt immunaktivitet, ökade signaler kopplade till T‑cellsstimulering och inflammation samtidigt som vissa regulatoriska T‑celler som normalt dämpar angrepp minskade.
När hjälpsamma förändringar blir skadliga
Trots denna korta förstärkning får de flesta patienter ändå återfall och blir resistenta mot platinabaserade läkemedel som cisplatin. För att förstå varför undersökte forskarna djupare hur olika celltyper kommunicerar efter behandling. De upptäckte att kemoterapi kraftigt ökade uttrycket av gener involverade i prostaglandinsyntes i tumörassocierade makrofager och fibroblaster, och förstärkte kommunikationen mellan dessa celler och T‑celler. Med avancerade matematiska verktyg visade de att miljön som helhet skiftade mot ett proinflammatoriskt men i slutändan hämmande tillstånd, med ökande nivåer av kemokiner som lockar myeloida celler och förhöjda vägar som över tid kan utarma T‑celler. Detta antyder att prostaglandiner kan fungera som en molekylär strömbrytare som omvandlar en inledningsvis hjälpsam immunstöt till en bestående broms för antitumorimmunitet.
Kemoterapi, prostaglandiner och tysta T‑celler
För att pröva denna idé experimentellt använde teamet en musmodell av ovarialcancer som behandlades med cisplatin. Single‑cell‑analys av tiotusentals celler från bukhålan visade att cisplatin minskade tumörceller och ökade totala T‑celler, men också markant utvidgade myeloid‑deriverade suppressorceller (MDSC) och utmattade mördande T‑celler. Både tumörceller och dessa suppressorceller producerade höga nivåer av prostaglandinsyntetiserande enzymer. I samkultur i odlingsskålar drev cisplatinbehandlade tumörceller benmärgsceller att anta ett MDSC‑liknande tillstånd och försvagade aktiviteten och tillväxten hos CD8+ mördande T‑celler. Forskarna spårade denna effekt till NF‑κB‑signaleringen i tumörcellerna, som slog på PTGES‑genen—ett nyckelsteg i produktionen av prostaglandin E2. Blockering av denna väg minskade PTGES‑nivåer och prostaglandinutsläpp.
Vända utvecklingen med kombinationsbehandling
Den mest praktiska frågan var om blockering av prostaglandiner kunde göra kemoterapin mer effektiv. I möss använde forskarna genetisk deletion av Ptges i tumörceller, antikroppar som neutraliserar prostaglandin E2, eller småmolekylära läkemedel som hämmar prostaglandin E‑syntas. Alla dessa metoder sänkte prostaglandinnivåerna, minskade ansamlingen av MDSC och återställde CD8+ T‑cellernas mördande förmåga och stamliknande motståndskraft. I kombination med cisplatin, eller med standardregimen cisplatin‑paklitaxel, bromsade prostaglandinhämmare tumörtillväxt och spridning mer effektivt än enbart kemoterapi. Data visar att prostaglandindriven immunsuppression inte är en bisak utan en central orsak till att tumörer undkommer efter ett initialt svar.
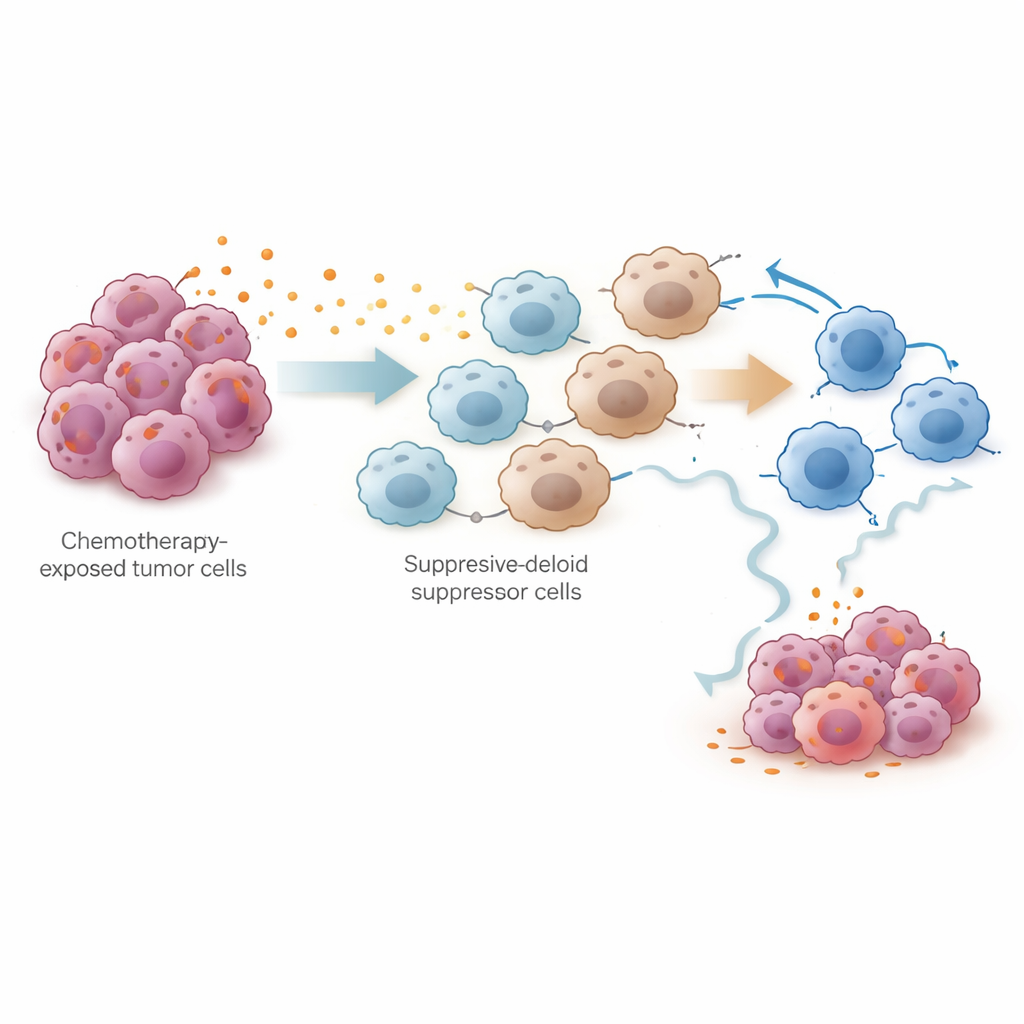
En ny infallsvinkel för att bibehålla behandlingens effekt
I vardagliga termer antyder detta arbete att kemoterapi förändrar tumörens omgivning i två faser: först försvagar den cancern och samlar kortvarigt immunsystemet, men därefter utlöser den en våg av prostaglandiner som lockar suppressorceller och tröttar ut kroppens naturliga tumördödande krafter. Genom att identifiera PTGES‑driven prostaglandinproduktion som en nyckelorsak pekar studien på en konkret strategi: att para ihop standard platina‑kemoterapi med läkemedel som blockerar prostaglandinvägar kan hjälpa till att upprätthålla ett starkt immunangrepp och fördröja eller förhindra återfall vid ovarialcancer. Även om kliniska prövningar fortfarande krävs, erbjuder denna kombinationsstrategi en hoppfull ny riktning för att förlänga nyttan av befintliga behandlingar.
Citering: Wu, M., Lv, F., Jin, Y. et al. Dynamic changes of the immune microenvironment in ovarian cancer following neoadjuvant chemotherapy. Cell Death Discov. 12, 130 (2026). https://doi.org/10.1038/s41420-026-03070-6
Nyckelord: ovarialcancer, tumörmikromiljö, kemoterapiresistens, prostaglandiner, immunterapi