Clear Sky Science · sv
Epigenetiskt sammanhang bestämmer transkriptionell aktivitet hos kanonisk och non-kanonisk NF-κB‑signalering i bukspottkörtelcancer
Varför denna studie är viktig för patienter
Bukspottkörtelcancer är en av de dödligaste cancerformerna, delvis därför att dess celler är skickliga på att avläsa och reagera på farosignaler i omgivningen. Denna studie undersöker två sådana signaler, kallade TNFα och TWEAK, och visar hur de slår på olika ”avläsningslägen” i cancercellernas DNA. Att förstå dessa lägen kan öppna nya vägar för att bromsa tumörtillväxt, begränsa spridning och göra behandlingar mer effektiva.
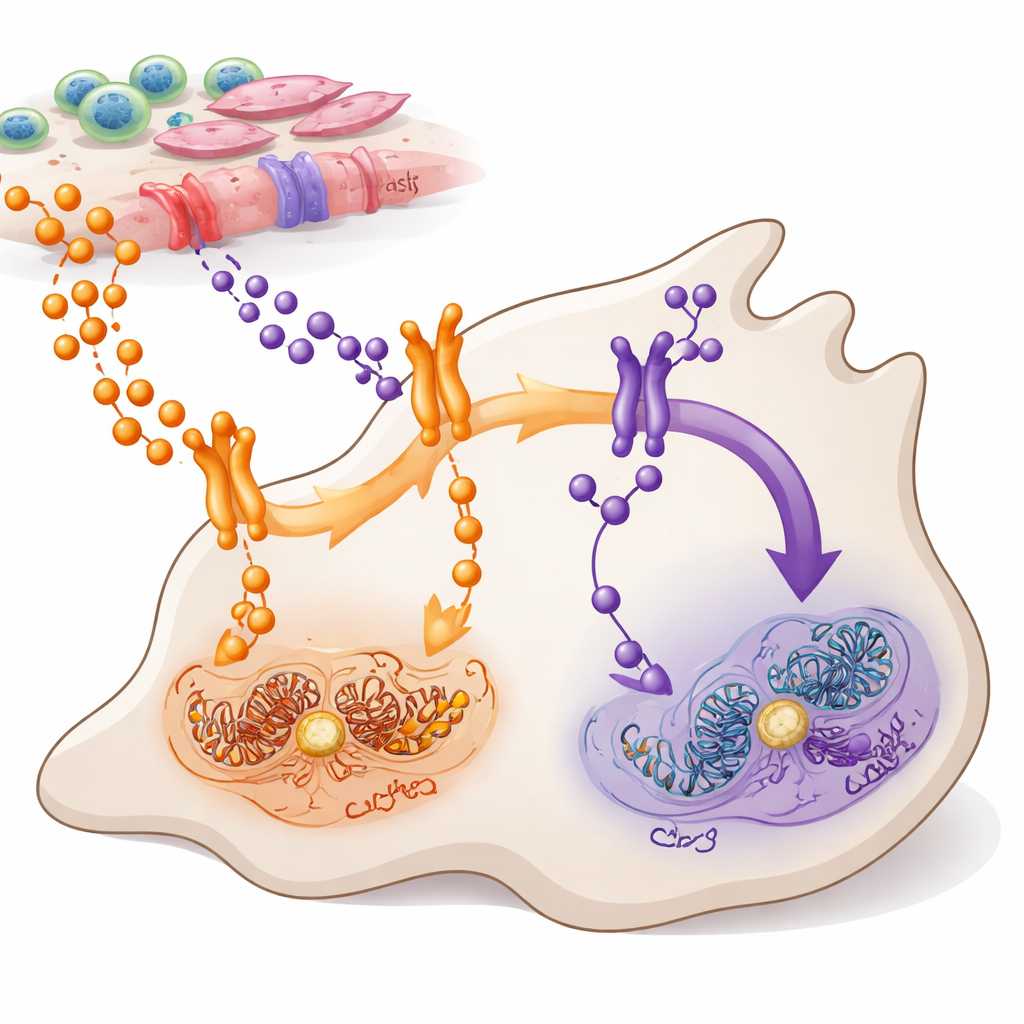
Två budbärarrutter in i cancercellerna
TNFα och TWEAK är små proteinbudbärare som frisätts av celler i och runt en tumör. Båda talar till ett viktigt kontrollsystem inne i cellerna som kallas NF-κB, vilket hjälper till att avgöra om celler ska växa, röra sig eller dö. Författarna fokuserade på pankreas ductalt adenokarcinom, den vanligaste och mest aggressiva formen av bukspottkörtelcancer, där NF-κB är onormalt aktivt i de flesta tumörer. De kartlade vilka celler som producerar TNFα och TWEAK, vilka celler som bär deras receptorer och hur dessa signaler flödar genom två närbesläktade NF-κB‑grenar—ofta kallade den kanoniska (via RELA) och den non-kanoniska (via RELB) vägen.
Vem skickar signalerna i tumörens grannskap
Genom att kombinera single-cell RNA-sekvensering från tusentals celler i patienttumörer med avancerad mikroskopi fann teamet att TNFα främst kommer från immunceller, särskilt makrofager och vissa T‑ och B‑celler. TWEAK, däremot, produceras av en bredare grupp: makrofager, fibroblaster, endotelceller och stellatceller. Deras receptorer skiljer sig också åt. Tumörceller och intilliggande fibroblaster uttryckte starkt den huvudsakliga TNFα‑receptorn och den centrala TWEAK‑receptorn. Nätverksanalys antydde att TWEAK‑baserad signalering bildar ett bredare och mer komplext kommunikationsnät över tumör‑ och stödjeceller, medan TNFα‑signalering är mer fokuserad inom immunrika områden.
Olika responsdjup inne i tumörcellerna
I cellinjer från bukspottkörtelcancer behandlade forskarna cellerna med TNFα eller TWEAK och mätte vilka gener som aktiverades över tid. TNFα utlöste en snabb och omfattande våg av genaktivitet kopplad till inflammation, cellulär rörelse, vävnadsombyggnad och överlevnad. TWEAK framkallade en mindre, långsammare uppsättning förändringar som till stor del överlappade TNFα:s mål snarare än att starta ett unikt program. Båda signalerna kunde främja cellmigration och, under vissa förhållanden, celldöd, men TNFα hade starkast effekt på rörelse. När teamet granskade patienttumördata från The Cancer Genome Atlas såg de att tumörer med höga nivåer av TNFα eller TWEAK delade många aktiverade gener, vilket bekräftade dessa mönster i verkliga mänskliga tumörer.
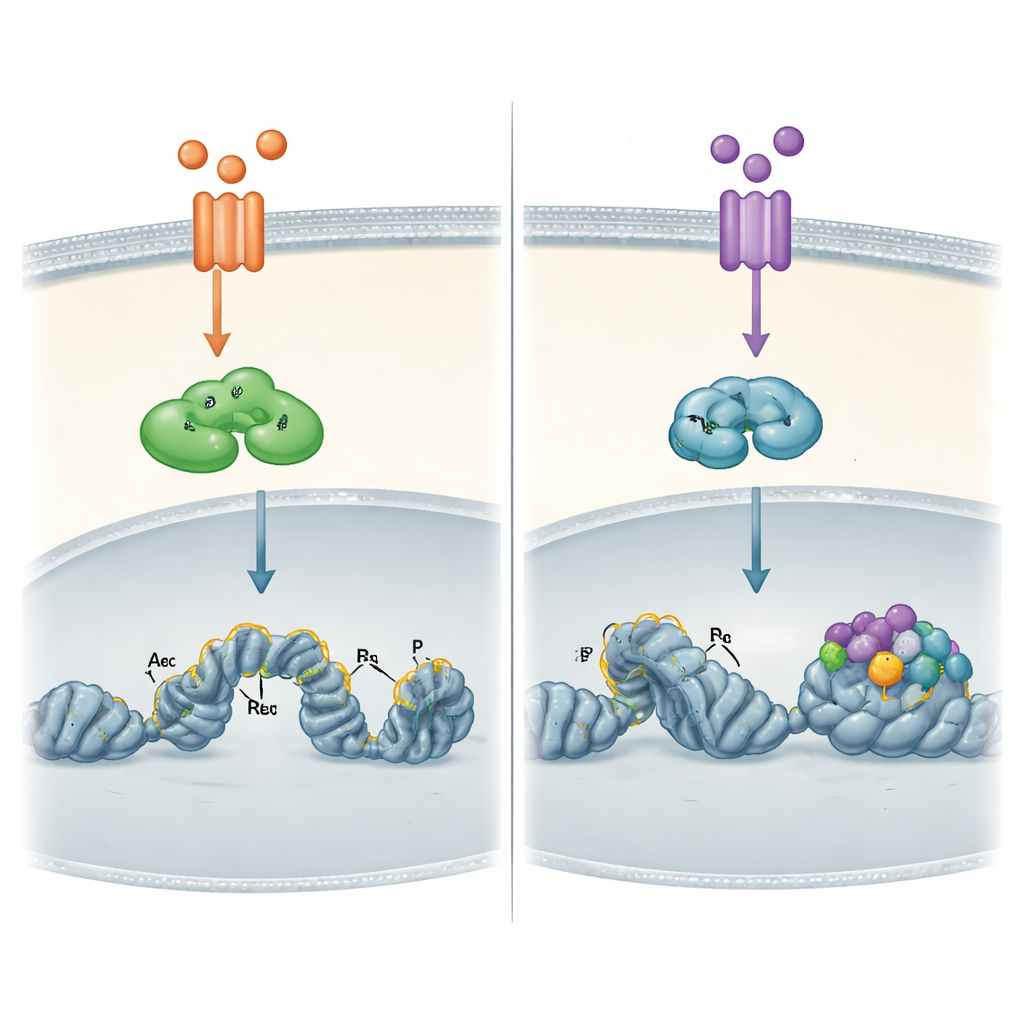
Hur DNA‑landskapet formar varje väg
De mest slående skillnaderna uppstod när författarna tittade direkt på cancercellernas kromatin—den packade formen av DNA och dess associerade proteiner. Med hjälp av genomomfattande bindningskartor visade de att RELA, aktiverad av TNFα, kan binda inte bara till redan öppna DNA‑regioner utan också till tätare packade områden och sedan hjälpa till att ”öppna” dem genom att lägga till kemiska markörer som är förknippade med aktiva brytare. RELB, som aktiveras senare av TWEAK, band nästan uteslutande till platser som redan var tillgängliga och prydda med sådana aktiva markörer. Dessa RELB‑platser var särskilt rika på dockningsmotiv för en annan faktorgrupp, AP‑1, vilket tyder på att RELB är beroende av andra proteiner för att förbereda marken innan den kan agera.
Vad detta innebär för framtida behandlingar
För en icke‑specialist är huvudpoängen att TNFα och TWEAK använder samma NF‑κB‑verktyg på väldigt olika sätt. TNFα, via RELA, beter sig som en huvudströmbrytare som kan pröva upp stängda delar av cancercellens DNA och aktivera ett brett spektrum av gener inblandade i tillväxt, överlevnad och spridning. TWEAK, via RELB, är mer som en specialist som bara kan verka där DNA redan är öppet och där kofaktorer som AP‑1 finns närvarande. Denna arbetsfördelning tyder på att läkemedel som riktar sig mot kromatinombyggnad, AP‑1 eller specifika NF‑κB‑grenar kan selektivt dämpa skadliga genprogram i bukspottkörtelcancer samtidigt som andra funktioner i större utsträckning lämnas intakta.
Citering: Aggrey-Fynn, J.E., Busch, J., Saul, D. et al. Epigenetic context defines the transcriptional activity of canonical and noncanonical NF-κB signaling in pancreatic cancer. Cell Death Discov. 12, 152 (2026). https://doi.org/10.1038/s41420-026-03019-9
Nyckelord: bukspottkörtelcancer, NF-kappaB-signalering, tumörmikromiljö, epigenetisk reglering, TNF och TWEAK