Clear Sky Science · sv
Att utnyttja pyroptos i bröstcancerterapi: immunologiska mekanismer och framväxande biomaterialstrategier
Göra celldöd till ett nytt vapen mot bröstcancer
Bröstcancer är fortfarande en av de vanligaste och mest svårbehandlade cancerformerna i världen. Många tumörer lyckas så småningom undkomma kirurgi, cytostatika och till och med moderna immunoterapier. Denna översikt tar upp en framväxande idé: att medvetet utlösa en ”brinnande” form av celldöd kallad pyroptos inne i brösttumörer. Genom att få cancerceller att brista på ett kontrollerat, inflammatoriskt sätt hoppas forskare både kunna döda tumören direkt och väcka immunförsvaret att delta i anfallet.
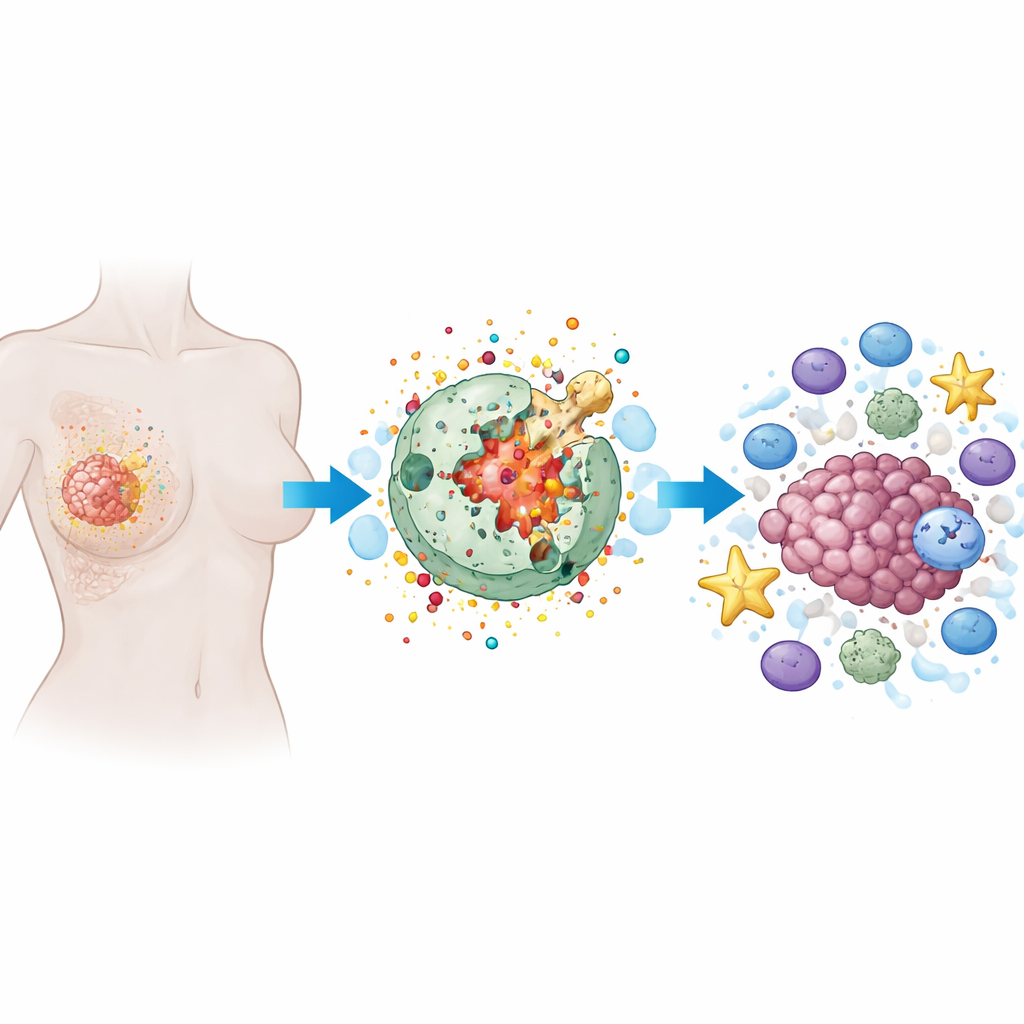
Hur en brinnande celldöd fungerar
Pyroptos är en programmerad form av celldöd där en cell sväller, dess yttre membran blir fullt av porer och den slutligen brister och spiller ut sitt innehåll. Till skillnad från tyst, prydlig celldöd som ses vid många behandlingar är pyroptos högljudd och inflammatorisk. Specialiserade proteiner, framför allt en familj kallad gasderminer, fungerar som små sprängladdningar. När de klyvs av interna enzymer borrar gasderminer hål i cellmembranet. Detta förstör inte bara cancercellen utan frigör också varningssignaler och inflammatoriska molekyler som kan rekrytera och aktivera immunceller.
Varför brösttumörer är en särskild utmaning
Bröstcancer är inte en enda sjukdom utan en samling subtyper med olika beteenden. Vissa, som trippelnegativ bröstcancer, saknar vanliga läkemedelsmål och är ofta svårbehandlade. Många brösttumörer anses vara ”immunologiskt kalla”, vilket innebär att de innehåller få aktiva immunceller. Översikten förklarar hur egenskaper i tumörens omgivning — inklusive stromaceller, immunsuppressiva celler och lokala syrebrister — samtidigt kan skapa förutsättningar för pyroptos och, om den är illa kontrollerad, omvandla dess inflammation till bränsle för tumörtillväxt och spridning. Denna tveeggade natur gör precision särskilt viktig.
Gasdermin‑strömbrytarna inne i tumörcellerna
Ett centralt tema i artikeln är hur olika gasderminproteiner fungerar som molekylära strömbrytare inne i bröstcancerceller. Varianter som GSDMD och GSDME kan omvandla signaler från kemoterapi, strålning eller angripande immunceller till fullskalig pyroptos. Andra, som GSDMC och vissa former av GSDMB, är ofta uppreglerade i aggressiva tumörer och kan både främja eller hämma sjukdomen beroende på hur de aktiveras. Många bröstcancerformer tystar kemiskt GSDME, vilket dämpar pyroptos och immunaktivering. Att återställa eller selektivt utlösa rätt gasderminer kan avgöra om en behandling bara dödar några celler eller förvandlar hela tumören till ett in situ‑vaccin som väcker immunsystemet.
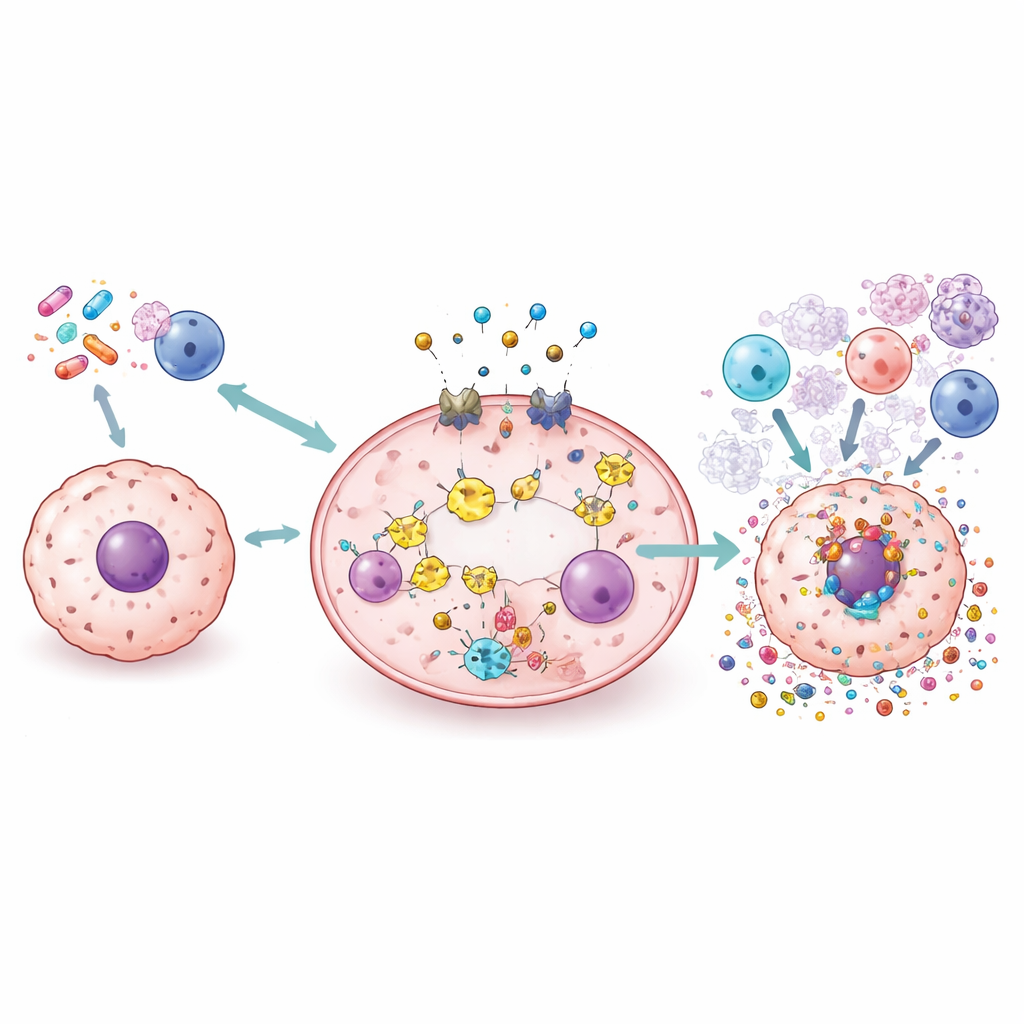
Nya verktyg: läkemedel, nanopartiklar, virus och strålning
Översikten går igenom en rad strategier under studie för att tygla pyroptos på ett säkert sätt. Standardläkemedel som cisplatin och doxorubicin kan omprövas eller omformuleras för att styra cancerceller mot gasderminstyrd bristning istället för tyst död. Små molekyler kan antingen förstärka eller blockera delar av vägen för att finjustera inflammationen. Nanopartiklar och biomimetiska bärare designas för att leverera cytostatika, kopparjoner eller ljusaktiverade molekyler direkt in i tumörer, där de utlöser pyroptos samtidigt som frisk vävnad skonas. Onkolytiska virus och radioterapi kan också konstrueras eller kombineras med andra agenter för att framkalla pyroptos och omforma tumörens immunologiska landskap, vilket potentiellt kan göra immunkontrollpunktsläkemedel mer effektiva.
Att väga kraftfull nytta mot verkliga risker
Eftersom pyroptos är så inflammatorisk kan samma reaktioner som hjälper immunförsvaret att bekämpa cancer också skada normal vävnad eller till och med främja tumörtillväxt om de blir kroniska. Författarna belyser tidiga biomarkörer — såsom gensignaturer, metyleringsmönster, fragment av gasderminproteiner i blodet och cytokinprofiler — som kan hjälpa till att identifiera vilka patienter som sannolikt får nytta och vilka som löper högre risk för farliga ”cytokinstormar”. Avancerade nanomedicinska designer, noggrant utvalda läkemedelskombinationer och övervakning i realtid av inflammatoriska markörer utforskas för att hålla svaret skarpt men kontrollerat.
Vad detta kan innebära för framtida patienter
Enkelt uttryckt hävdar denna översikt att få cancerceller att ”dö högljutt” kan förändra bröstcancervården. Genom att utlösa pyroptos i en precist utvald del av tumörcellerna kan läkare både krympa tumören och väcka ett kraftfullt, bestående immunsvar, vilket förvandlar kalla tumörer till varma och mer responsiva för moderna immunoterapier. Men pyroptos är en flyktig bundsförvant: om den släpps lös för vida eller för länge kan den förvärra inflammation eller gynna resistenta celler. Framtida forskning kommer att fokusera på att kartlägga vilka som får nytta, förfina riktade leveranssystem och genomföra kliniska prövningar som parar ihop pyroptos‑inducerande metoder med immunläkemedel. Om dessa utmaningar kan lösas kan utnyttjandet av pyroptos lägga till en potent ny dimension i bröstcancerbehandlingen.
Citering: Asiedu, R.K.F., Souley Abdou, M., Wei, R. et al. Harnessing pyroptosis in breast cancer therapy: immunological mechanisms and emerging biomaterial strategies. Cell Death Discov. 12, 157 (2026). https://doi.org/10.1038/s41420-026-02996-1
Nyckelord: pyroptos, bröstcancer, gasdermin, tumörmikromiljö, nanomedicin