Clear Sky Science · sv
Absolut dynamik och relativ statik: förhållandet mellan glykolys och OXPHOS i cancerutveckling
Varför cancerns energival spelar roll
Cancerceller liknar extrema uthållighetsidrottare: de måste ständigt försörja sig för att växa, sprida sig och undvika behandling. Denna översikt förklarar hur tumörceller utnyttjar två huvudsakliga energisystem—ett snabbt och ett effektivt—och, viktigast av allt, hur de blandar och växlar mellan dem. Att förstå dessa skiftande energistrategier ger ett nytt sätt att tänka kring diagnostik och behandling av cancer under hela sjukdomsförloppet.
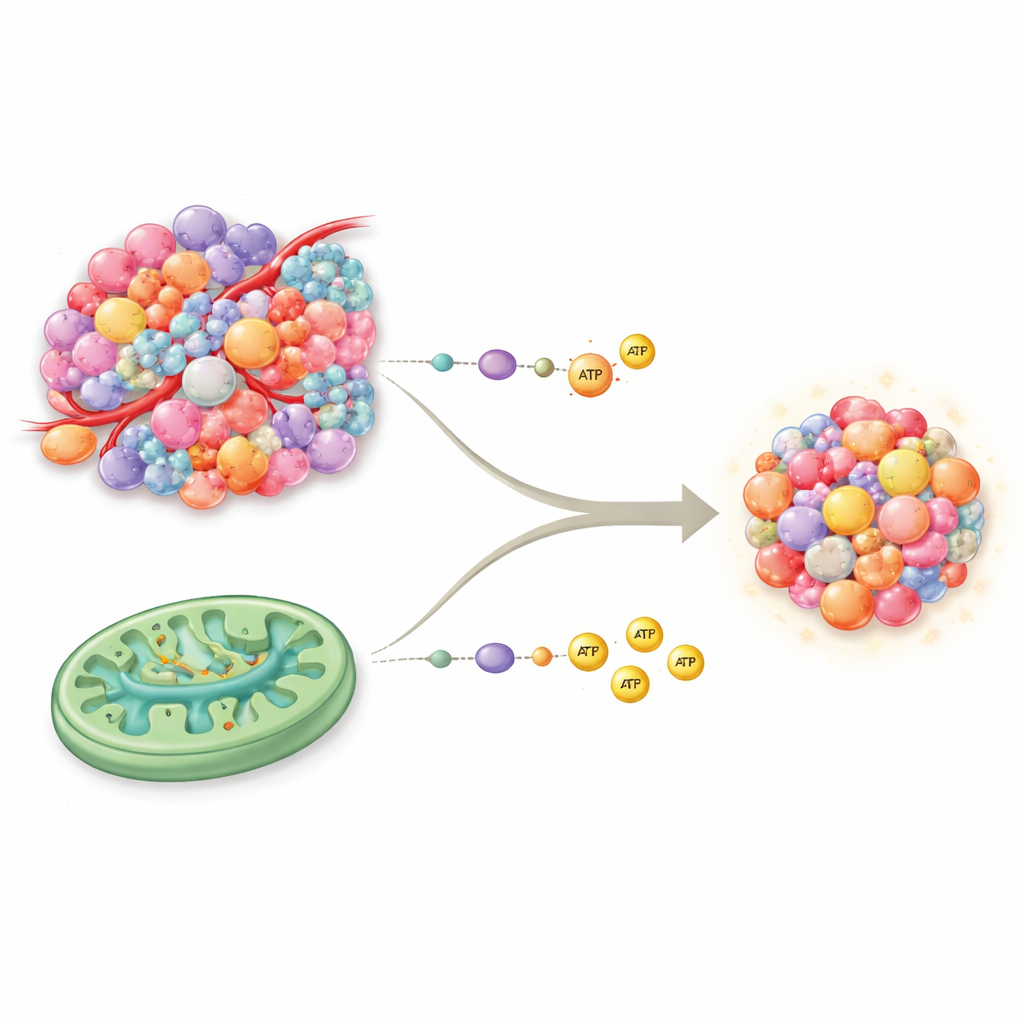
Två huvudsakliga sätt som celler skapar bränsle
Våra celler producerar vanligtvis energi via två grundläggande vägar. Glykolys är det snabba, ”kontanta” systemet som bryter ner socker snabbt men ger relativt lite energi per enhet. Oxidativ fosforylering, eller OXPHOS, sker i mitokondrierna och fungerar mer som ett hög-effektivt kraftverk, som producerar mycket mer energi men kräver god tillgång på syre och näring. Under decennier trodde man att cancer nästan uteslutande förlitade sig på glykolys även när syre fanns tillgängligt—ett mönster känt som Warburg-effekten. Nyare bevis ifrågasätter denna förenklade bild: många tumörer har fullt fungerande mitokondrier och kan använda OXPHOS och trikarboxylsyracykeln (TCA) tillsammans med glykolys, vilket ger en rikare och mer flexibel energiverktygslåda än man tidigare uppskattade.
Många celltyper, många energival
En tumör är inte en homogen klump. Den är ett litet ekosystem som innehåller cancerceller, stödjeceller, blodkärl och immunceller, var och en med skilda energibehov. Vissa cancerceller lever nära blodkärl och har gott om syre och näring; andra är begravda djupt i dåligt försörjda områden. Som ett resultat kan celler inom samma tumör föredra glykolys, förlita sig främst på OXPHOS eller använda båda samtidigt. Denna metaboliska mångfald—kallad heterogenitet—uppstår från skillnader i blodflöde, näringsnivåer, celltyp och signaler från omgivningen. Därtill visar tumörer ofta metabol symbios: glykolytiska celler exporterar laktat som en slags avfallsprodukt, vilken närliggande OXPHOS-beroende celler importerar och förbränner som ett värdefullt bränsle. Liknande laktatdelning sker mellan cancerceller och stödjeceller såsom fibroblaster, kärlbyggande celler och immunsuppressiva celler, vilket tillsammans hjälper tumören att frodas och motstå terapi.
Ständigt i förändring: hur tumörens energi skiftar över tid
Tumörmetabolism är inte bara mångfaldig vid en given tidpunkt; den är också mycket dynamisk. När tumörer växer möter de förändrade förhållanden som lågt syre, syrabildning, näringsbrist och variationer i vävnadens styvhet. Under hårda, syrefattiga förhållanden skiftar många cancerceller mot glykolys. Vid syrabildning eller sockersvält kan de istället svänga tillbaka mot tyngre användning av OXPHOS. Samma flexibilitet syns under viktiga biologiska skeden. Snabbt delande celler lutar mot glykolys för att skapa byggstenar till nytt DNA, fetter och membran. Celler som vilar eller cirkulerar i blodet förlitar sig ofta mer på OXPHOS. Under invasion och metastas anpassar sig cancerceller upprepade gånger: vissa steg gynnar glykolys, andra OXPHOS, och metastatiska celler som koloniserar nya organ finjusterar sin metabolism för att passa ”jorden” i målvävnaden.
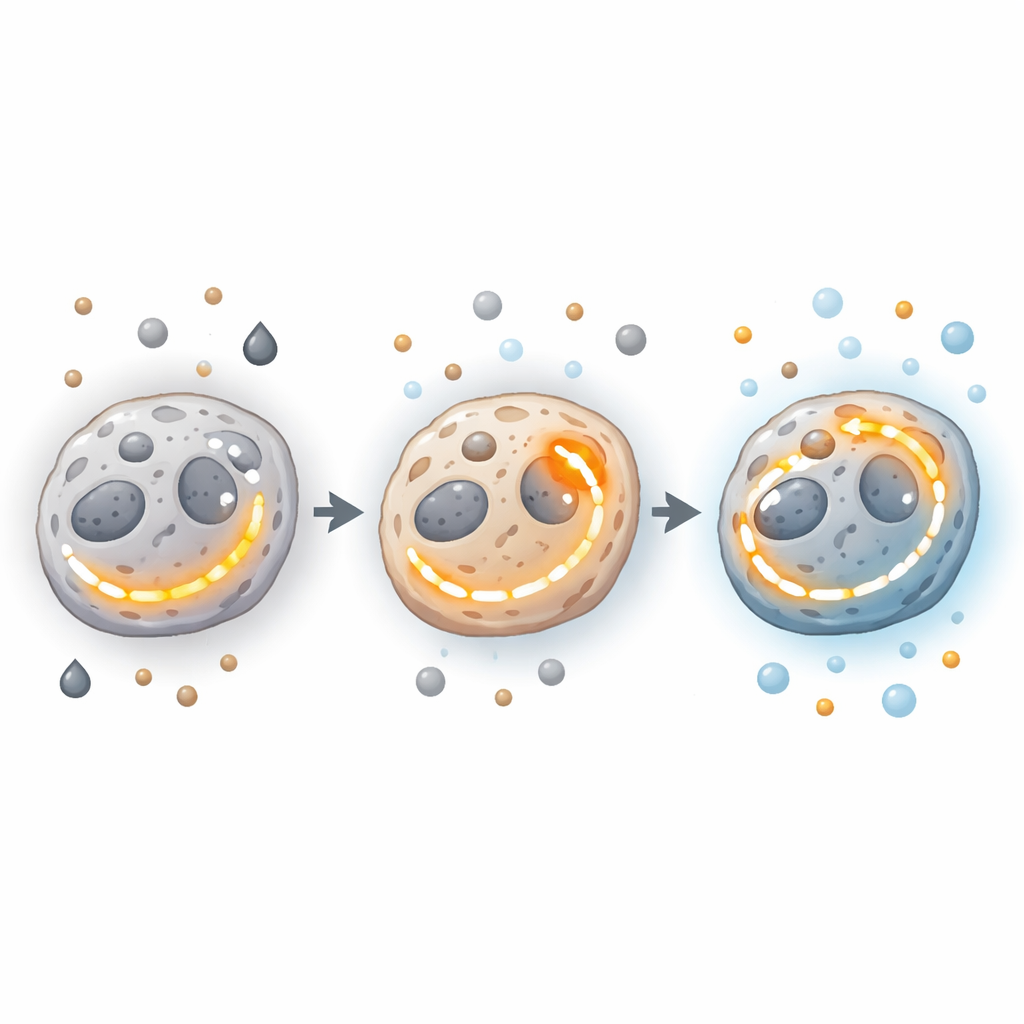
Gener, enzymer och kraftverk bakom skiftet
Djup i cellens maskineri styr gener och enzymer dessa energibeslut. Onkogener och tumörsuppressorer kan driva celler mot glykolys eller OXPHOS, eller möjliggöra att båda ökas samtidigt. Mutationer eller förändringar i viktiga TCA-enzym—sådana som hanterar citrat, succinat eller isocitrat—kan rubba balansen och ibland driva cancerskapande signaler som kärltillväxt och invasion. Enzymer som sitter vid avgörande korsningar—som pyruvatkinas M2, som hjälper avgöra om sockerassocierat kol blir energi eller byggmaterial—binder ihop glykolys och mitokondriell funktion. Samtidigt breddar skillnader i mitokondriernas antal, struktur och prestanda över tumörområden ytterligare spektrumet av möjliga energitillstånd.
Omprövning av behandling genom ett rörligt energimål
Eftersom tumörceller kan skifta mellan glykolys och OXPHOS räcker det ofta inte att bara blockera en väg; cancern kan dirigera om sitt bränsleanvändande och överleva. Författarna menar att energimetabolismen i cancer bara är stabil under korta perioder och i grunden, ständigt förändras. De föreslår att se tumörer genom ett ”energimetabolisk spektrum” som måste mätas över tid, inte bara en gång. I praktiken kan detta innebära att man följer en tumörs bränslepreferenser under olika sjukdomsstadier och kombinerar hämmare av glykolys och OXPHOS i skräddarsydda kombinationer. Sådana dynamiska, metabolismstyrda behandlingsstrategier skulle bättre kunna skära av tumörens strömtillförsel, begränsa dess förmåga att anpassa sig och förbättra långsiktigt kontroll över sjukdomen.
Citering: Bao, X., Hou, B., Guo, Z. et al. Absolute dynamic and relative static: the relationship of glycolysis and OXPHOS in cancer development. Cell Death Discov. 12, 136 (2026). https://doi.org/10.1038/s41420-026-02992-5
Nyckelord: cancermetabolism, glykolys, oxiderande fosforylering, tumörmikromiljö, metabolisk plasticitet