Clear Sky Science · sv
Exosomalt S100A9 främjar lungmetastaser av adenoid cystiskt karcinom genom att aktivera cancerassocierade fibroblaster
Hur en tyst spottkörtelcancer hittar vägen till lungorna
Adenoid cystiskt karcinom är en långsamt växande men seglivad cancer som ofta börjar i spottkörtlarna och senare dyker upp i lungorna, ibland år efter att den första tumören avlägsnats. För patienter och deras familjer är denna fördröjda spridning skrämmande och svår att förutsäga eller förebygga. Denna studie klargör hur celler i dessa tumörer i hemlighet förbereder avlägset lungvävnad för cancerinvasion, och avslöjar en dold kommunikation mellan tumörceller och omgivande stödjeceller som slutligen kan erbjuda nya behandlingsmöjligheter.
Cancern som dröjer kvar och återkommer
Adenoid cystiskt karcinom (ACC) är en cancer i körtlarna i huvud- och halsområdet, särskilt spottkörtlarna. Kirurgi och strålning kan ofta kontrollera primärtumören, men många patienter utvecklar så småningom lungmetastaser, vilket är den ledande dödsorsaken. Nuvarande läkemedel för utbredd ACC är begränsade, delvis eftersom forskarna inte fullt ut förstår hur celler från den ursprungliga tumören lyckas etablera sig och växa i lungorna. Författarna till denna artikel ville identifiera de centrala signalerna som gör det möjligt för ACC-celler att omforma sin omgivning och skapa en välkomnande ”jordmån” för framtida lungtumörer.
Små paket med stort inflytande
Forskarlaget koncentrerade sig på exosomer, små membranbundna blåsor som cancerceller släpper ut i blodet. Dessa vesikler bär proteiner och genetiskt material som kan omprogrammera andra celler på avstånd. Genom att jämföra en standard ACC-cellinje med en version selekterad för stark lungspredd förmåga fann teamet att både de aggressiva cellerna och deras exosomer var berikade på ett protein kallat S100A9, som kopplats till inflammation. Patienter vars tumörer och blodexosomer innehöll mer S100A9 löpte större risk att få lungmetastaser och kortare sjukdomsfria intervall, vilket tyder på att detta protein bidrar till cancer spridning.
Omprogrammering av tumörens stödteam
Med hjälp av encells-RNA-sekvensering byggde författarna en detaljerad karta över alla celltyper inne i ACC-tumörer och närliggande normala körtlar. De upptäckte intensiv kommunikation mellan tumörets epitelceller och närliggande fibroblaster, de strukturella cellerna som producerar bindväv. I cancer kan dessa fibroblaster bli ”rekryterade” och omvandlas till cancerassocierade fibroblaster (CAF), som gör vävnad stelare, driver inflammation och hjälper cancerceller att röra sig. Studien visade att S100A9-rika exosomer från aggressiva ACC-celler kunde omvandla normala fibroblaster till aktiverade CAF:er: de blev mer kontraktila, mer rörliga och började producera enzymer och inflammatoriska molekyler som omformar vävnad och gynnar tumörtillväxt.
Från lokala signaler till lungkolonier
Teamet frågade sedan om dessa exosomaktiverade fibroblaster faktiskt underlättar för ACC att kolonisera lungorna. I musmodeller primade injektion av S100A9‑laddade exosomer blodomloppet och förberedda lungorna: fibroblaster där slog på aktiveringsmarkörer och lungvävnad började uttrycka faktorer kopplade till ny blodkärlsbildning och matrixnedbrytning. När ACC‑celler senare introducerades utvecklade möss som förbehandlats med S100A9‑exosomer fler och större lungmetastaser. Ytterligare analyser visade att denna process berodde på en kedja av inflammatoriska signaler centrerade kring budbäraren IL‑17, tillsammans med TNF och NF‑κB, vilka tillsammans förstärkte fibroblastaktiveringen och omformade lungmikromiljön.
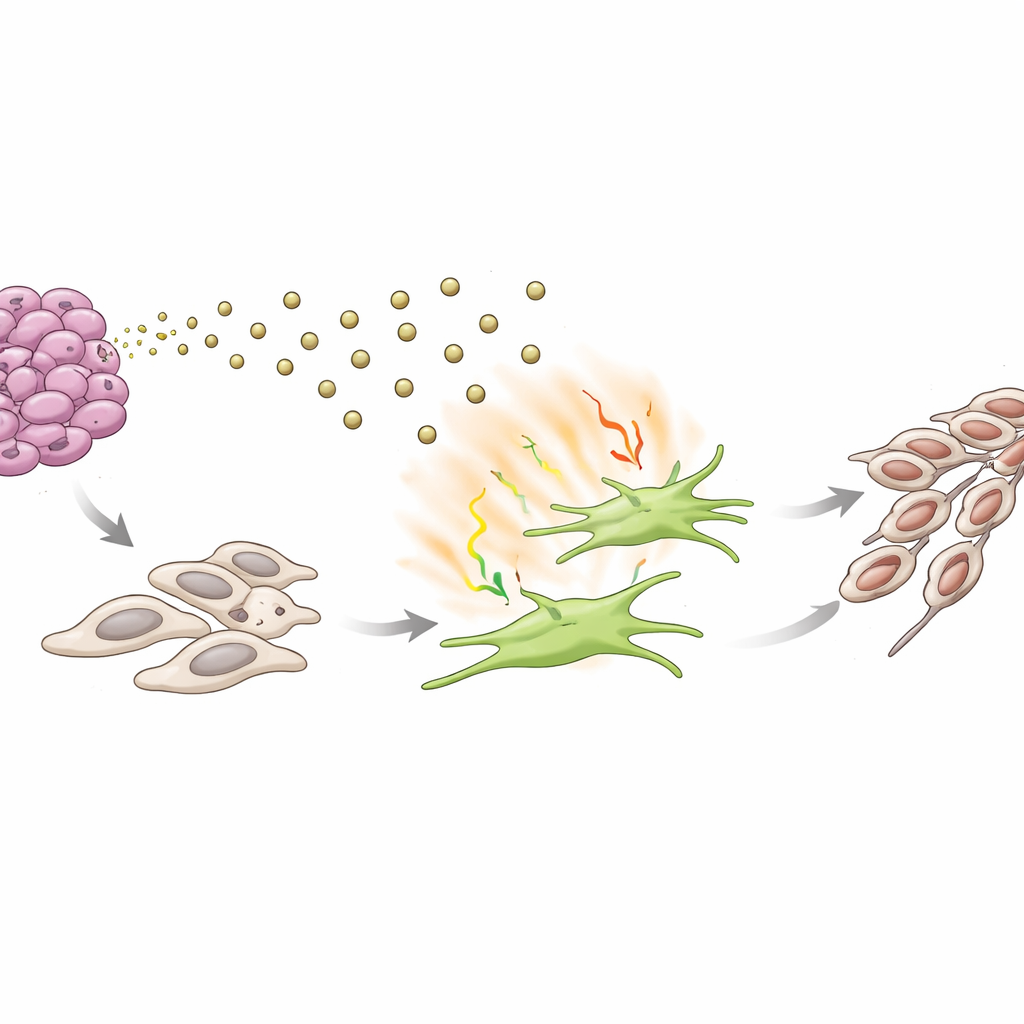
En ond cirkel som driver cancerns formförändring
I laboratoriekokultursystem gjorde fibroblaster som blivit ”utbildade” av S100A9‑rika exosomer, eller av denna IL‑17‑drivna signalväg, närliggande ACC‑celler mer aggressiva. Cancercellerna blev bättre på att röra sig, invadera barriärer, bilda kolonier och anta en mer mobil, spolformad form som förknippas med en epitelial–mesenkymal övergång, ett viktigt steg mot metastasering. Att blockera IL‑17 med en neutraliserande antikropp vände många av dessa förändringar, medan tillsats av ren IL‑17 ensam drev ACC‑celler mot detta mer invasiva tillstånd. Tillsammans beskriver dessa fynd en självförstärkande slinga: tumörceller skickar S100A9 i exosomer för att aktivera fibroblaster; aktiverade fibroblaster släpper ut IL‑17 och andra signaler som i sin tur gör tumörceller mer benägna att sprida sig.
Att bryta den dolda kommunikationsslingan
För en lekmannaläsare är budskapet att ACC inte sprider sig till lungorna av en slump. I stället tränar den ursprungliga tumören i hemlighet stödjeceller och avlägsen vävnad för att hjälpa den växa på andra platser, med hjälp av små proteinfyllda paket som budbärare. Detta arbete identifierar S100A9 och den efterföljande IL‑17‑signalvägen som centrala nav i den processen. Genom att rikta in sig på denna kommunikationsaxel — antingen genom att blockera S100A9, dämpa IL‑17‑signalering eller störa aktiveringen av fibroblaster — kan framtida terapier potentiellt avbryta ”förberedelsefasen” för lungmetastasering och ge kliniker nya sätt att hindra denna tysta men farliga cancer från att återkomma långt från dess ursprung.
Citering: Chen, Cw., Zhang, Sr., Yan, Ym. et al. Exosomal S100A9 promotes lung metastasis of adenoid cystic carcinoma via activating cancer-associated fibroblasts. Cell Death Discov. 12, 120 (2026). https://doi.org/10.1038/s41420-026-02991-6
Nyckelord: adenoid cystiskt karcinom, exosomer, cancerassocierade fibroblaster, lungmetastaser, S100A9 IL-17-axel