Clear Sky Science · sv
APOA2-medierad endotelial-mesenkymal omvandling och omprogrammering av cancerlipidmetabolism ger resistens mot antiangiogena läkemedel via TGF-β
Varför denna upptäckt är viktig för patienter
Läkare använder i allt större utsträckning läkemedel som svälter ut levertumörer genom att skära av deras blodförsörjning, men många patienter upplever att deras cancer slutar reagera efter en initial förbättring. Denna studie ställer en brännande fråga: varför blir vissa levercancerformer resistenta mot dessa kärlblockerande behandlingar, och hur kan vi överlista dem? Forskarna avslöjar ett dolt samspel mellan ett blodfettsprotein och en stark tillväxtsignal som gör att tumörer kan omprogrammera både sina blodkärl och sin energianvändning, vilket pekar på ett annat sätt att behandla en svårbotad cancer.
En tumör som lär sig leva utan sin vanliga livlina
Hepatocellulärt karcinom, den vanligaste formen av levercancer, är starkt beroende av nybildade blodkärl för att växa. Standardläkemedel för avancerad sjukdom är utformade för att blockera en nyckelväg för kärltillväxt centrerad på VEGF och dess receptor VEGFR2. Ändå fortsätter tumörer i många patienter att frodas trots dessa mediciner. Genom att jämföra tumörprover från patienter som antingen svarade eller inte svarade på det antiangiogena läkemedlet apatinib fann författarna att en gen, APOA2, stack ut. Tumörer från resistenta patienter uppvisade markant högre nivåer av APOA2, ett protein mest känt för sin roll i transport av fetter i blodet. Detta väckte möjligheten att APOA2 kan hjälpa tumörer att undkomma kärl-riktade läkemedel.
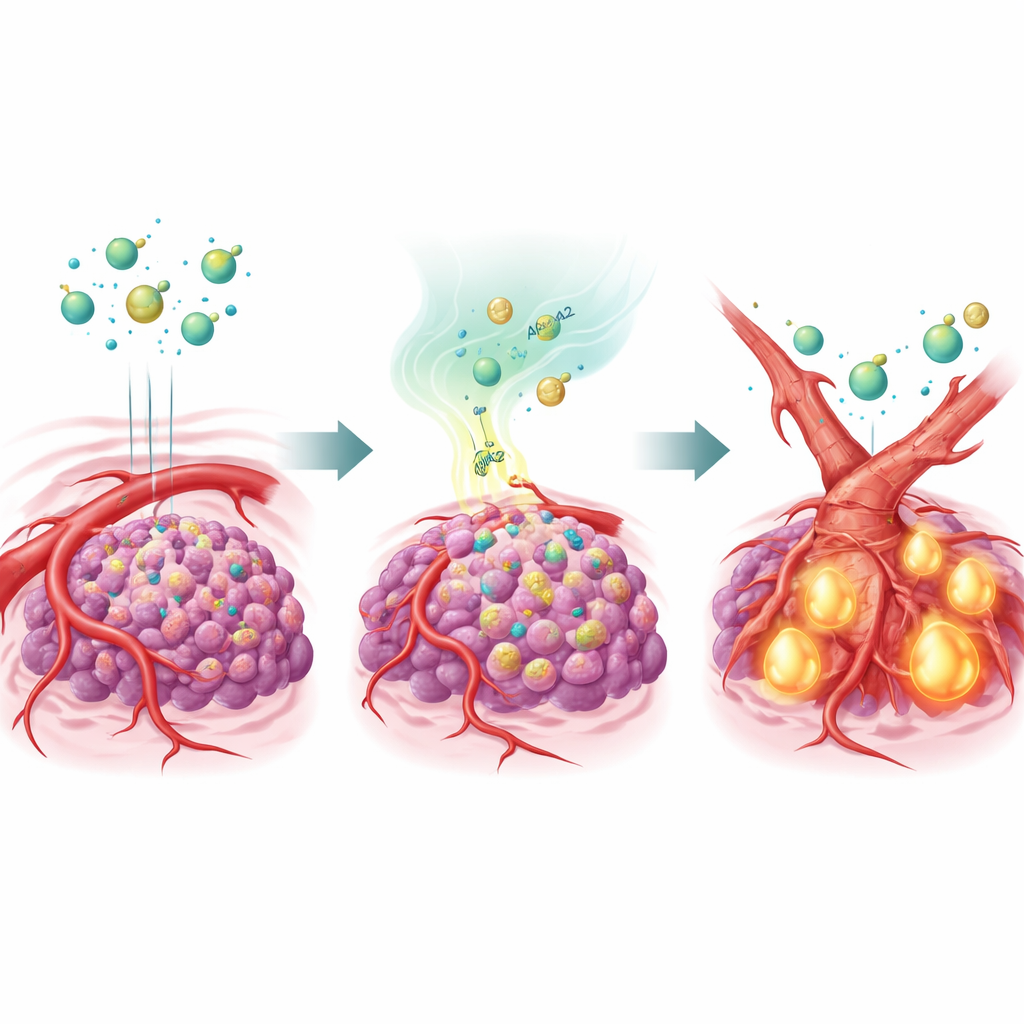
Ett fetttransportprotein som omformar blodkärlen
För att pröva denna hypotes konstruerade teamet levercancerceller som överproducerade APOA2 och implanterade dem i möss. När de behandlades med flera olika antiangiogena läkemedel ignorerade dessa APOA2-rika tumörer i stort sett terapin: deras blodkärl bestod och cancerna fortsatte växa. Detaljerade analyser visade att en mästarsignal kallad TGF-β var kraftigt aktiverad i dessa tumörer, och dess nivåer var förhöjda både i tumörmiljön och i djurens blod. TGF-β verkade på cellerna som bekläder blodkärlen och drev dem att ändra identitet i en process som kallas endotelial-till-mesenkymal omvandling. När de skiftade mot ett mer ärrliknande, mesenkymalt tillstånd förlorade dessa celler stora delar av sitt VEGFR2, just det handtag som antiangiogena läkemedel är avsedda att greppa. I praktiken omformades kärlen till en form som läkemedlen inte längre kunde rikta in sig på.
En metabol omväg som håller cancercellerna drivna
Berättelsen slutade inte vid kärlväggen. Samma TGF-β-signal som drivs av APOA2 omprogrammerade också hur cancerceller förser sig med energi. Istället för att i huvudsak förlita sig på nedbrytning av socker började APOA2-höga celler ta upp fler fria fettsyror från omgivningen och förbränna dem i sina mitokondrier via fettsyreoxidation. Experiment som mätte näringsanvändning och syreförbrukning visade att dessa celler blev mer beroende av fett som energikälla och producerade mer cellulärt bränsle (ATP). Detta skifte gjorde det möjligt för tumörceller att fortsätta dela sig snabbt och undvika celldöd, även när blodförsörjningen pressades av antiangiogen behandling.
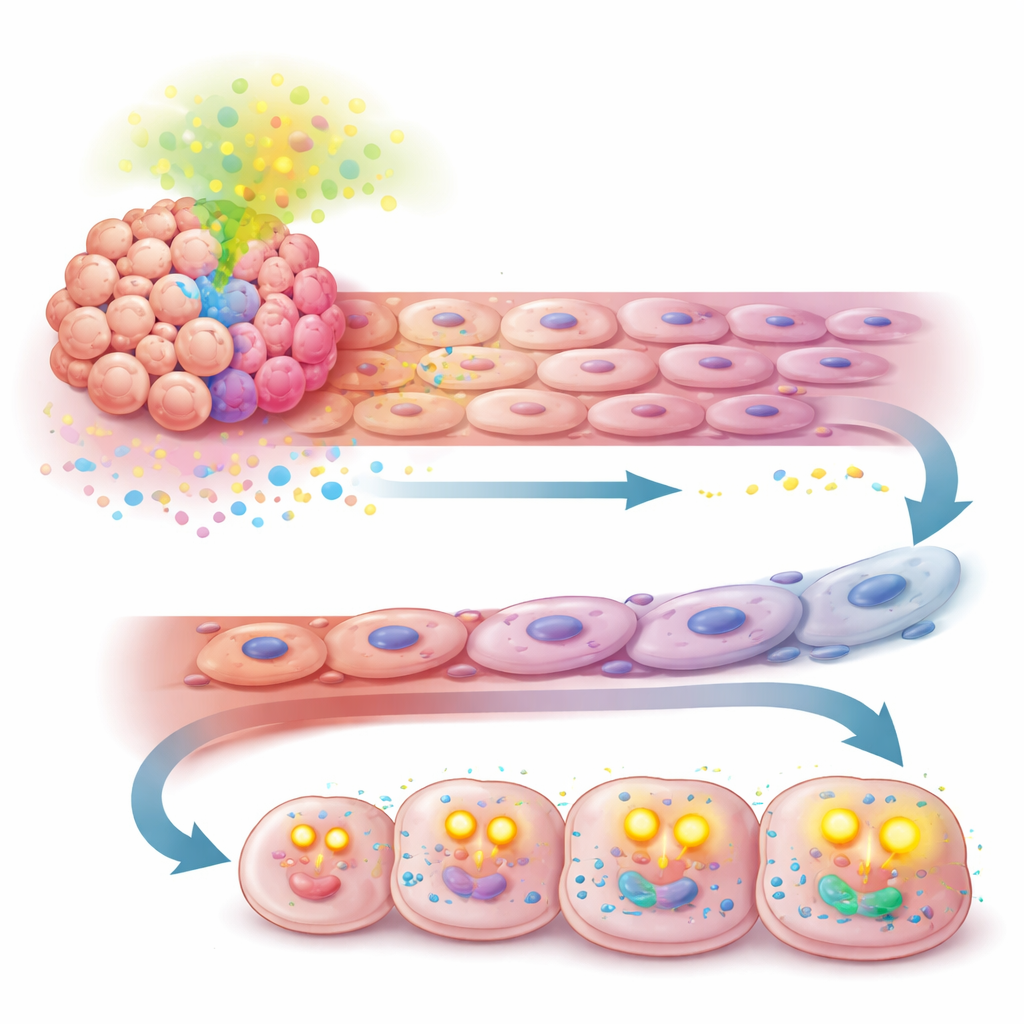
Att vända en svaghet till ett nytt behandlingsmål
Avgörande var att när forskarna blockerade TGF-β föll fördelarna som APOA2 gav samman. Att hämma denna signal i musmodeller minskade de onormala kärlförändringarna, återställde känsligheten för behandling och bromsade tumörtillväxten. Ännu mer lovande var att en dubbelantikropp som samtidigt blockerar TGF-β och immuncheckpointen PD-1 fungerade bättre än vardera strategin ensam i APOA2-höga tumörer. Dessa resultat tyder på att i en undergrupp av levercancer markerad av hög APOA2 har sjukdomen tyst bytt sitt beroende från den vanliga VEGF-vägen till en TGF-β-centrerad bana som upprätthåller både blodkärl och tumörmetabolism.
Vad detta innebär för framtida levercancervård
För en lekman är huvudbudskapet att vissa levertumörer undkommer dagens kärl-riktade läkemedel genom att omkoppla både sin ”rördragning” och sin energiförsörjning. Ett fettassocierat protein, APOA2, skruvar upp TGF-β-signalen, som i sin tur förkläder blodkärlen så att befintliga läkemedel inte längre känner igen dem och lär cancercellerna att leva på fett i stället för socker. Studien antyder att analys av tumörer för APOA2-nivåer skulle kunna identifiera patienter som sannolikt inte får nytta av standard antiangiogen terapi men som kan svara på läkemedel som blockerar TGF-β, särskilt i kombination med modern immunterapi. Kort sagt, genom att avslöja hur tumörer anpassar sig pekar detta arbete på en mer skräddarsydd strategi som angriper både kärlen och energikällan som dessa tåliga cancerformer är beroende av.
Citering: Zhang, S., Fu, Z., Zhu, F. et al. APOA2-mediated endothelial mesenchymal transition and cancer lipid metabolism reprogramming confers antiangiogenic drug resistance through TGF-β. Cell Death Discov. 12, 119 (2026). https://doi.org/10.1038/s41420-026-02984-5
Nyckelord: hepatocellulärt karcinom, resistens mot antiangiogenes, APOA2, TGF-beta signalering, cancerlipidmetabolism